Каким свойством углерода объясняется то что
Óãëåðîä (Ñ) íàõîäèòñÿ â IV ïîäãðóïïå ïåðèîäè÷åñêîé òàáëèöû Ä.È. Ìåíäåëååâà. Íà âíåøíåì óðîâíå 4 íåñïàðåííûõ ýëåêòðîíà. Óãëåðîä – íåìåòàëë. Îáëàäàåò âîññòàíîâèòåëüíûìè ñâîéñòâàìè.
Àëëîòðîïèÿ óãëåðîäà.
Óãëåðîä ñóùåñòâóåò â íåñêîëüêèõ àëëîòðîïíûõ ìîäèôèêàöèÿõ:
— ãðàôèò (èìååò ñëîèñòóþ ñòðóêòóðó, î÷åíü ïëàñòè÷åí),
— àëìàç (ñàìîå òâåðäîå ñîåäèíåíèå),
— Ñ60 (ôóëëåðåí).
Èç ãðàôèòà ìîæíî ïîëó÷èòü àëìàç ïóòåì äëèòåëüíîãî íàãðåâà ïðè âûñîêèì äàâëåíèåì. È àëìàç è ãðàôèò èìåþò ðàçëè÷íûå êðèñòàëëè÷åñêèå ðåøåòêè, âñëåäñòâèå ÷åãî íàáëþäàþòñÿ ðàçëè÷èÿ â ñâîéñòâàõ.
Õèìè÷åñêèå ñâîéñòâà óãëåðîäà.
1. Âçàèìîäåéñòâèå ñ êèñëîðîäîì:
Ñ + Î2 + ÑÎ2,
 íåäîñòàòêå êèñëîðîäà îáðàçóþòñÿ ìîíîîêñèäû:
2Ñ +Î2 = 2ÑÎ,
2. Ñî ñëîæíûìè âåùåñòâàìè:
Ñ + Î2 = 2ÑÎ,
Ñ + ÑÎ2 = 2ÑÎ,
3. Ïðè îáû÷íîé òåìïåðàòóðå âçàèìîäåéñòâóåò ñî ôòîðîì, ïðè íàãðåâàíèè – ñ õëîðîì, ñåðîé è àçîòîì:
4C + S8 = 4CS2,
2C + N2 = C2N2,
Ñ êðåìíèåì óãëåðîä îáðàçóåò êàáðîðóíä – ñîåäèíåíèå ïî òâåðäîñòè ñðàâíèìîå ñ àëìàçîì:
Si + C = SiC,
4. Ðàçáàâëåííûå êèñëîòû íå äåéñòâóþò íà óãëåðîä, à êîíöåíòðèðîâàííûå îêèñëÿþò:
C + 2H2SO4 = CO2 + 2SO2 + 2H2O,
5. Óãëåðîä ó÷àñòâóåò â ðåàêöèÿõ â êà÷åñòâå âîññòàíîâèòåëÿ:
CuO + C = C + CO,
6. Ïðè íàãðåâå âçàèìîäåéñòâóåò ñ îêñèäàìè àêòèâíûõ ìåòàëëîâ, îáðàçóÿ êàðáèäû:
CaO + 3C = CaC2 + CO,
7. Ïðè âçàèìîäåéñòâèè ñ ìåòàëëàìè óãëåðîä âûñòóïàåò â êà÷åñòâå îêèñëèòåëÿ:
Ca + 2C = CaC2.
Êàëüêóëÿòîðû ïî õèìèè | |
| Õèìèÿ îíëàéí íà íàøåì ñàéòå äëÿ ðåøåíèÿ çàäà÷ è óðàâíåíèé. | |
| Êàëüêóëÿòîðû ïî õèìèè | |
Õèìè÷åñêèå ýëåìåíòû | |
| Õèìè÷åñêèå ýëåìåíòû Ïåðèîäè÷åñêîé ñèñòåìû Ìåíäåëååâà, ñâîéñòâà, âàëåíòíîñòü õèìè÷åñêèõ ýëåìåíòîâ | |
| Õèìè÷åñêèå ýëåìåíòû | |
Õèìèÿ 7,8,9,10,11 êëàññ, ÅÃÝ, ÃÈÀ | |
| Îñíîâíàÿ èíôîðìàöèÿ ïî êóðñó õèìèè äëÿ îáó÷åíèÿ è ïîäãîòîâêè â ýêçàìåíàì, ÃÂÝ, ÅÃÝ, ÎÃÝ, ÃÈÀ | |
| Õèìèÿ 7,8,9,10,11 êëàññ, ÅÃÝ, ÃÈÀ | |
Ñîåäèíåíèÿ õèìè÷åñêèõ ýëåìåíòîâ | |
| Àëêàíû, âîäà, ãàëîãåíû, ìûëà, æèðû, ãèäðîêñèäû; îêñèäû, õëîðèäû, ïðîèçâîäíûå õèìè÷åñêèõ ýëåìåíòîâ òàáëèöû Ìåíäåëååâà | |
| Ñîåäèíåíèÿ õèìè÷åñêèõ ýëåìåíòîâ | |
Âîäà. Ñâîéñòâà âîäû. | |
| Âîäà íàèáîëåå øèðîêî ðàñïðîñòðàí¸ííîå ñîåäèíåíèå íà íàøåé ïëàíåòå. | |
| Âîäà. Ñâîéñòâà âîäû. | |
Éîä. Ñâîéñòâà éîäà. | |
| Éîä ( I 2 ) íàõîäèòñÿ â 7-îé ãðóïïå ïåðèîäè÷åñêîé òàáëèöû Ä. | |
| Éîä. Ñâîéñòâà éîäà. | |
Ali Elaidy · 17 июня 2019
< 100
TutorOnline — одна из крупнейших онлайн-школ. Мы преподаем более 150 предметов… · tutoronline.ru
Атом углерода в органических соединениях имеет валентность четыре. Это объясняется с позиции теории гибридизации. Атом углерода переходит в возбужденное состояние 2s1 2p3. Одна s орбиталь и три p орбитали смешиваются, образую четыре гибридныеиорбитали, одинаковые по форме и энергии. Эти гибридные орбитали далее участвуют в образовании химических связей в молекулах органических веществ.
Для каких элементов характерны летучие водородные соединения?
Автор проекта ChemistryToday, человек, заинтересованный химией и продвигающий… · vk.com/chemtoday
Летучие водородные соединения (ЛВС) образуют, в основном, неметаллы: практически у каждого из них есть такие соединения — гидриды элемента или элемент’иды водорода.
Посмотрим на 2 период Таблицы Менделеева: ЛВС характерны для бора (различные бораны BnHm), углерода (вся органика! CxHy), азота (аммиак, например NH3), кислорода (вода!) и фтора (плавиковая кислота HF). Это как раз все неметаллы 2 периода (за исключением неона, благородного газа).
В 3 периоде всё то же самое: алюминий образует AlH3, алан, кремний — силан SiH4, фосфор — фосфин PH3, сера — сероводород H2S, хлор — хлороводород HCl.
Но так как при движении вниз по группе «металличность» элементов повышается, то для галлия (который под алюминием) уже гораздо менее характерно образование водородных соединений, тем более летучих, поэтому галлий уже выбывает из ЛВС неметаллов 4 периода. Следующий за ним — германий — образует герман GeH4, мышьяк — арсин AsH3, селен — селеноводород H2Se, бром — бромоводород HBr.
Все остальные также существуют: PbH4, SnH4, H2Te, SbH3, BiH3 (очень нестабилен), HI, HAt, H2Po.
Почему наша форма жизни именуется углеродной, а не, например, кислородной, и какие ещё формы жизни могут теоретически существовать?
Researcher, Institute of Physics, University of Tartu
Живые организмы состоят в основном из органических соединений (и воды). Органические соединения — это, собственно, соединения углерода (за исключением карбидов, карбонатов и еще некоторого количества соединений углерода, которые относятся к неорганическим веществам). Отсюда и термин «углеродные формы жизни». Возможно, более правильно было бы назвать это «углеводородной» жизнью, но это уже вопрос терминологии.
Почему именно органические соединения? Жизнь в принципе можно представить как совокупность химических процессов и в этом смысле органические соединения стали основой жизни благодаря тому, что их химия достаточно сложна и разнообразна. Во-первых, структурные характеристики: возможность построения сложных и разветвленных многофункциональных молекул, гомологические ряды, позволяющие тонко настраивать свойства этих молекул, разнообразие функциональных групп. Во-вторых, сами функциональные возможности: органические соединения могут быть и окислителями и восстановителями и кислотами и основаниями, вступать в реакции присоединения, отщепления, обмена, практически в любые типы реакций, собственно говоря. В-третьих, соответствие условиям окружающей среды: два основных источника энергии для жизни на Земле — это солнечный свет и кислород, органические соединения с одной стороны открывают богатые возможности по фотосинтезу, а с другой — способны участвовать в обратимых процессах окисления/восстановления с кислородом (очень важно, что обратимых, поскольку иначе живые организмы сгорали бы или сгнивали при взаимодействии с кислородом).
Соответственно, из этого видно, какие требования могут быть к другим «базовым» элементам жизни. Строго говоря, тут многое зависит от внешних условий. В близких к земным условиях я лично не вижу возможности существования неуглеродной жизни, а если фантазировать произвольные условия, то многие р-элементы могли бы стать основой жизни. И кремний и фосфор, наверное, и бор и сера. В общем любой элемент, способный образовывать структурно-сложные соединения. Дальше можно фантазировать, что могло бы играть роль «кислорода», а что «водорода» для этого базового элемента и т.д. Кремний нравится фантастам за то, что он близок по многим свойствам к углероду. Но что было бы для него «кислородом»? Может быть, хлор? А «водородом»? Возможно, тот же водород. Ну, в общем это уже бессмысленное фантазирование, для начала нужно задать условия внешней среды.
Прочитать ещё 2 ответа
Как были получены пространственные модели электронных орбиталей?
Researcher, Institute of Physics, University of Tartu
Я сам не большой специалист в квантовой механике, но если самым примитивным и приближенным способом объяснять, то орбиталь представляет собой область пространства, в которой вероятность нахождения электрона больше 90-95%. Как известно, плотность вероятности нахождения электронов в данной точке определяется квадратом модуля волновых функций этих электронов. Если взять радиальную функцию распределения вероятности нахождения электрона в сферических координатах, то она будет выглядеть как
Wr = 4πr2|ψ|2dr
где r — это радиальная координата, то есть в нашем случае расстояние от ядра (а 2 — это возведение в квадрат здесь и далее тоже, верхние индексы не получаются здесь). Таким образом, чтобы определить форму орбитали некоторого электрона необходимо решить для него уравнение Шредингера. Формы орбиталей — это результат решения уравнения Шредингера в приближении одноэлектронной модели (потенциальная энергия электрона E = −e2 / r). Данное приближение означает, что разные электроны одного атома между собой не взаимодействуют. Это достаточно грубое приближение, но зато при таком потенциале можно получить решение уравнение Шредингера, то есть получить аналитическое выражение для волновой функции электрона.
ψ(x,y,z) = R(r) Θ(θ) Φ(φ)
Это выражение, как видно, получается тоже в сферических координатах, при этом радиальная и угловые составляющие функции зависят от квантовых чисел. Именно в связи с этим у s, p, d, f и т.д. орбиталей разные формы, равно как и у разных p, d, f орбиталей тоже разные формы, поскольку форму определяют все квантовые числа, кроме спинового, а не только главное.
Показать, каким образом получаются именно такие формы, какие получаются, для чего угодно, кроме 1s орбитали, будет достаточно зубодробительно, я не возьмусь, но суть такая.
Углерод — химический элемент № (6). Он расположен в IVА группе Периодической системы.
C6+6)2e)4e
На внешнем слое атома углерода содержатся четыре валентных электрона, и до его завершения не хватает четырёх электронов. Поэтому в соединениях с металлами углероду характерна степень окисления (–4), а при взаимодействии с более электроотрицательными неметаллами он проявляет положительные степени окисления: ( +2) или (+4).
В природе углерод встречается как в виде простых веществ, так и в виде соединений. В воздухе содержится углекислый газ. В земной коре распространены карбонаты (например, CaCO3 образует мел, мрамор, известняк). Горючие ископаемые (уголь, торф, нефть, природный газ) состоят из органических соединений, главным элементом которых является углерод.
Углерод относится к жизненно важным элементам, так как входит в состав молекул всех органических веществ.
Углерод образует несколько аллотропных видоизменений, из которых наиболее известны алмаз и графит.
Алмаз имеет атомную кристаллическую решётку. Каждый атом углерода в алмазе связан четырьмя прочными ковалентными связями с соседними атомами, расположенными в вершинах тетраэдра.
Благодаря такому строению алмаз — самое твёрдое из известных природных веществ. Все четыре валентных электрона каждого атома углерода участвуют в образовании связей, поэтому алмаз не проводит электрический ток. Это бесцветное прозрачное кристаллическое вещество, хорошо преломляющее свет.
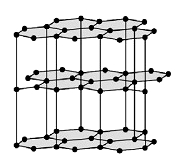
Графит тоже имеет атомную кристаллическую решётку, но устроена она иначе. Решётка графита слоистая. Каждый атом углерода соединён прочными ковалентными связями с тремя соседними атомами. Образуются плоские слои из шестиугольников, которые между собой связаны слабо. Один валентный электрон у атома углерода остаётся свободным.
Графит представляет собой тёмно-серое вещество с металлическим блеском, жирное на ощупь. В отличие от алмаза графит непрозрачный, проводит электрический ток и оставляет серый след на бумаге. У графита очень высокая температура плавления ((3700) °С).
Алмаз и графит взаимопревращаемы. При сильном нагревании без доступа воздуха алмаз чернеет и превращается в графит. Графит можно превратить в алмаз при высокой температуре и большом давлении.
Из мельчайших частиц графита состоят сажа, древесный уголь и кокс. Сажа образуется при неполном сгорании топлива. Древесный уголь получают при нагревании древесины без доступа воздуха, а кокс — переработкой каменного угля.
Древесный уголь имеет пористое строение и обладает способностью поглощать газы и растворённые вещества. Такое свойство называется адсорбцией.
Аллотропные модификации углерода в химических реакциях могут проявлять и окислительные, и восстановительные свойства. Окислительные свойства углерода выражены слабее, чем у других неметаллов второго периода (азота, кислорода и фтора).
- Взаимодействие с металлами.
Углерод реагирует с металлами при высокой температуре с образованием карбидов:
4Al0+3C0=tAl+34C−43.
В этой реакции углерод выступает как окислитель.
- Взаимодействие с водородом.
Реакция происходит при сильном нагревании. Образуется метан. Углерод — окислитель.
C0+2H02=tC−4H+14.
- Взаимодействие с кислородом.
Углерод горит в кислороде с образованием углекислого газа и проявляет в этой реакции восстановительные свойства:
C0+O02=tC+4O−22.
- Взаимодействие с оксидами металлов.
Углерод способен восстанавливать металлы из их оксидов:
2Cu+2O+C0=t2Cu0+C+4O2.
Применение простых веществ
Алмаз применяется:
- для обработки твёрдых поверхностей;
- для резки стекла;
- для изготовления буров и свёрл;
- для изготовления ювелирных украшений.
Графит используется:
- при изготовлении карандашей;
- как твёрдая смазка в подшипниках;
- для изготовления электродов;
- в качестве замедлителя нейтронов в ядерных реакторах;
- для получения искусственных алмазов.
Сажа:
- входит в состав типографской краски, крема для обуви;
- используется как наполнитель для производства резины.
Уголь используется:
- в противогазах, промышленных и бытовых фильтрах;
- для очистки сахарного сиропа, спирта и т. д.;
- в медицине.
Кокс применяется в металлургической промышленности.

- Обозначение — C (Carbon);
- Период — II;
- Группа — 14 (IVa);
- Атомная масса — 12,011;
- Атомный номер — 6;
- Радиус атома = 77 пм;
- Ковалентный радиус = 77 пм;
- Распределение электронов — 1s22s22p2;
- t плавления = 3550°C;
- t кипения = 4827°C;
- Электроотрицательность (по Полингу/по Алпреду и Рохову) = 2,55/2,50;
- Степень окисления: +4, +3, +2, +1, 0, -1, -2, -3, -4;
- Плотность (н. у.) = 2,25 г/см3 (графит);
- Молярный объем = 5,3 см3/моль.
Соединения углерода:
- Оксиды углерода CO, CO2
- Угольная кислота H2CO3 и ее соли
Углерод в виде древесного угля известен человеку с незапамятных времен, поэтому, о дате его открытия говорить не имеет смысла. Собственно свое название «углерод» получил в 1787 году, когда была опубликована книга «Метод химической номенклатуры», в которой вместо французского названия «чистый уголь» (charbone pur) появился термин «углерод» (carbone).
Углерод обладает уникальной способностью образовывать полимерные цепочки неограниченной длины, порождая тем самым огромный класс соединений, изучением которых занимается отдельный раздел химии — органическая химия. Органические соединения углерода лежат в основе земной жизни, поэтому, о важности углерода, как химического элемента, говорить не имеет смысла — он основа жизни на Земле.
Сейчас рассмотрим углерод с точки зрения неорганической химии.
Углерод в Периодической таблице химических элементов Д. И. Менделеева, стоит под номером «6», относится к 14(IVa) группе (См. Атомы 14(IVa) группы).
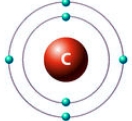
Рис. Строение атома углерода.
Электронная конфигурация углерода — 1s22s22p2 (см. Электронная структура атомов). На внешнем энергетическом уровне у углерода находятся 4 электрона: 2 спаренных на s-подуровне + 2 неспаренных на p-орбиталях. При переходе атома углерода в возбужденное состояние (требует энергетических затрат) один электрон с s-подуровня «покидает» свою пару и переходит на p-подуровень, где имеется одна свободная орбиталь. Т. о., в возбужденном состоянии электронная конфигурация атома углерода приобретает следующий вид: 1s22s12p3.
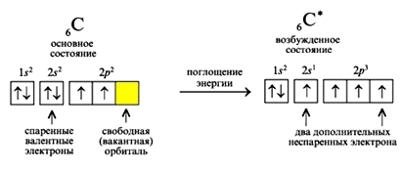
Рис. Переход атома углерода в возбужденное состояние.
Такая «рокировка» существенно расширяет валентные возможности атомов углерода, которые могут принимать степень окисления от +4 (в соединениях с активными неметаллами) до -4 (в соединениях с металлами).
В невозбужденном состоянии атом углерода в соединениях имеет валентность 2, например, CO(II), а в возбужденном — 4: CO2(IV).
«Уникальность» атома углерода заключается в том, что на его внешнем энергетическом уровне находятся 4 электрона, поэтому, для завершения уровня (к чему, собственно, стремятся атомы любого химического элемента) он может с одинаковым «успехом», как отдавать, так и присоединять электроны с образованием ковалентных связей (см. Ковалентная связь).
Углерод, как простое вещество
Как простое вещество углерод может находиться в виде нескольких аллотропных модификаций:
- Алмаз
- Графит
- Фуллерен
- Карбин
Алмаз
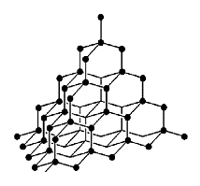
Рис. Кристаллическая решетка алмаза.
Свойства алмаза:
- бесцветное кристаллическое вещество;
- самое твердое вещество в природе;
- обладает сильным преломляющим эффектом;
- плохо проводит тепло и электричество.
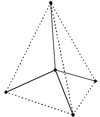
Рис. Тетраэдр алмаза.
Исключительная твердость алмаза объясняется строением его кристаллической решетки, которая имеет форму тетраэдра — в центре тетраэдра находится атом углерода, который связан равноценно прочными связями с четырьмя соседними атомами, образующими вершины тетраэдра (см. рисунок выше). Такая «конструкция» в свою очередь связана с соседними тетраэдрами.
Графит

Рис. Кристаллическая решетка графита.
Свойства графита:
- мягкое кристаллическое вещество серого цвета слоистой структуры;
- обладает металлическим блеском;
- хорошо проводит электричество.
В графите атомы углерода образуют правильные шестиугольники, лежащие в одной плоскости, организованные в бесконечные слои.
В графите химические связи между соседними атомами углерода образованы за счет трех валентных электронов каждого атома (изображены синим цветом на рисунке ниже), при этом четвертый электрон (изображен красным цветом) каждого атома углерода, расположенный на p-орбитали, лежащей перпендикулярно плоскости слоя графита, не участвует в образовании ковалентных связей в плоскости слоя. Его «предназначение» заключается в другом — взаимодействуя со своим «собратом», лежащим в соседнем слое, он обеспечивает связь между слоями графита, а высокая подвижность p-электронов обусловливает хорошую электропроводность графита.
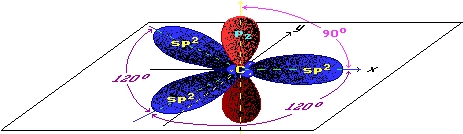
Рис. Распределение орбиталей атома углерода в графите.
Фуллерен
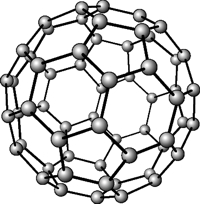
Рис. Кристаллическая решетка фуллерена.
Свойства фуллерена:
- молекула фуллерена представляет собой совокупность атомов углерода, замкнутых в полые сферы типа футбольного мяча;
- это мелкокристаллическое вещество желто-оранжевого цвета;
- температура плавления = 500-600°C;
- полупроводник;
- входит в состав минерала шунгита.
Карбин
Свойства карбина:
- инертное вещество черного цвета;
- состоит из полимерных линейных молекул, в которых атомы связаны чередующимися одинарными и тройными связями;
- полупроводник.
Химические свойства углерода
При нормальных условиях углерод является инертным веществом, но при нагревании может реагировать с разнообразными простыми и сложными веществами.
Выше уже было сказано, что на внешнем энергетическом уровне углерода находится 4 электрона (ни туда, ни сюда), поэтому углерод может, как отдавать электроны, так и принимать их, проявляя в одних соединениях восстановительные свойства, а в других — окислительные.
Углерод является восстановителем в реакциях с кислородом и другими элементами, имеющими более высокую электроотрицательность (см. таблицу электроотрицательности элементов):
- при нагревании на воздухе горит (при избытке кислорода с образованием углекислого газа; при его недостатке — оксида углерода(II)):
C + O2 = CO2;
2C + O2 = 2CO. - реагирует при высоких температурах с парами серы, легко взаимодействует с хлором, фтором:
C + 2S = CS2
C + 2Cl2 = CCl4
2F2 + C = CF4 - при нагревании восстанавливает из оксидов многие металлы и неметаллы:
C0 + Cu+2O = Cu0 + C+2O;
C0+C+4O2 = 2C+2O - при температуре 1000°C реагирует с водой (процесс газификации), с образованием водяного газа:
C + H2O = CO + H2;
Углерод проявляет окислительные свойства в реакциях с металлами и водородом:
- реагирует с металлами с образованием карбидов:
Ca + 2C = CaC2 - взаимодействуя с водородом, углерод образует метан:
C + 2H2 = CH4
Углерод получают термическим разложением его соединений или пиролизом метана (при высокой температуре):
CH4 = C + 2H2.
Применение углерода
Соединения углерода нашли самое широкое применение в народном хозяйстве, перечислить все их не представляется возможным, укажем только некоторые:
- графит применяется для изготовления грифелей карандашей, электродов, плавильных тиглей, как замедлитель нейтронов в ядерных реакторах, как смазочный материал;
- алмазы применяются в ювелирном деле, в качестве режущего инструмента, в буровом оборудовании, как абразивный материал;
- в качестве восстановителя углерод используют для получения некоторых металлов и неметаллов (железа, кремния);
- углерод составляет основную массу активированного угля, который нашел широчайшее применение, как в быту (например, в качестве адсорбента для очистки воздуха и растворов), так и в медицине (таблетки активированного угля) и в промышленности (в качестве носителя для каталитических добавок, катализатора полимеризации и проч.).
