Каким свойством обладает поверхностный слой жидкости
Лекция 11.Характеристика жидкого состояния вещества. Поверхностный слой жидкости. Энергия поверхностного слоя. Явления на границе жидкости с твердым телом. Капиллярные явления.
ХАРАКТЕРИСТИКА ЖИДКОГО СОСТОЯНИЯ ВЕЩЕСТВА
Жидкость — это агрегатное состояние вещества, промежуточное между газообразным и твердым.
Вещество в жидком состоянии сохраняет свой объем, но принимает форму сосуда, в котором оно находится Сохранение объема у жидкости доказывает, что между ее молекулами действуют силы притяжения.
Если вокруг молекулы жидкости описать сферу молекулярного действия, то внутри этой сферы окажутся центры многих других молекул, которые будут взаимодействовать с нашей молекулой. Эти силы взаимодействия удерживают молекулу жидкости около ее временного положения равновесия примерно в течение 10-12-10-10 с, после чего она перескакивает в новое временное положение равновесия приблизительно на расстояние своего диаметра. Молекулы жидкости между перескоками совершают колебательное движение около временного положения равновесия.
Время между двумя перескоками молекулы из одного положения в другое называется временем оседлой жизни.
Это время зависит от вида жидкости и от температуры. При нагревании жидкости среднее время оседлой жизни молекул уменьшается.
Итак, в небольшом объеме жидкости наблюдается упорядоченное расположение ее молекул, а в большом объеме оно оказывается хаотическим. В этом смысле говорят, что в жидкости существует ближний порядок в расположении молекул и отсутствует дальний порядок. Такое строение жидкости называют квазикристаллическим (кристаллоподобным).
СВОЙСТВА ЖИДКОСТИ
1.Если время действия силы на жидкость мало, то жидкость проявляет упругие свойства. Например, при резком ударе палкой о поверхность воды палка может вылететь из руки или сломаться; камень можно бросить так, что он при ударе о поверхность воды отскакивает от нее, и лишь совершив несколько скачков, тонет в воде.
2. Если же время воздействия на жидкость велико, то вместо упругости проявляется текучесть жидкости. Например, рука легко проникает внутрь воды.
3. При кратковременном действии силы на струю жидкости последняя обнаруживает хрупкость. Прочность жидкости нд разрыв хотя и меньше, чем у твердых веществ, но мало уступает им по величине. Для воды она составляет 2,5-107 Н/м2.
4.Сжимаемость жидкости тоже очень мала, хотя она и больше, чем у этих же веществ в твердом состоянии. Например, при увеличении давления на 1 атм объем воды уменьшается на 50 миллионных долей.
Разрывы внутри жидкости, в которой нет посторонних веществ, например воздуха, могут получаться только при интенсивном воздействии на жидкость, например при вращении гребных винтов в воде, при распространении в жидкости ультразвуковых волн . Такого рода пустоты внутри жидкости долго существовать не могут и резко захлопываются, т. е. исчезают. Это явление называют кавитацией (от греческого «кавитас» – полость). Оно служит причиной быстрого износа гребных винтов.
ПОВЕРХНОСТНЫЙ СЛОЙ ЖИДКОСТИ
Среднее значение равнодействующей молекулярных сил притяжения, приложенных к молекуле, которая находится внутри жидкости (рис. 2), близко к нулю. Случайные флуктуации этой равнодействующей заставляют молекулу совершать лишь хаотическое движение внутри жидкости. Несколько иначе обстоит дело с молекулами, находящимися в поверхностном слое жидкости.
Опишем вокруг молекул сферы молекулярного действия радиусом R(порядка 10-8 м). Тогда для верхней молекулы в нижней полусфере окажется много молекул, а в верхней – значительно меньше, так как снизу находится жидкость, а сверху – пар и воздух. Поэтому для верхней молекулы равнодействующая молекулярных сил притяжения в нижней полусфере много больше равнодействующей молекулярных сил в верхней полусфере.
Таким образом, все молекулы жидкости, находящиеся в поверхностном слое толщиной, равной радиусу молекулярного действия, втягиваются внутрь жидкости. Но пространство внутри жидкости занято другими молекулами, поэтому поверхностный слой создает давление на жидкость, которое называют молекулярным давлением.
Силы, действующие в горизонтальной плоскости, стягивают поверхность жидкости. Они называются силами поверхностного натяжения
Поверхностное натяжение — физическая величина, равная отношению силы F поверхностного натяжения, приложенной к границе поверхностного слоя жидкости и направленной по касательной к поверхности, к длине l этой границы:
Единица поверхностного натяжения – ньютон на метр (Н/м).
Поверхностное натяжение различно для разных жидкостей и зависит от температуры.
Обычно поверхностное натяжение уменьшается с возрастанием температуры и при критической температуре, когда плотность жидкости и пара одинаковы, поверхностное натяжение жидкости равно нулю.
Вещества, которые уменьшают поверхностное натяжение, называют поврхностно – активными (спирт, мыло, стиральный порошок)
Чтобы увеличить площадь поверхности жидкости требуется выполнить работу против поверхностного натяжения.
Имеется другое определение коэффициента поверхностного натяжения — энергетическое. Оно исходит из того, что если площадь поверхности жидкости увеличивается, то некоторое количество молекул из ее объема поднимается на слой поверхности. С этой целью внешние силы совершают работу против молекулярных сил сцепления молекул. Величина данной работы будет пропорциональна изменению площади поверхности жидкости:
Коэффициент пропорциональности σ и называется поверхностным натяжением жидкости.
Выведем единицу поверхностного, натяжения а в СИ: о=1 Дж/1 м2= 1 Дж/м2.
Поверхностный слой жидкости обладает
особыми свойствами. Молекулы жидкости в этом слое находятся в непосредственной
близости от другой фазы – газа. Молекула, расположенная вблизи границы раздела жидкость
– газ, имеет ближайших соседей только с одной стороны, поэтому сложение всех
сил, действующих на эту молекулу, дает равнодействующую, направленную внутрь
жидкости. Следовательно, любая молекула жидкости, находящаяся вблизи свободной
поверхности, имеет избыток потенциальной энергии, по сравнению с молекулами,
находящимися внутри.

Для того чтобы перевести молекулу из
объема жидкости на поверхность, необходимо совершить работу. При увеличении
поверхности определенного объема жидкости внутренняя энергия жидкости
увеличивается. Эта составляющая внутренней энергии пропорциональна площади
поверхности жидкости и называется поверхностной энергией. Величина
поверхностной энергии зависит от сил молекулярного взаимодействия и количества
ближайших соседних молекул. Для различных веществ поверхностная энергия
принимает разные значения. Энергия поверхностного слоя жидкости пропорциональна
его площади: Е= σ ·Ѕ
Величина силы F, действующей на единицу длины границы поверхности,
определяет поверхностное натяжение жидкости: σ =F/L; σ- коэффициент поверхностного натяжения жидкости, Н/м.
Проще всего уловить характер сил
поверхностного натяжения, наблюдая образование капли у неплотно закрытого
крана. Всмотритесь внимательно, как постепенно растет капля, образуется сужение
— шейка и капля отрывается. Поверхностный слой воды ведет себя, как растянутая
эластичная пленка.
Можно осторожно положить швейную иглу на поверхность воды. Поверхностная
пленка прогнется и не даст игле утонуть.

По этой же причине легкие насекомые – водомерки могут быстро скользить по поверхности воды. Прогиб пленки не позволяет выливаться воде, осторожно налитой в достаточно частое решето.Ткань – это то же решето, образованное переплетением нитей. Поверхностное натяжение сильно затрудняет просачивание воды сквозь нее, и поэтому ткань не промокает мгновенно. Благодаря силам поверхностного натяжения происходит образование пены.
Изменение поверхностного натяжения
При соприкосновении жидкости с твердым телом наблюдается явление смачивания или несмачивания. Если силы
взаимодействия между молекулами жидкости и твердого тела больше, чем между
молекулами жидкости, то жидкость растекается по поверхности твердого тела, т.е.
смачивает и наоборот, если силы взаимодействия между молекулами жидкости
больше, чем между молекулами жидкости и твердого тела, то жидкость собирается в
каплю и не смачивает поверхность жидкости.
Капиллярные явления.
В природе часто встречаются тела, имеющие пористое строение (пронизаны множеством мелких каналов). Такую структуру имеют бумага, кожа, дерево, почва, многие строительные материалы. Вода или другая жидкость, попадая на такое твердое тело, может впитываться в него, поднимаясь вверх на большую высоту. Так поднимается влага в стеблях растений, керосин поднимается по фитилю, ткань впитывает влагу. Такие явления называются капиллярными.

В узкой цилиндрической
трубке смачивающая жидкость за счет сил молекулярного взаимодействия
поднимается вверх, принимая вогнутую форму. Под вогнутой поверхностью появляется
дополнительное давление, направленное вверх, в связи с чем уровень жидкости в
капилляре выше уровня свободной поверхности. Несмачивающая же жидкость
принимает выпуклую поверхность. Под выпуклой поверхностью жидкости возникает
обратное дополнительное давление, направленное вниз, так что уровень жидкости с
выпуклым мениском ниже, чем уровень свободной поверхности.
Величина добавочного
давления равна p= 2 σ / R
Жидкость в капилляре
поднимается на такую высоту, чтобы давление столба жидкости уравновесило
избыточное давление. Высота подъема жидкости в капилляре равна: h = 2 σ / ρgr

Явление смачивания применяют при обогащении
руд. Суть обогащения состоит в отделении пустой породы от полезных ископаемых.
Этот способ носит название флотации (флотация – всплывание). Раздробленную в
мелкий порошок руду взбалтывают в воде, в которую добавлено небольшое
количество жидкости, смачивающей полезную руду, например масло. Вдувая в эту
смесь воздух, можно отделить обе составляющие. Покрытые пленкой кусочки полезной
руды, прилипая к пузырькам воздуха, поднимутся вверх, а порода осядет на дно.
Адсорбция — явление
аналогичное смачиванию, наблюдается при соприкосновении твердой и газообразной
фаз. Если силы взаимодействия между молекулами твердого тела и газа велики, то
тело покрывается слоем молекул газа. Большой адсорбционной способностью
обладают пористые вещества. Свойство активированного угля адсорбировать большое
количество газа используют в противогазах, в химической промышленности, в
медицине.
Значение
поверхностного натяжения
Понятие поверхностного
натяжения впервые ввел Я. Сегнер (1752). В 1-й половине 19 в. на основе
представления о поверхностном натяжении была развита математическая теория
капиллярных явлений (П. Лаплас, С. Пуассон, К. Гаусс, А.Ю. Давидов). Во 2-й
половине 19 в. Дж. Гиббс развил термодинамическую теорию поверхностных явлений,
в которой решающую роль играет поверхностное натяжение. Среди современных
актуальных проблем — развитие молекулярной теории поверхностного натяжения различных
жидкостей, включая расплавленные металлы. Силы поверхностного натяжения играют
существенную роль в явлениях природы, биологии, медицине, в различных
современных технологиях, полиграфии, технике, в физиологии нашего организма. Без этих сил мы не могли бы писать чернилами.
Обычная ручка не зачерпнула бы чернил из чернильницы, а автоматическая сразу же
поставила бы большую кляксу, опорожнив весь свой резервуар. Нельзя было бы
намылить руки: пена не образовалась бы. Нарушился бы водный режим почвы, что оказалось
бы гибельным для растений. Пострадали бы важные функции нашего организма.
Проявления сил поверхностного натяжения столь многообразны, что даже
перечислить их все нет возможности.
В медицине измеряют
динамическое и равновесное поверхностное натяжение сыворотки венозной крови, по
которым можно диагностировать заболевание и вести контроль над проводимым
лечением. Установлено, что вода с низким поверхностным натяжением биологически
более доступна. Она легче вступает в молекулярные взаимодействия, тогда клеткам
не надо будет тратить энергию на преодоление поверхностного натяжения.
Непрерывно растут объёмы
печати на полимерных плёнках благодаря бурному развитию упаковочной индустрии,
высокому спросу на потребительские товары в красочной полимерной упаковке.
Важное условие грамотного внедрения подобных технологий — точное определение
условий их применения в полиграфических процессах. В полиграфии обработка
пластика перед печатью необходима для того, чтобы краска ложилась на материал.
Причина заключается в поверхностном натяжении материала. Результат определяется
тем, как жидкость смачивает поверхность изделия. Смачивание считается
оптимальным, когда капля жидкости остается там же, где она была нанесена. В
других случаях жидкость может скатываться в каплю, либо, наоборот, растекаться.
Оба случая в равной степени приводят к отрицательным результатам во время
переноса краски.
Некоторые выводы:
1. Жидкость может смачивать и не смачивать твёрдое тело.
2. Коэффициент поверхностного натяжения зависит от рода жидкости.
3. Коэффициент поверхностного натяжения зависит от температуры .T ↑σ ↓
4. Высота подъёма жидкости в капилляре зависит от его диаметра. d ↑ h ↓
5. Сила поверхностного натяжения зависит от длины свободной поверхности жидкости. l ↑ F ↑

Вещество, находящееся в жидком состоянии, характеризуется крайне плотным расположением молекул друг относительно друга. Отличаясь от твердых кристаллических тел, чьи молекулы формируют упорядоченные структуры по всему объему кристалла и ограничены в своих тепловых колебаниях фиксированными центрами, молекулы жидкости обладают значительной степенью свободы. Любая конкретная молекула жидкого вещества, как это происходит и в твердых телах, «зажата» соседними молекулами и может совершать тепловые колебания поблизости с некоторым положением равновесия. Несмотря на это, в какой-то момент, любая молекула может переместиться на соседнее вакантное место. Подобные перемещения в жидкостях происходят довольно часто, благодаря чему молекулы не привязаны к конкретным центрам, как в кристаллах, а имеют возможность перемещаться по всему объему жидкости. Именно на этом факте основывается текучесть жидкостей.
Определение 1
По причине сильного взаимодействия между близко расположенными молекулами они могут образовывать локальные, то есть неустойчивые, упорядоченные группы, включающие в себя несколько молекул. Данное явление носит название ближнего порядка (рис. 3.5.1).
Рисунок 3.5.1. Пример ближнего порядка молекул жидкости и дальнего порядка молекул кристаллического вещества: 1 – вода; 2 – лед.
Свойства жидкостей
На рисунке 3.5.2, на примере воды, проиллюстрировано различие между газообразным веществом и жидкостью. Молекула воды H2O включает в свой состав один атом кислорода и два атома водорода, которые расположены под углом 104°. В среднем, расстояние между молекулами пара в десятки раз больше, чем между молекулами воды. На рисунке 3.5.2, в отличие от рисунка 3.5.1, на котором молекулы воды представляют из себя шарики, дается представление о структуре молекулы воды.
Рисунок 3.5.2.Водяной пар (1) и вода (2). Молекулы воды увеличены примерно в 5·107 раз.
Сжимаемость жидкостей, то есть изменение объема вещества при изменении давления, по причине плотности расположения молекул в десятки и сотни тысяч раз меньше, чем сжимаемость газов. К примеру, чтобы изменить объем воды всего на 1 % необходимо повысить значение давления примерно в 200 раз. Подобное увеличение давления по сравнению с атмосферным достигается на глубине близкой к 2 км.
Подобно твердым телам, жидкости имеют свойство менять свой объем при изменении температуры. В случае не самых больших интервалов температур относительное изменение объема ΔVV0 пропорционально изменению температуры ΔT, что может быть записано в виде следующего соотношения:
ΔVV0=β∆T.
В котором коэффициент β представляет собой температурный коэффициент объемного расширения. Данный коэффициент у жидкостей в десятки раз превышает значение такого же у твердых тел.
Пример 1
К примеру, у воды в случае, если температура равна 20 °С βв≈2·10–4 К–1, у стали βст≈3,6·10–5 К–1, у кварцевого стекла βкв≈9·10–6 К–1.
Тепловое расширение воды обладает важным для жизни на Земле эффектом. В условиях температуры ниже 4 °С вода начинает расширяется при снижении температуры β<0. Максимальную плотность ρв=103 кг/м3 вода приобретает при температуре 4 °С.
Замерзая, вода расширяется, из-за чего лед продолжает плавать на поверхности замерзающего водоема. Температура замерзающей воды подо льдом эквивалентна величине в 0 °С. У дна водоема, то есть слоях воды, обладающих большей плотностью, температура держится около 4 °С.
Поверхностное натяжение
Наличие свободной поверхности в жидкостях является одной из самых интересных ее особенностей. В отличие от газов, жидкость не заполняет весь объем сосуда, в котором она находится. Между жидкостью и газом, возможно паром, возникает граница раздела, находящаяся в особых условиях по сравнению с остальной массой жидкости. В отличие от молекул в глубине жидкости, молекулы, располагающиеся в пограничном ее слое, окружены другими молекулами этой же жидкости не со всех сторон. В среднем воздействующие на одну из молекул внутри жидкости со стороны соседних молекул силы межмолекулярного взаимодействия взаимно скомпенсированы. Каждая отдельно взятая молекула в пограничном слое притягивается находящимися внутри жидкости молекулами. При этом, силами, которые оказывают воздействие на такую молекулу жидкости со стороны молекул газа можно пренебречь. Вследствие этого возникает некая направленная вглубь жидкости равнодействующая сила. Поверхностные молекулы втягиваются внутрь жидкости, с помощью действия сил межмолекулярного притяжения. Однако все молекулы, в том числе и принадлежащие пограничному слою, должны находиться в состоянии равновесия. Оно достигается за счет сокращения расстояния между молекулами в пограничном слое и ближайшими их соседями в жидкости. Как проиллюстрировано на рисунке 3.1.2, в процессе уменьшения расстояния расстояния между молекулами появляются силы отталкивания. В случае, когда средняя величина расстояния между молекулами в жидкости равна r0, молекулы поверхностного слоя расположены плотнее, и по этой причине по сравнению с внутренними молекулами они имеют дополнительным запас потенциальной энергии, что можно увидеть на рисунке 3.1.2.
Замечание 1
Стоит обратить внимание на то, что более плотного поверхностного слоя не приводит к сколь-нибудь заметному изменению объема жидкости по причине чрезвычайно низкой сжимаемости.
Силы межмолекулярного взаимодействия совершают положительную работу, в случае, когда молекула перемещается с поверхности внутрь жидкости. И наоборот, чтобы достать некоторое количество молекул на поверхность из глубины жидкости, то есть повысить площадь поверхности жидкости, внешним силам необходимо произвести пропорциональную изменению ΔS площади поверхности положительную работу ΔAвнеш:
ΔAвнеш=σ∆S,
где коэффициент σ носит название коэффициента поверхностного натяжения (σ>0).
Определение 2
Из всего вышесказанного следует, что коэффициент поверхностного натяжения — это величина равная работе, необходимой для увеличения площади поверхности жидкости при постоянной температуре на единицу.
В СИ коэффициент поверхностного натяжения измеряется в джоулях на метр квадратный (Дж/м2) или же в ньютонах на метр (1 Н/м=1 Дж/м2).
Таким образом, по сравнению с молекулами внутри жидкости молекулы поверхностного слоя жидкости обладают избыточной потенциальной энергией. Потенциальная энергия Eр поверхности жидкости пропорциональна ее площади и выражается в виде следующей формулы:
Eр=Aвнеш=σS.
Из раздела механики известно, что равновесным состояниям системы соответствует минимальное значение ее потенциальной энергии. Следовательно, свободная поверхность жидкости стремится уменьшить свою площадь. По данной причине свободная капля жидкости принимает шарообразную форму.
Определение 3
Жидкость ведет себя таким образом, будто по касательной к ее поверхности действуют сокращающие данную поверхность силы. Такие силы называются силами поверхностного натяжения.
Силы поверхностного натяжения влияют на поверхность жидкости таким образом, что она становится похожей на упругую растянутую пленку, с той лишь разницей, что упругие силы в пленке зависят от площади ее поверхности, то есть от степени деформированности пленки, а силы поверхностного натяжения, зависимости от площади поверхности жидкости не имеют.
Пример 2
Некоторые жидкости, например, мыльная вода, имеют способность формировать тонкие пленки. Хорошо известные каждому человеку мыльные пузыри обладают правильной сферической формой, в чем также проявляется воздействие сил поверхностного натяжения. В случае, когда в мыльный раствор опускают проволочную рамку с одной подвижной стороной, вся она затягивается пленкой жидкости, как это показано на рисунке 3.5.3.
Рисунок 3.5.3. Подвижная сторона проволочной рамки в равновесии под действием внешней силы Fвн→ и результирующей сил поверхностного натяжения Fн→.
Силы поверхностного натяжения действуют на уменьшение поверхности пленки. Ради равновесия подвижной стороны рамки к ней необходимо приложить внешнюю силу
Fвн→=-Fн→. Если воздействие силы Fвн→ спровоцирует перемещение перекладины на некоторое Δx, то будет произведена работа ΔAвн=FвнΔx=ΔEp=σΔS, где ΔS=2LΔx является увеличением площади поверхности обеих сторон мыльной пленки. По той причине, что модули сил Fвн→ и Fн→ эквивалентны, справедливой будет запись:
Fн∆x=σ2L∆x или σ=Fн2L.
Определение 4
Исходя из этого, можно заявить, что коэффициент поверхностного натяжения σ может быть определен как модуль силы поверхностного натяжения, действующей на единицу длины линии, ограничивающей поверхность.
По причине воздействия сил поверхностного натяжения на капли жидкости и их действия внутри мыльных пузырей появляется некоторое избыточное давление Δp. При мысленном разрезании сферической капли с радиусом R на две равные части каждая из половин должна находиться в равновесии под действием приложенных к границе разреза длиной 2πR и сил избыточного давления, действующих на площадь πR2 сечения (рис. 3.5.4) сил поверхностного натяжения. Условие равновесия может быть записано в следующем виде:
σ2πR=∆pπR2.
Исходя из этого, можно заявить, что избыточное давление внутри капли эквивалентно:
∆p=2σR(капля жидкости).
Рисунок 3.5.4.Сечение сферической капли жидкости.
Из-за того, что пленка обладает двумя поверхностями, величина избыточного давления внутри мыльного пузыря в два раза выше, чем в капле:
∆p=4σR(мыльный пузырь).
Пренебрегая взаимодействием с молекулами газа, можно сказать, что поблизости с границей между твердым телом, жидкостью и газом форма свободной поверхности жидкости зависима от сил взаимодействия молекул жидкости с молекулами твердого тела.
Определение 5
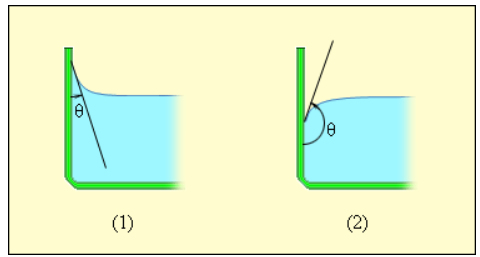
В случае, когда данные силы превышают силы взаимодействия между молекулами жидкости, жидкость смачивает поверхность твердого тела. В таком случае жидкость подходит к поверхности твердого тела под некоторым характерным для данной пары жидкость – твердое тело острым углом θ. Такой угол носит название краевого угла.
Краевой угол θ является тупым (рисунок 3.5.5), в случае, если силы взаимодействия между молекулами жидкости превосходят силы их взаимодействия с молекулами твердого тела. В подобном случае можно сказать, что поверхность твердого тела не смачивается жидкостью. В условиях полного смачивания θ=0, полного несмачивания θ=180°.

Рисунок 3.5.5. Краевые углы смачивающей (1) и несмачивающей (2) жидкостей.
Капиллярные явления
Определение 6
Капиллярными явлениями называют процесс подъема или опускания жидкости в трубках малого диаметра, другими словами, в капиллярах.
Смачивающие жидкости поднимаются по капиллярам, несмачивающие – опускаются. На рисунке 3.5.6 проиллюстрирована опущенная нижним концом в смачивающую жидкость плотности ρ капиллярная трубка, обладающая некоторым радиусом r. При этом верхний конец капилляра является открытым. Подъем жидкости в капилляре будет происходить до тех пор, пока сила тяжести Fт→, оказывающая воздействие на столб жидкости в капилляре, не станет эквивалентна по модулю результирующей Fндействующих вдоль границы соприкосновения жидкости с поверхностью капилляра сил поверхностного натяжения: Fт=Fн, где Fт=mg=ρhπr2g, Fн=σ2πr cos θ.
Из этого следует:
h=2σ cos θρgr.
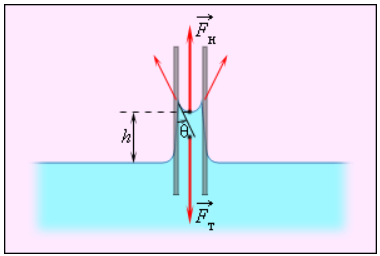
Рисунок 3.5.6. Подъем смачивающей жидкости в капилляре.
При полном смачивании θ=0, cos θ=1. В таком случае:
h=2σρgr.
При полном несмачивании θ=180°, cos θ=–1 и, соответственно, h<0. Уровень несмачивающей жидкости в капилляре опускается ниже уровня жидкости в сосуде, в которую опущен капилляр.
Вода почти полностью смачивает чистую поверхность стекла. Ртуть же, строго наоборот, полностью не смачивает стеклянную поверхность. По этой причине уровень ртути в стеклянном капилляре опускается ниже, чем уровень в сосуде.
