Какие свойства проявляют атомы азота

Азот — неметаллический элемент Va группы периодической таблицы Д.И. Менделеева. Составляет 78% воздуха. Входит в состав
белков, являющихся важной частью живых организмов.
Температура кипения азота составляет -195,8 °C. Однако быстрого замораживания объектов, которое часто демонстрируют в
кинофильмах, не происходит. Даже для заморозки растения нужно продолжительное время, это связано с низкой теплоемкостью
азота.
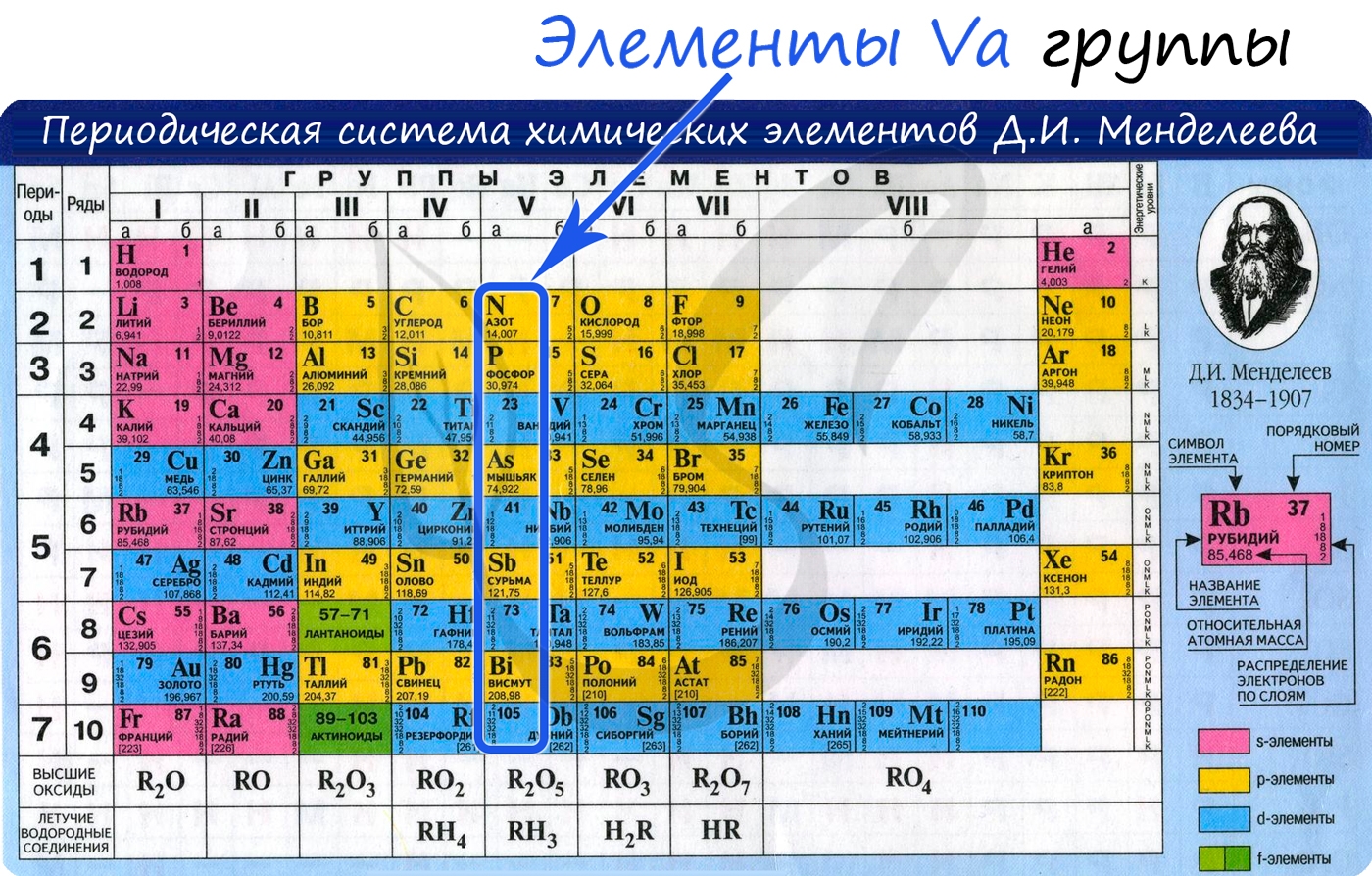
Общая характеристика элементов Va группы
От N к Bi (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств.
Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Азот, фосфор и мышьяк являются неметаллами, сурьма — полуметалл, висмут — металл.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns2np3:
- N — 2s22p3
- P — 3s23p3
- As — 4s24p3
- Sb — 5s25p3
- Bi — 6s26p3
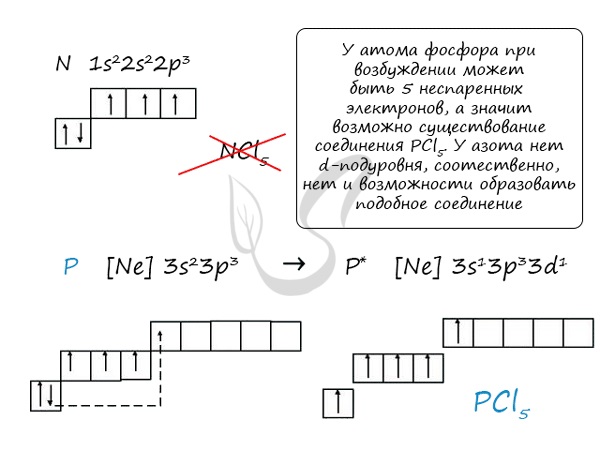
Основное и возбужденное состояние азота
При возбуждении атома азота электроны на s-подуровне распариваются и переходят на p-подуровень. Поскольку азот находится во втором периоде, то
3ий уровень у него отсутствует, что проявляется в особенностях электронной конфигурации возбужденного состояния.
Сравнивая возможности перемещения электронов у азота и фосфора, разница становится очевидна.
Природные соединения
В природе азот встречается в виде следующих соединений:
- Воздух — во вдыхаемом нами воздухе содержится 78% азота
- Азот входит в состав нуклеиновых кислот, белков
- KNO3 — индийская селитра, калиевая селитра
- NaNO3 — чилийская селитра, натриевая селитра
- NH4NO3 — аммиачная селитра (искусственный продукт, в природе не встречается)
Селитры являются распространенными азотными удобрениями, которые обеспечивают быстрый рост и развитие растений, повышают урожайность. Однако,
следует строго соблюдать правила их применения, чтобы не превысить допустимые концентрации.

Получение
В промышленности азот получают путем сжижения воздуха. В дальнейшем путем испарения их сжиженного воздуха получают азот.
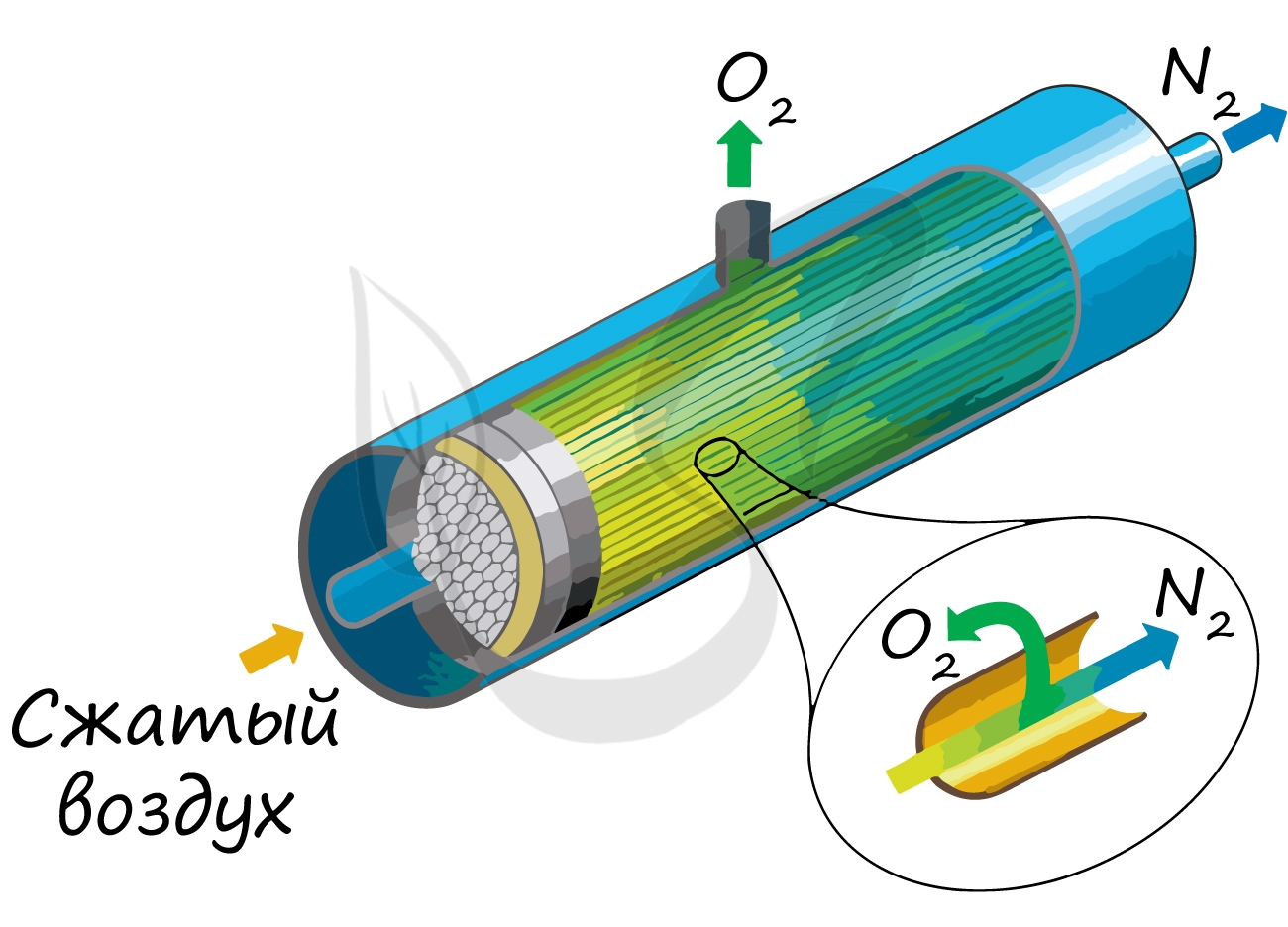
Применяют и метод мембранного разделения, при котором через специальный фильтр из сжатого воздуха удаляют кислород.
В лаборатории методы не столь экзотичны. Чаще всего получают азот разложением нитрита аммония
NH4NO2 → (t) N2 + H2O
Также азот можно получить путем восстановления азотной кислоты активными металлами.
HNO3(разб.) + Zn → Zn(NO3)2 + N2 + H2O

Химические свойства
Азот восхищает — он принимает все возможные для себя степени окисления от -3 до +5.

Молекула азота отличается большой прочностью из-за наличия тройной связи. Вследствие этого многие реакции эндотермичны: даже горение
азота в кислороде сопровождается поглощением тепла, а не выделением, как обычно бывает при горении.

- Реакция с металлами
- Реакция с неметаллами
Без нагревания азот взаимодействует только с литием. При нагревании реагирует и с другими металлами.
N2 + Li → Li3N (нитрид лития)
N2 + Mg → (t) Mg3N2
N2 + Al → (t) AlN
Важное практическое значение имеет синтез аммиака, который применяется в дальнейшим при изготовлении удобрений, красителей, лекарств.
N2 + H2 ⇄ (t, p) NH3
Аммиак
Бесцветный газ с резким едким запахом, раздражающим слизистые оболочки. Раствор концентрацией 10% аммиака применяется в медицинских целях,
называется нашатырным спиртом.
Получение
В промышленности аммиак получают прямым взаимодействием азота и водорода.
N2 + H2 ⇄ (t, p) NH3
В лабораторных условиях сильными щелочами действуют на соли аммония.
NH4Cl + NaOH → NH3 + NaCl + H2O
Химические свойства
Аммиак проявляет основные свойства, окрашивает лакмусовую бумажку в синий цвет.
- Реакция с водой
- Основные свойства
- Восстановительные свойства
Образует нестойкое соединение — гидроксид аммония, слабое основание. Оно сразу же распадается на воду и аммиак.
NH3 + H2O ⇄ NH4OH
Как основание аммиак способен реагировать с кислотами с образованием солей.
NH3 + HCl → NH4Cl (хлорид аммония)
NH3 + HNO3 → NH4NO3 (нитрат аммония)

Поскольку азот в аммиаке находится в минимальной степени окисления -3 и способен только ее повышать, то аммиак проявляет выраженные
восстановительные свойства. Его используют для восстановления металлов из их оксидов.
NH3 + FeO → N2↑ + Fe + H2O
NH3 + CuO → N2↑ + Cu + H2O
Горение аммиака без катализатора приводит к образованию азота в молекулярном виде. Окисление в присутствии катализатора сопровождается
выделением NO.
NH3 + O2 → (t) N2 + H2O
NH3 + O2 → (t, кат) NO + H2O

Соли аммония
Получение
NH3 + H2SO4 → NH4HSO4 (гидросульфат аммония, избыток кислоты)
3NH3 + H3PO4 → (NH4)3PO4
Химические свойства
Помните, что по правилам общей химии, если по итогам реакции выпадает осадок, выделяется газ или образуется вода — реакция идет.
- Реакции с кислотами
- Реакции с щелочами
- Реакции с солями
- Реакция гидролиза
- Реакции разложения
NH4Cl + H2SO4 → (NH4)2SO4 + HCl↑
В реакциях с щелочами образуется гидроксид аммония — NH4OH. Нестойкое основание, которое легко распадается на воду и аммиак.
NH4Cl + KOH → KCl + NH3 + H2O
(NH4)2SO4 + BaCl2 = BaSO4↓ + NH4Cl
В воде ион аммония подвергается гидролизу с образованием нестойкого гидроксида аммония.
NH4+ + H2O ⇄ NH4OH + H+
NH4OH ⇄ NH3 + H2O
NH4Cl → (t) NH3↑ + HCl↑
(NH4)2CO3 → (t) NH3↑ + H2O + CO2↑
NH4NO2 → (t) N2↑ + H2O
NH4NO3 → (t) N2O↑ + H2O
(NH4)3PO4 → (t) NH3↑ + H3PO4

Оксид азота I — N2O
Закись азота, веселящий газ — N2O — обладает опьяняющим эффектом. Несолеобразующий оксид. При н.у. является бесцветным газом с приятным
сладковатым запахом и привкусом. В медицине применяется в больших концентрациях для ингаляционного наркоза.

Получают N2O разложением нитрата аммония при нагревании:
NH4NO3 → N2O + H2O
Оксид азота I разлагается на азот и кислород:
N2O → (t) N2 + O2
Оксид азота II — NO
Окись азота — NO. Несолеобразующий оксид. При н.у. бесцветный газ, на воздухе быстро окисляется до оксида азота IV.
Получение
В промышленных масштабах оксид азота II получают при каталитическом окислении аммиака.
NH3 + O2 → (t, кат) NO + H2O
В лабораторных условиях — в ходе реакции малоактивных металлов с разбавленной азотной кислотой.
Cu + HNO3(разб.) → Cu(NO3)2 + NO + H2O
Химические свойства
На воздухе быстро окисляется с образованием бурого газа — оксида азота IV — NO2.
NO + O2 → NO2

Оксид азота III — N2O3
При н.у. жидкость синего цвета, в газообразной форме бесцветен. Высокотоксичный, приводит к тяжелым ожогам кожи.

Получение
Получают N2O3 в две стадии: сначала реакцией оксида мышьяка III с азотной кислотой, затем
охлаждением полученной смеси газов до температуры — 36 °C.
As2O3 + HNO3 → H3AsO 3 + NO↑ + NO2↑
При охлаждении газов образуется оксид азота III.
NO + NO2 → N2O3
Химические свойства
Является кислотным оксидом. соответствует азотистой кислота — HNO2, соли которой называются нитриты (NO2-).
Реагирует с водой, основаниями.
H2O + N2O3 → HNO2
NaOH + N2O3 → NaNO2 + H2O
Оксид азота IV — NO2
Бурый газ, имеет острый запах. Ядовит.

Получение
В лабораторных условиях данный оксид получают в ходе реакции меди с концентрированной азотной кислотой. Также NO2 выделяется при
разложении нитратов.
Cu + HNO3(конц) → Cu(NO3)2 + NO2 + H2O

Cu(NO3)2 → (t) CuO + NO2 + O2
Pb(NO3)2 → (t) PbO + NO2 + O2
Химические свойства
Проявляет высокую химическую активность, кислотный оксид.
- Окислительные свойства
- Реакции с водой и щелочами
Как окислитель NO2 ведет себя в реакциях с фосфором, углеродом и серой, которые сгорают в нем.
NO2 + C → CO2 + N2
NO2 + P → P2O5 + N2
Окисляет SO2 в SO3 — на этой реакции основана одна из стадий получения серной кислоты.
SO2 + NO2 → SO3 + NO
Оксид азота IV соответствует сразу двум кислотам — азотистой HNO2 и азотной HNO3. Реакции с
водой и щелочами протекают по одной схеме.
NO2 + H2O → HNO3 + HNO2
NO2 + LiOH → LiNO3 + LiNO2 + H2O
Если растворение в воде оксида проводить в избытке кислорода, образуется азотная кислота.
NO2 + H2O + O2 → HNO3

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.

Азот — первый представитель главной подгруппы пятой группы, представитель пниктогенов. Именно поэтому эти элементы называют подгруппой азота. Однако азот имеет ряд особенностей:
Число ковалентных связей, образуемых атомом азота по обменному механизму, не может быть больше 3-х, так как у атома азота на внешнем электронном слое отсутствует d-орбиталь.
Электронная конфигурация атома азота: $1s^22s^22p^3$Атом азота может образовывать ковалентную связь по донорно-акцепторному механизму за счет наличия неподеленной электронной пары на 2s-подуровне. Подробнее эта тема раскрыта в разделе «Валентные возможности азота»

Высшая валентность N равна IV.
3. В соединениях с кислородом азот проявляет степени окисления: +1; +2; +3; +4; +5.
Степени окисления азота в его соединениях
| $N^{-3}$ | $N^0$ | $N^{+1}$ | $N^{+2}$ | $N^{+3}$ | $N^{+4}$ | $N^{+5}$ |
|---|---|---|---|---|---|---|
$NH_3$ аммиак летучее водородное соединение | $N_2$ свободный азот | $N_2O$ $NO$ низшие оксиды, несолеобразующие | $N_2O_3$ $to$ $NO$ + $NO_2$ неустойчивый кислотный оксид | $NO_2$ $leftrightarrow$ $N_2O_4$ кислотный оксид | $2N_2O_5$ → $4NO_2$ + $O_2$ неустойчивый кислотный оксид | |
| В воздухе | $HNO_2$ азотистая кислота | $HNO_3$ азотная кислота | ||||
$NH_4K$ соли аммония $Me_xN_y$ нитриды | $Me(NO_2)_х$ нитриты | $Me(NO_3)_х$ нитраты | ||||
История открытия азота
Соединения азота — селитра, азотная кислота, аммиак — были известны задолго до получения азота в свободном состоянии.

В 1772 г. Д.Резерфорд, сжигая фосфор и другие в-ва в стеклянном колоколе, показал, что остающийся газ не поддерживает дыхания и горения. Д.Резерфорд назвал его «удушливым воздухом».
 К.Шееле назвал этот элемент, извлеченный из воздуха, «дурным воздухом».
К.Шееле назвал этот элемент, извлеченный из воздуха, «дурным воздухом».
В 1787 г. А.Лавуазье установил, что «жизненный» и «удушливый» газы, входящие в состав воздуха, это простые вещества, и предложил название «азот». «А» — отсутствие, «зоо» — жизнь. «Безжизненный» — азот.
И не случайно: испытания проводили на лабораторных мышах, помещая их под колпак с азотом, где они погибали.


ФИЗИЧЕСКИЕ СВОЙСТВА АЗОТА
Входит в состав воздуха: $varphi$ $(N_2)$ = 78%. Также входит в состав других неорганических соединений и состав живой материи.
Азот
немного легче воздуха; плотность 1,2506 $textrm{$кг/м^3$}$ (при н.у.),
$t_{textrm{пл.}}$ = — 209,8 $^circ C$, $t_{textrm{кип.}}$ = -195,8 $^circ C$
азот сжижается с трудом: плотность жидкого азота 800 $textrm{$кг/м^3$}$.
Жидкий азот используют для охлаждения различного оборудования и техники; для охлаждения компонентов компьютера при экстремальном разгоне. В химии жидкий азот применяют при работе с вакуумными линиями, для охлаждения веществ и проведения реакций при низких температурах, для создания инертной атмосферы. При этом транспортировка азота осуществляется в сосудах Дьюара:


В воде азот менее растворим чем кислород: при 0 $^circ C$ в 1$textrm{$м^3$}$ $H_2O$ растворяется 23,3 г азота.
Азот не поддерживает дыхание и горение; он чрезвычайно инертен. Малая реакционная способность азота обусловлена строением его молекулы.

N≡N — это самая прочная (из всех двухатомных) молекула. Молекула азота очень устойчива: энергия диссоциации ее на атомы составляет 942,9 кДж/моль, поэтому даже при температуре 3300 $^circС$ степень диссоциации азота составляет 0,1%.
Азот – один из распространенных элементов на Земле.

— в атмосфере — 4$cdot10^{15}$ тонн по массе и 78% газообразного азота по объёму;
— литосфере – 1,9$cdot10^{-3}$% по массе;
— в живых организмах — 0,3% по массе.
В белке животных и человека — 16–17% азота. В организмах человека и плотоядных животных белок образуется за счёт потребляемых белковых веществ травоядных животных и в растениях. “Жизнь — есть способ существования белковых тел на Земле” — по определению Ф.Энгельса.
СПОСОБЫ ПОЛУЧЕНИЯ АЗОТА
Промышленные способы:
Ректификация (разделение) жидкого воздуха:
сначала улетучивается $N_2$ (t$_{textrm{кип.}}$= -196$ ^circ C$);
затем $О_2$ (t$_{textrm{кип.}}$ = -183,0 $^circ C$)
Лабораторные способы:
Окислительно-восстановительное разложение некоторых солей аммония:
$NH_4NO_2$ = $N_2$ + $2H_2O$
$(NH_4)_2Cr_2O_7$ = $Cr_2O_3$ + $N_2$ + $4H_2O$
Окисление аммиака и солей аммония:
$4NH_3$ + $3O_2$ = $2N_2$ + $6H_2O$
$8NH_3$+ $3Br_2$ = $N_2$ + $6NH_4Br$
$NaNO_2 + NH_4Cl xrightarrow[]{t, ^circ C} NaCl + N_2 + 2H_2O$
ХИМИЧЕСКИЕ СВОЙСТВА АЗОТА
Молекулярный азот — химически инертное вещество (см.выше строение азота), поэтому легко реагирует только с металлами:
$N_2 + 6Lixrightarrow[]{t_textrm{комн.}}2Li_3N$
Магний горит с образованием не только оксида, но и нитрида магния:
$3N_2 + 6Mg xrightarrow{}2Mg_3N_2$
$N_2 + 2Al xrightarrow{t} 2AlN$
Азот при взаимодействии с металлами проявляет окислительные свойства: образуются нитриды металлов, в которых степень окисления азота равна -3.
С неметаллами азот реагирует тяжелее: для инициирования и ускорения реакций необходимо применять высокие температуры, искровые электрические разряды, ионизирующее излучение, катализаторы (Fe, Cr, V, Ti и их соединения):
$N_2 + 3H_2 xrightarrow{textrm{ t; кат; Р}}2NH_3$
$3F_2 + N_2 xrightarrow{textrm{эл. разряд}} 2NF_3$
$Cl_2 + N_2 ne$
$S$ + $N_2$ $ne$
Реакция горения азота идет при высокой температуре, в электрическом разряде или в присутствии катализатора:
$N_2 + O_2 = 2NO -Q$
Обратите внимание: реакция эндотермическая!
Азот не реагирует со сложными веществами.
Общая характеристика химических
элементов подгруппы азота

Подгруппа азота (пниктогены) – V группа, главная подгруппа «А» — азот, фосфор, мышьяк, сурьма, висмут.
НАХОЖДЕНИЕ В ПРИРОДЕ |
Содержание в земной коре: азот — 0,01%, фосфор — |
Свойства элементов V-A подгруппы
Элемент | Азот | Фосфор | Мышьяк | Сурьма | Висмут |
Свойство | |||||
Порядковый номер элемента | 7 | 15 | 33 | 51 | 83 |
Относительная атомная масса | 14,007 | 30,974 | 74,922 | 121,75 | 208,980 |
Температура плавления,С0 | -210 | 44,1 | 817 | 631 | 271 |
Температура кипения,С0 | -196 | 280 | 613 | 1380 | 1560 |
Плотность г/см3 | 0,96 | 1,82 | 5,72 | 6,68 | 9,80 |
Степени окисления | +5, +3,-3 | +5, +3,-3 | +5, +3,-3 | +5, +3,-3 | +5, +3,-3 |
1. Строение атомов химических
элементов
Название химического элемента | Схема | Электронное | Формула | Формула RH3 |
1. Азот | N+7)2)5 | …2s22p3 | N2O5 | NH3 |
2. Фосфор | P+15)2)8)5 | …3s23p3 | P2O5 | PH3 |
3. Мышьяк | As+33)2)8)18)5 | …4s24p3 | As2O5 | AsH3 |
4. Сурьма | Sb+51)2)8)18)18)5 | …5s25p3 | Sb2O5 | SbH3 |
5. Висмут | Bi+83)2)8)18)32)18)5 | …6s26p3 | Bi2O5 | BiH3 |

Наличие трех
неспаренных электронов на внешнем энергетическом уровне объясняет то, что в
нормальном, невозбужденном состоянии валентность элементов подгруппы азота
равна трем.
У атомов
элементов подгруппы азота (кроме азота — внешний уровень азота состоит только
из двух подуровней — 2s и 2p) на внешних энергетических уровнях имеются
вакантные ячейки d-подуровня, поэтому они могут распарить один электрон с
s-подуровня и перенести его на d-подуровень. Таким образом, валентность
фосфора, мышьяка, сурьмы и висмута равна 5.
Элементы группы
азота образуют с водородом соединения состава RH3, а с кислородом
оксиды вида — R2O3 и R2O5. Оксидам
соответствуют кислоты HRO2 и HRO3 (и ортокислоты H3PO4,
кроме азота).
Высшая степень окисления этих элементов равна +5, а низшая -3.
Так как заряд ядра атомов увеличивается, число
электронов на внешнем уровне постоянно, число энергетических уровней в атомах
растёт и радиус атома увеличивается от азота к висмуту, притяжение
отрицательных электронов к положительному ядру ослабевает и способность к отдаче электронов
увеличивается, и, следовательно, в подгруппе азота с ростом порядкового номера
неметаллические свойства убывают, а металлические усиливаются.
Азот
— неметалл, висмут — металл. От азота к висмуту прочность соединений RH3
уменьшается, а прочность кислородных соединений возрастает.
Наибольшее значение среди
элементов подгруппы азота имеют азот и
фосфор .
Азот, физические и химические свойства, получение и применение
1. Азот – химический
элемент

N +7)2)5
1s22s22p3 незавершённый внешний уровень, p-элемент, неметалл
Ar(N)=14
2. Возможные степени
окисления
Из-за наличия трёх
неспаренных электронов азот очень активен, находится только в виде соединений.
Азот проявляет в соединениях степени окисления от «-3» до «+5»
3. Азот – простое
вещество, строение молекулы, физические свойства
Азо́т (от греч. ἀζωτος — безжизненный, лат. Nitrogenium), вместо предыдущих названий
(«флогистированный», «мефитический» и «испорченный» воздух) предложил в 1787 году Антуан
Лавуазье. Как показано выше, в то время уже было известно, что азот не поддерживает
ни горения, ни дыхания. Это свойство и сочли наиболее важным. Хотя впоследствии
выяснилось, что азот, наоборот, крайне необходим для всех живых существ,
название сохранилось во французском и русском языках.
N2 – ковалентная неполярная связь, тройная
(σ, 2π), молекулярная кристаллическая решётка

Тройная связь | Энергия связи 945 кДж/моль |
Вывод:
1. Малая реакционная
способность при обычной температуре
2. Газ, без цвета,
запаха, легче воздуха
Mr(Bоздуха)/Mr(N2) = 29/28
4. Химические свойства
азота
N – окислитель ( 0 → -3) | N – восстановитель (0 → +5) |
1. С металлами образуются нитриды MxNy — при нагревании с Mg и щелочно-земельными и щелочными: 3Сa + N2 = Ca3N2 (при t) — c Li при к t комнатной Нитриды разлагаются Са3N2 2. С водородом 3H2+N2 ↔ 2NH3 (условия — T, p, kat) | N2 + O2 ↔ 2 NO – Q (при t= 2000 C) Азот не реагирует с |
5. Получение:
В промышленности азот получают из воздуха. Для этого
воздух сначала охлаждают, сжижают, а жидкий воздух подвергают перегонке
(дистилляции). Температура кипения азота немного ниже (–195,8°C), чем другого
компонента воздуха — кислорода (–182,9°C), поэтому при осторожном нагревании
жидкого воздуха азот испаряется первым. Потребителям газообразный азот
поставляют в сжатом виде (150 атм. или 15 МПа) в черных баллонах, имеющих
желтую надпись «азот». Хранят жидкий азот в сосудах Дьюара.
В лаборатории чистый («химический») азот получают
добавляя при нагревании насыщенный раствор хлорида аммония NH4Cl к
твердому нитриту натрия NaNO2:
NaNO2 + NH4Cl = NaCl + N2
+ 2H2O.
Можно также нагревать
твердый нитрит аммония:
NH4NO2 = N2 + 2H2O. ОПЫТ
6. Применение:
В промышленности газ
азот используют главным образом для получения аммиака. Как химически инертный
газ азот применяют для обеспечения инертной среды в различных химических и
металлургических процессах, при перекачке горючих жидкостей. Жидкий азот широко
используют как хладагент, его применяют в медицине, особенно в косметологии.
Важное значение в поддержании плодородия почв имеют азотные минеральные
удобрения.
7. Биологическая роль
Азот является элементом, необходимым для существования животных и растений,
он входит в состав белков (16—18 % по массе), аминокислот, нуклеиновых кислот,
нуклеопротеидов, хлорофилла, гемоглобина
и др. В составе живых клеток по числу атомов азота
около 2%, по массовой доле — около 2,5 % (четвертое место после водорода,
углерода и кислорода). В связи с этим значительное количество связанного азота
содержится в живых организмах, «мёртвой органике» и дисперсном веществе морей и
океанов. Это количество оценивается примерно в 1,9·1011 т. В
результате процессов гниения и разложения азотсодержащей органики, при условии
благоприятных факторов окружающей среды, могут образоваться природные залежи
полезных ископаемых, содержащие азот, например, «чилийская селитра» (нитрат натрия с
примесями других соединений), норвежская, индийская селитры.
Тренажёр №1 «Простое вещество азот»
Тренажёр №2 «Характеристика азота по положению
в Периодической системе элементов Д. И. Менделеева»
Задания для закрепления
№1. Осуществите
превращения по схеме:
N2→Li3N→NH3
№2. Составьте уравнения реакции
взаимодействия азота с кислородом, магнием и водородом. Для каждой реакции
составьте электронный баланс, укажите окислитель и восстановитель.
№3. В одном цилиндре находится газ азот, в другом —
кислород, а в третьем — углекислый газ. Как различить эти газы?
№4. В некоторых горючих газах содержится в виде примеси свободный азот. Может
ли при сгорании таких газов в обыкновенных газовых плитах образоваться оксид
азота (II). Почему?
