Какие свойства проявляет hcl в водном растворе

Характеристики и физические свойства соляной кислоты
Сильная кислота: pKa = -7,1. Концентрированная соляная кислота содержит около 37% HCl.
Основные физические свойства соляной кислоты приведены в таблице:
Температура плавления, oС | -30 |
Температура кипения, oС | 48 |
Энтальпия образования, кДж/моль | -605,22 |
Плотность, г/см3 | 1,19 |
Удельная теплоемкость, кДж/(кг×К) | 2,46 |
Вязкость, МПа×с | 1,99 |
Получение соляной кислоты
Соляная кислота получается растворением в воде хлороводорода. В настоящее время основным способом промышленного получения хлороводорода является синтез его из водорода и хлора:
H2 + Cl2 = 2HCl + 183 кДж.
Этот процесс осуществляют в специальных установках, в которых смесь водорода и хлора непрерывно образуется и тут же сгорает ровным пламенем. Тем самым достигается спокойное (без взрыва) протекание реакции. Исходным сырьем для получения хлороводорода служат хлор и водород, образующиеся при электролизе раствора хлорида натрия.
Большие количества соляной кислоты получают также в качестве побочного продукта хлорирования органических соединений согласно уравнению реакции, представленному ниже:
R-H + Cl2 = R-Cl + HCl,
где R – углеводородный радикал.
Химические свойства соляной кислоты
Соляная кислота – сильный электролит. Для нее характерны следующие химические свойства, общие для всех кислот:
— способность взаимодействовать с основаниями с образованием солей:
HCldilute + NaOHdilute = NaCl + H2O;
HCldilute + NH3×H2O = NH4Cl + H2O;
— способность взаимодействовать с некоторыми металлами с выделением водорода (разбавленный раствор):
2HCldilute + Fe = FeCl2 + H2↑;
2HCldilute + Zn = ZnCl2 + H2↑;
— способность вступать в реакции взаимодействия с основными и амфотерными оксидами с образованием солей и воды:
4HClconc + MnO2 = MnCl2 + 2H2O + Cl2↑;
4HClconc + PbO2 = PbCl2↓ + Cl2↑ + 2H2O;
— способность взаимодействовать с солями более слабых кислот:
2HCldilute + CaCO3 = CaCl2 + CO2↑ + H2O;
— способность изменять цвета индикаторов, в частности, вызывать красную окраску лакмуса;
— кислый вкус.
При диссоциации соляной кислоты образуются ионы водорода:
HCl↔H+ + Cl—.
Нагревание смеси растворов соляной и азотной кислот до температуры 100-150oС приводит к образованию очень сильного окислителя — соединения, которое называют «царская водка»:
6HClconc + 2HNO3 conc = 2NO↑ + 3Cl2↑ + 4H2O.
Соляная кислота в окислительно-восстановительных реакциях может выступать и как восстановитель (за счет хлорид-аниона Cl—) и как окислитель (за счет катиона водорода H+). Уравнения ОВР с участием соляной кислоты приведены ниже:
16HClconc + 2KMnO4 = 2MnCl2 + 5Cl2↑ + 8H2O + 2KCl;
14 HClconc + K2Cr2O7 = 2CrCl3 + 3Cl2↑ + 7H2O + 2KCl (t = 60 – 80oC);
4 HClconc + Ca(ClO)2 = 2Cl2↑ + CaCl2 + 2H2O;
6 HClconc + KClO3 = 3Cl2↑ + KCl + 3H2O.
Применение соляной кислоты
Соляная кислота – одна из важнейших кислот в химической практике. Ежегодное мировое производство соляной кислоты исчисляется миллионами тонн. Широкое применение находят также многие её соли.
Соляная кислота применяется в таких областях народного хозяйства как гидрометаллургия и гальванопластика, для травления, декапирования и лужения поверхности металлов; пищевом производстве, как регулятор кислотности (добавка Е507); в медицине, в качестве лекарства (смесь с ферментом пепсином) при недостаточной кислотности желудка.
Примеры решения задач
Соляная кислота (также хлороводородная, хлористоводородная кислота, хлористый водород) — раствор хлороводорода (HCl) в воде, сильная одноосновная кислота. Бесцветная, прозрачная, едкая жидкость, «дымящаяся» на воздухе (техническая соляная кислота — желтоватого цвета из-за примесей железа, хлора и пр.). В концентрации около ω = 0,5 % присутствует в желудке человека, что соответствует pH = pω − lg ( ρH2O / μHCl ) ≅ 0,86. Максимальная концентрация при 20 °C равна 38 % по массе, плотность такого раствора 1,19 г/см³. Соли соляной кислоты называются хлоридами.
Физические свойства
Физические свойства соляной кислоты сильно зависят от концентрации растворённого хлороводорода:
| Конц. (вес), кг HCl/кг | Конц. (г/л), кг HCl/м³ | Плотность, кг/л | Молярность M | Водородный показатель (pH) | Вязкость, мПа·с | Удельная теплоемкость, кДж/(кг·К) | Давление пара, Па | Температура кипения, °C | Температура плавления, °C |
| 10 % | 104,80 | 1,048 | 2,87 | −0,4578 | 1,16 | 3,47 | 0,527 | 103 | −18 |
| 20 % | 219,60 | 1,098 | 6,02 | −0,7796 | 1,37 | 2,99 | 27,3 | 108 | −59 |
| 30 % | 344,70 | 1,149 | 9,45 | −0,9754 | 1,70 | 2,60 | 1,410 | 90 | −52 |
| 32 % | 370,88 | 1,159 | 10,17 | −1,0073 | 1,80 | 2,55 | 3,130 | 84 | −43 |
| 34 % | 397,46 | 1,169 | 10,90 | −1,0374 | 1,90 | 2,50 | 6,733 | 71 | −36 |
| 36 % | 424,44 | 1,179 | 11,64 | −1,06595 | 1,99 | 2,46 | 14,100 | 61 | −30 |
| 38 % | 451,82 | 1,189 | 12,39 | −1,0931 | 2,10 | 2,43 | 28,000 | 48 | −26 |
При 20 °C, 1 атм (101 кПа)При затвердевании даёт кристаллогидраты составов HCl·H2O, HCl·2H2O, HCl·3H2O, HCl·6H2O.
Химические свойства
- Взаимодействие с металлами, стоящими в ряду электрохимических потенциалов до водорода, с образованием соли и выделением газообразного водорода:
2Na + 2HCl ⟶ 2NaCl + H2 ↑Mg + 2HCl ⟶ MgCl2 + H2 ↑
2Al + 6HCl ⟶ 2AlCl3 + 3H2 ↑
- Взаимодействие с оксидами металлов с образованием растворимой соли и воды:
Na2O + 2HCl ⟶ 2NaCl + H2O MgO + 2HCl ⟶ MgCl2 + H2OAl2O3 + 6HCl ⟶ 2AlCl3 + 3H2O
- Взаимодействие с гидроксидами металлов с образованием растворимой соли и воды (реакция нейтрализации):
NaOH + HCl ⟶ NaCl + H2O Ba(OH)2 + 2HCl ⟶ BaCl2 + 2H2OAl(OH)3 + 3HCl ⟶ AlCl3 + 3H2O
- Взаимодействие с солями металлов, образованных более слабыми кислотами, например угольной:
Na2CO3 + 2HCl ⟶ 2NaCl + H2O + CO2 ↑
- Взаимодействие с сильными окислителями (перманганат калия, диоксид марганца) с выделением газообразного хлора:
2KMnO4 + 16HCl ⟶ 5Cl2 ↑ + 2MnCl2 + 2KCl + 8H2O
- Взаимодействие с аммиаком с образованием густого белого дыма, состоящего из мельчайших кристалликов хлорида аммония:
NH3 + HCl ⟶ NH4Cl
- Качественной реакцией на соляную кислоту и её соли является её взаимодействие с нитратом серебра, при котором образуется белый творожистый осадок хлорида серебра, нерастворимый в азотной кислоте:
HCl + AgNO3 → AgCl ↓ + HNO3

Получение
Соляную кислоту получают растворением газообразного хлороводорода в воде. Хлороводород получают сжиганием водорода в хлоре, полученная таким способом кислота называется синтетической. Также соляную кислоту получают из абгазов — побочных газов, образующихся при различных процессах, например, при хлорировании углеводородов. Хлороводород, содержащийся в этих газах, называется абгазным, а полученная таким образом кислота — абгазной. В последние десятилетия доля абгазной соляной кислоты в объёме производства постепенно увеличивается, вытесняя кислоту, полученную сжиганием водорода в хлоре. Но полученная методом сжигания водорода в хлоре соляная кислота содержит меньше примесей и применяется при необходимости высокой чистоты.
В лабораторных условиях используется разработанный ещё алхимиками способ, заключающийся в действии концентрированной серной кислоты на поваренную соль:
NaCl + H2SO4 →150oC NaHSO4 + HCl
При температуре выше 550 °C и избытке поваренной соли возможно взаимодействие:
2NaCl + H2SO4 →550oC Na2SO4 + 2HCl
Возможно получение путём гидролиза хлоридов магния, алюминия (нагревается гидратированная соль):
MgCl2 ⋅ 6H2O →t,oC MgO + 2HCl + 5H2O
AlCl3 ⋅ 6H2O →t,oC Al(OH)3 + 3HCl + 3H2O
Эти реакции могут идти не до конца с образованием основных хлоридов (оксихлоридов) переменного состава, например:
MgCl2 + H2O → Mg2OCl2 + HCl
Хлороводород хорошо растворим в воде. Так, при 0 °C 1 объём воды может поглотить 507 объёмов HCl, что соответствует концентрации кислоты 45 %. Однако при комнатной температуре растворимость HCl ниже, поэтому на практике обычно используют 36-процентную соляную кислоту.
Применение

Перевозка соляной кислоты железнодорожным транспортом осуществляется в специализированных вагонах-цистернах
Промышленность
- Применяется в гидрометаллургии и гальванопластике (травление, декапирование), для очистки поверхности металлов при пайке и лужении, для получения хлоридов цинка, марганца, железа и др. металлов. В смеси с поверхностно-активными веществами используется для очистки керамических и металлических изделий (тут необходима ингибированная кислота) от загрязнений и дезинфекции.
- В пищевой промышленности зарегистрирована как регулятор кислотности (пищевая добавка E507). Применяется для изготовления зельтерской (содовой) воды.
Медицина
Основная статья: Кислотность желудочного сока
- Естественная составная часть желудочного сока человека. В концентрации 0,3—0,5 %, обычно в смеси с ферментом пепсином, назначается внутрь при недостаточной кислотности.
Особенности обращения
Высококонцентрированная соляная кислота — едкое вещество, при попадании на кожу вызывает сильные химические ожоги. Особенно опасно попадание в глаза. Для нейтрализации ожогов применяют раствор слабого основания, или соли слабой кислоты, обычно питьевой соды.
При открывании сосудов с концентрированной соляной кислотой пары хлороводорода, притягивая влагу воздуха, образуют туман, раздражающий глаза и дыхательные пути человека.
Реагируя с сильными окислителями (хлорной известью, диоксидом марганца, перманганатом калия) образует токсичный газообразный хлор.
В РФ оборот соляной кислоты концентрации 15 % и более — ограничен.

- Химическая энциклопедия
СОЛЯНАЯ КИСЛОТА (хлористоводородная кислота, хлороводородная кислота)
раствор HCl в воде — бесцветная жидкость с резким запахом; сильная одноосновная кислота. Хлористый водород HCl (мол. м. 36,461 ) — бесцветный газ с резким запахом, во влажном воздухе сильно дымит; длина связи H—С1 0,1274 нм, μ 3,716∙10−30 Кл∙м, энергия диссоциации 427,77 кДж/моль; т. кип. −85,1 °C (бесцв. легко подвижная жидкость), т. пл. −114,22 °C; кристаллизуется в кубич. решетке, ниже −174,15 °C существует ромбич. модификация; тройная точка −114,22 °C; плотн. по воздуху 1,2679; Гкрнт 51,4 °C, pкрит 8,258 МПа, dкрит 0,42 г/см3; 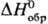 −92,31 кДж/моль, ΔHпл 1,9924 кДж/моль ( −114,22 °C), ΔHисп 16,1421 кДж/моль ( −8,05 °C);
−92,31 кДж/моль, ΔHпл 1,9924 кДж/моль ( −114,22 °C), ΔHисп 16,1421 кДж/моль ( −8,05 °C); 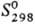 186,79 Дж/(моль∙К); давление пара (Па): 133,32∙10−6 ( −200,7 °C), 2,775∙103 ( −130,15 °C), 10,0∙104 ( −85,1 °C), 74,0∙104 ( −40 °C), 24,95∙105 (0 °C), 76,9∙105 (50 °C); уравнение температурной зависимости давления пара lgp(кПа) = −905,53/Т+ 1,75lgT— −500,77∙10−5T+3,78229 (160–260 К); коэф. сжимаемости 0,00787; γ 23 мН/см ( −155 °C); ρ 0,29∙107 Ом∙м ( −85 °C), 0,59∙107 ( −114,22 °C). См. также табл. 1.
186,79 Дж/(моль∙К); давление пара (Па): 133,32∙10−6 ( −200,7 °C), 2,775∙103 ( −130,15 °C), 10,0∙104 ( −85,1 °C), 74,0∙104 ( −40 °C), 24,95∙105 (0 °C), 76,9∙105 (50 °C); уравнение температурной зависимости давления пара lgp(кПа) = −905,53/Т+ 1,75lgT— −500,77∙10−5T+3,78229 (160–260 К); коэф. сжимаемости 0,00787; γ 23 мН/см ( −155 °C); ρ 0,29∙107 Ом∙м ( −85 °C), 0,59∙107 ( −114,22 °C). См. также табл. 1.

Растворимость HCl в углеводородах при 25 °C и 0,1 МПа (мол. %): в пентане-0,47, гексане-1,12, гептане-1,47, октане-1,63. Растворимость HCl в алкил- и арилгалогенидах невелика, напр. 0,07 моль/моль для C4H9С1. Растворимость в интервале от −20 до 60° С уменьшается в ряду дихлорэтан-три-хлорэтан-тетрахлорэтан-трихлорэтилен. Растворимость при 10 °C в ряде спиртов составляет примерно 1 моль/моль спирта, в эфирах карбоновых кислот 0,6 моль/моль, в карбоновых кислотах 0,2 моль/моль. В простых эфирах образуются устойчивые аддукты R2O ∙ HCl. Растворимость HCl в расплавах хлоридов подчиняется закону Генри и составляет для KCl 2,51∙10−4 (800 °C), 1,75∙10−4 моль/моль (900 °C), для NaCl 1,90∙10−4 моль/моль (900 °C).
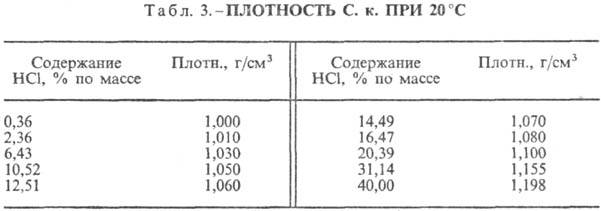
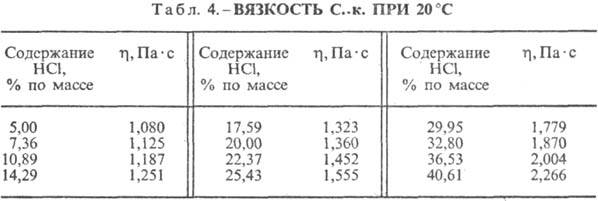
Соляная кислота. Растворение HCl в воде-сильно экзо-термич. процесс, для бесконечно разб. водного раствора ΔH0 растворения HCl −69,9 кДж/моль, 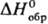 иона Cl−— 167,080 кДж/моль; HCl в воде полностью ионизирован. Растворимость HCl в воде зависит от температуры (табл. 2) и парциального давления HCl в газовой смеси. Плотность С. к. разл. концентрации и η при 20 °C представлены в табл. 3 и 4. С повышением температуры η С. к. понижается, напр.: для 23,05%-ной С. к. при 25 °C η 1364мПа∙с, при 35 °C 1,170 мПа∙с.
иона Cl−— 167,080 кДж/моль; HCl в воде полностью ионизирован. Растворимость HCl в воде зависит от температуры (табл. 2) и парциального давления HCl в газовой смеси. Плотность С. к. разл. концентрации и η при 20 °C представлены в табл. 3 и 4. С повышением температуры η С. к. понижается, напр.: для 23,05%-ной С. к. при 25 °C η 1364мПа∙с, при 35 °C 1,170 мПа∙с.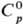 С. к., содержащей η молей воды на 1 моль HCl, составляет [кДж/(кг∙К)]: 3,136 (п = 10), 3,580 (n = 20), 3,902 (n =50), 4,036 (n = 100), 4,061 (п = 200).
С. к., содержащей η молей воды на 1 моль HCl, составляет [кДж/(кг∙К)]: 3,136 (п = 10), 3,580 (n = 20), 3,902 (n =50), 4,036 (n = 100), 4,061 (п = 200).
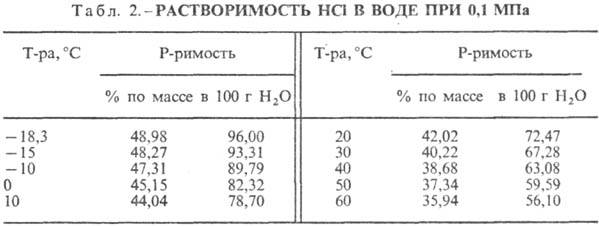
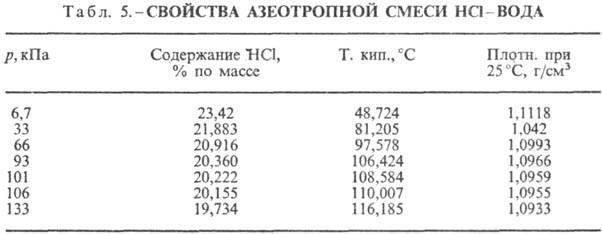
HCl образует с водой азеотропную смесь (табл. 5). В системе HCl-вода существует три эвтектич. точки: — 74,7 °C (23,0% по массе HCl); −73,0 °C (26,5% HCl); −87,5 °C (24,8% HCl, метастабильная фаза). Известны кристаллогидраты HCl∙nH2O, где n = 8, 6 (т. пл. −40 °C), 4, 3 (т. пл. −24,4 °C), 2 (т. пл. −17,7 °C) и 1 (т. пл. −15,35 °C). Лед кристаллизуется из 10%-ной С. к. при —20, из 15%-ной — при -30, из 20%-ной — при −60 и из 24%-ной — при −80 °C. Растворимость галогенидов металлов с увеличением концентрации HCl в С. к. падает, что используют для их высаливания.
Химические свойства. Чистый сухой HCl начинает диссоциировать выше 1500 °C, химически пассивен. Мн. металлы, С, S, P не взаимод. даже с жидким HCl. С нитридами, карбидами, боридами, сульфидами реагирует выше 650 °C, с гидридами Si, Ge и Веществ присут. AlCl3, с оксидами переходных металлов — при 300 °C и выше. Окисляется O2 и HNO3 до Cl2, с SO3 дает C1SO3H. О реакциях с орг. соединениями см. гидрогалогенирование.
С. к. химически весьма активна. Растворяет с выделением H2 все металлы, имеющие отрицат. нормальный потенциал, со мн. оксидами и гидроксидами металлов образует хлориды, выделяет своб. кислоты из таких солей, как фосфаты, силикаты, бораты и др.
Получение. В промышленности HCl получают след. способами-сульфатным, синтетич. и из абгазов (побочных газов) ряда процессов. Первые два метода теряют свое значение. Так, в США в 1965 доля абгазной С. к. составляла 77,6% в общем объеме производства, а в 1982–94%.
Производство С. к. (реактивной, полученной сульфатным способом, синтетич., абгазной) заключается в получении HCl с послед. его абсорбцией водой. В зависимости от способа отвода теплоты абсорбции (достигает 72,8 кДж/моль) процессы разделяются на изотермич., адиабатич. и комбинированные.
Сульфатный метод основан на взаимод. NaCl с конц. H2SO4 при 500–550 °C. Реакц. газы содержат от 50–65% HCl (муфельные печи) до 5% HCl (реактор с кипящим слоем). Предложено заменить H2SO4 смесью SO2 и O2 (температура процесса ок. 540 °C, кат. — Fe2O3).
В основе прямого синтеза HCl лежит цепная реакция горения: H2 + Cl2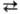 2HCl+184,7кДж Константа равновесия Кр рассчитывается по уравнению: lgKp = 9554/T— 0,5331g T+ 2,42.
2HCl+184,7кДж Константа равновесия Кр рассчитывается по уравнению: lgKp = 9554/T— 0,5331g T+ 2,42.
Реакция инициируется светом, влагой, твердыми пористыми (древесный уголь, пористая Pt) и некоторыми минер. веществами (кварц, глина). Синтез, ведут с избытком H2 (5–10%) в камерах сжигания, выполненных из стали, графита, кварца, огнеупорного кирпича. Наиб. совр. материал, предотвращающий загрязнение HCl,-графит, импрегнированный феноло-формальд. смолами. Для предотвращения взрывного характера горения реагенты смешивают непосредственно в факеле пламени горелки. В верх. зоне камер сжигания устанавливают теплообменники для охлаждения реакц. газов до 150–160 °C. Мощность совр. графитовых печей достигает 65 т/сут (в пересчете на 35%-ную С. к.). В случае дефицита H2 применяют разл. модификации процесса; напр., пропускают смесь Cl2 с водяным паром через слой пористого раскаленного угля:
2Cl2 + 2H2O + С : 4HCl + CO2 + 288,9 кДж
Температура процесса (1000–1600 °C) зависит от типа угля и наличия в нем примесей, являющихся катализаторами (напр., Fe2O3). Перспективно использование смеси CO с парами воды:
CO + H2O + Cl2 → 2HCl + CO2
Более 90% С. к. в развитых странах получают из абгаз-ного HCl, образующегося при хлорировании и дегидрохлорировании орг. соединений, пиролизе хлорорг. отходов, хлоридов металлов, получении калийных нехлорир. удобрений и др. Абгазы содержат разл. количества HCl, инертные примеси (N2, H2, CH4), малорастворимые в воде орг. вещества (хлорбензол, хлорметаны), водорастворимые вещества (уксусная кислота, хлораль), кислые примеси (Cl2, HF, O2) и воду. Применение изотермич. абсорбции целесообразно при низком содержании HCl в абгазах (но при содержании инертных примесей менее 40%). Наиб. перспективны пленочные абсорберы, позволяющие извлекать из исходного абгаза от 65 до 85% HCl.
Наиб. широко применяют схемы адиабатич. абсорбции. Абгазы вводят в ниж. часть абсорбера, а воду (или разбавленную С. к.) — противотоком в верхнюю. С. к. нагревается до температуры кипения благодаря теплоте растворения HCl. Изменение температуры абсорбции и концентрации HCl дано на рис. 1. Температура абсорбции определяется температурой кипения кислоты соответствующей концентрации (макс. температура-т. кип. азеотропной смеси — ок. 110 °C).
На рис. 2 дана типовая схема адиабатич. абсорбции HCl из абгазов, образующихся при хлорировании (напр., получение хлорбензола). HCl поглощается в абсорбере 1, а остатки малорастворимых в воде орг. веществ отделяют от воды после конденсации в аппарате 2, доочищают в хвостовой колонне 4 и сепараторах 3, 5 и получают товарную С. к.
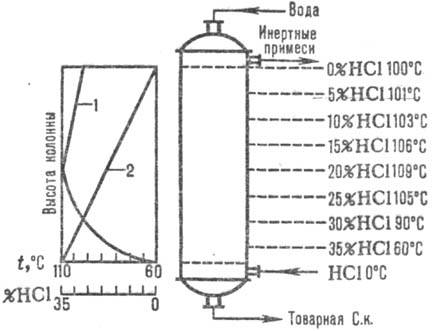
Рис. 1. Схема распределения температур (кривая 1) и концентрации (кривая 2) HCl по высоте адиабатич. абсорбера.
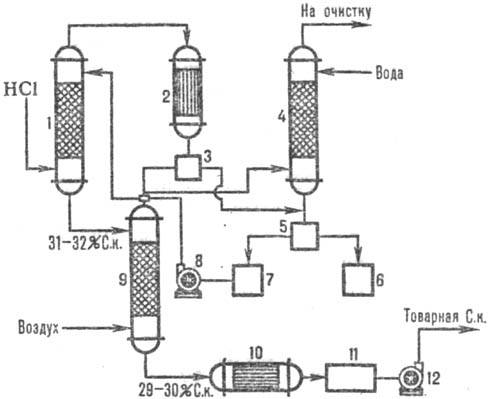
Рис. 2. Схема типовой адиабатич. абсорбции HCl из абгазов: 1 — адиабатич. абсорбер; 2 — конденсатор; 3, 5 — сепараторы; 4 — хвостовая колонна; 6 — сборник орг. фазы; 7 — сборник водной фазы; 8, 12 — насосы; 9 — отдувочная колонна; 10 — теплообменник; 11 — сборник товарной кислоты.
На рис. 3 дана типовая схема получения С. к. из абгазов с использованием комбинир. схемы абсорбции. В колонне адиабатич. абсорбции получают С. к. пониж. концентрации, но свободную от орг. примесей С. к. с повыш. концентрацией HCl производят в колонне изотермич. абсорбции при пониж. температурах. Степень извлечения HCl из абгазов95–99% (при использовании в качестве абсорбента разб. кислот) и практически полная — при использовании чистой воды.
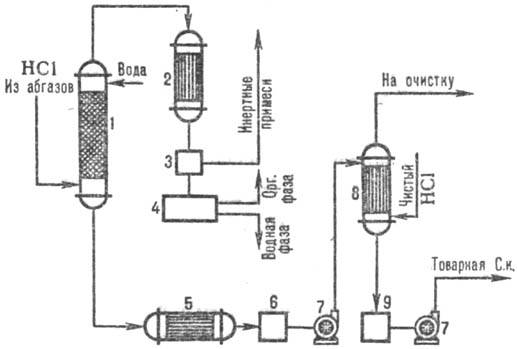
Рис. 3. Схема типовой комбинир. абсорбции HCl из абгазов: 1 — колонна адиабатич. абсорбции; 2 — конденсатор; 3 — отделитель газов; 4 — сепаратор; 5 — холодильник; 6, 9 — сборники кислоты; 7 — насосы; 8 — изотермич. абсорбер.
Определяют HCl в воздухе нефелометрически с образованием AgCl.
С. к. применяют для получения хлоридов Mn, Fe, Zn и др., для травления металлов, очистки поверхностей сосудов, скважин от карбонатов, обработки руд, при производстве каучуков, глу-тамината Na, соды, Cl2и т. д. Потребление С. к. в Японии (тыс. т); хим. промышленность 320,7, производство глутамината Na 99,8, производство соды 54,8, черная металлургия 50,0, целлюлозно-бумажная промышленность 22,2, прочие 80. HCl используют для регенерации Cl2, в орг. синтезе (получение винилхлорида, алкилхлоридов и т. д.), как катализатор (напр., при получении дифенилолпропана, алкилирование бензола).
Производство 31%-ной С. к. в СССР 1,52 млн. т (1986). HCl и С. к. токсичны, вызывают сильные ожоги слизистых оболочек, удушье, разрушают зубы и т. д. ПДК HCl в воздухе рабочей зоны 5,0 мг/м3.
Лит.: Якименко Л. М., Пасманик М. И., Справочник по производству хлора, каустической соды и основных хлорпродуктов, 2 изд., М., 1976; Левинский М. И., Мазанко А. Ф., Новиков И. Н., Хлористый водород и соляная кислота, М., 1985.
А. И. Торубаров
Источник:
Химическая энциклопедия
на Gufo.me
Значения в других словарях
- соляная кислота —
орф. соляная кислота
Орфографический словарь Лопатина - соляная кислота —
сущ., кол-во синонимов: 1 кислота 171
Словарь синонимов русского языка - Соляная кислота —
См. Хлористо-водородная кислота и Сульфат.
Энциклопедический словарь Брокгауза и Ефрона - соляная кислота —
СОЛЯНАЯ КИСЛОТА, то же, что хлористоводородная кислота.
Ветеринарный энциклопедический словарь - Соляная кислота —
Хлористо-водородная кислота, HCl, сильная одноосновная кислота, раствор хлористого водорода в воде. С. к. — бесцветная жидкость с острым запахом хлористого водорода. Техническая кислота имеет желтовато-зелёный цвет из-за примесей хлора и солей железа.
Большая советская энциклопедия - СОЛЯНАЯ КИСЛОТА —
СОЛЯНАЯ КИСЛОТА (НСl), водный раствор хлороводорода, бесцветного газа с резким запахом. Получают действием серной кислоты на поваренную соль, как побочный продукт хлорирования углеводородов, или реакцией водорода и хлора.
Научно-технический словарь - СОЛЯНАЯ КИСЛОТА —
СОЛЯНАЯ КИСЛОТА (хлористоводородная кислота) — раствор хлористого водорода в воде; сильная кислота. Бесцветная, «дымящая» на воздухе жидкость (техническая соляная кислота желтоватая из-за примесей Fe, Cl2 и др.).
Большой энциклопедический словарь


