Какие свойства характерны для металлов пластичность теплопроводность
Свойства металлов.
1.Основные свойства металлов.
Свойства металлов делятся на физические, химические, механические и технологические.
К физическим свойствам относятся: цвет, удельный вес, плавкость, электропроводность, магнитные свойства, теплопроводность, расширяемость при нагревании.
К химическим – окисляемость, растворимость и коррозионная стойкость.
К механическим – прочность, твердость, упругость, вязкость, пластичность.
К технологическим – прокаливаемость, жидкотекучесть, ковкость, свариемость, обрабатываемость резанием.
1. Физические и химические свойства.
Цвет. Металлы непрозрачны, т.е. не пропускают сквозь себя свет, и в этом отраженном свете каждый металл имеет свой особенный оттенок – цвет.
Из технических металлов окрашенными являются только медь (красная) и ее сплавы. Цвет остальных металлов колеблется от серо- стального до серебристо – белого. Тончайшие пленки окислов на поверхности металлических изделий придают им дополнительные окраски.
Удельный вес. Вес одного кубического сантиметра вещества, выраженный в граммах, называется удельным весом.
По величине удельного веса различают легкие металлы и тяжелые металлы. Из технических металлов легчайшим является магний ( удельный вес 1,74), наиболее тяжёлым – вольфрам (удельный вес 19,3). Удельный вес металлов в некоторой степени зависит от способа их производства и обработки.
Плавкость. Способность при нагревании переходить из твердого состояния в жидкое является важнейшим свойством металлов. При нагревании все металлы переходят из твердого состояния в жидкое, а при охлаждении расплавленного металла – из жидкого состояния в твердого. Температура плавления технических сплавов имеет не одну определённую температуру плавления, а интервал температур, иногда весьма значительный.
Электропроводность. Электропроводность заключается в переносе электричества свободными электронами. Электропроводность металлов в тысячи раз выше электропроводности неметаллических тел. При повышении температуры электропроводность металлов падет, и при понижении – возрастает. При приближении к абсолютному нулю (- 2730С) электропроводность беспредельно металлов колеблется от +2320 (олово) до 33700 (вольфрам). Большинство увеличивается (сопротивление, падает почти до нуля).
Электропроводность сплавов всегда ниже электропроводности одного из компонентов, составляющих сплавов.
Магнитные свойства. Явно магнитными (ферромагнитьными) являются только три металла: железо, никель, и кобальт, а также некоторые их сплавы. При нагревании до определённых температур эти металлы также теряют магнитные свойства. Некоторые сплавы железа и при комнатной температуре не являются ферромагнитными. Все прочие металлы разделяются на парамагнитные (притягивают магнитами) и диамагнитные (отталкиваются магнитами).
Теплопроводность. Теплопроводность называется переход тепла в теле от более нагретого места к менее нагретому без видимого перемещения частиц этого тела. Высокая теплопроводность металлов позволяет быстро и равномерно нагревать их и охлаждать.
Из технических металлов наибольшей теплопроводностью облает медь. Теплопроводность железа значительно ниже, а теплопроводность стали меняется в зависимости от содержания в ней компонентов. При повышении температуры теплопроводность уменьшается, при понижении – увеличивается.
Теплоёмкость. Теплоёмкость называется количество тепла, необходимое для повышения температуры тела на 10.
Удельной теплоемкостью вещества называется то количество тепла в килограмм – калориях, которое нужно сообщить 1кг вещества, чтобы повысить его температуру на 10.
Удельная теплоёмкость металлов в сравнении с другими веществами невелика, что позволяет относительно легко нагревать их до высоких температур.
Расширяемость при нагревании. Отношение приращения длины тела при его нагревании на 10 к первоначальной его длине называется коэффициентом линейного расширения. Для различных металлов коэффициентом линейного расширения колеблется в широких пределах. Так, например, вольфрам имеет коэффициент линейного расширения 4,0·10-6 , а свинец 29,5 ·10-6.
Коррозионная стойкость. Коррозия есть разрушение металла вследствие химического или электрохимического взаимодействия его с внешней средой. Примером коррозии является ржавление железа.
Высокая сопротивляемость коррозии (коррозионная стойкость) является важным природным свойством некоторых металлов: платины, золота и серебра, которые именно поэтому и получили название благородных. Хорошо сопротивляются коррозии также никель и другие цветные металлы. Черные металлы коррозируют сильнее и быстрее, чем цветные.
2. Механические свойства.
Прочность. Прочностью металла называют его способность сопротивляться действию внешних сил, не разрушаясь.
Твердость. Твердостью называется способность тела противостоять проникновению в него другого, более твердого тела.
Упругость. Упругостью металла называется его свойство востонавливать свою форму после прекращения действия внешних сил, вызывавших изменение формы(деформацию.)
Вязкость. Вязкость называется способность металла оказывать сопротивление быстро возрастающим (ударным) внешним силам. Вязкость – свойство, обратное хрупкости.
Пластичность. Пластичностию называется свойство металла деформироваться без разрушения под действием внешних сил и сохранять новую форму после прекращения действия сил. Пластичность – свойство, обратное упругости.
В табл. 1 приведены свойства технических металлов.
Таблица 1.
Свойства технических металлов.
3. Значение свойств металлов.
Механические свойства. Первое требование, предъявляемое ко всякому изделию, — это достаточная прочность.
Металлы обладают более высокой прочностью по сравнению с другими материалами, поэтому нагруженные детали машин, механизмов и сооружений обычно изготовляются из металлов.
Многие изделия, кроме общей прочности, должны обладать ещё особыми свойствами, характерными для работы данного изделия. Так, например, режущие инструменты должны обладать высокой твердостью. Для изготовления режущих других инструментов применяются инструментальные стали и сплавы.
Для изготовления рессор и пружин применяются специальные стали и сплавы, обладающие высокой упругостью
Вязкие металлы применяются в тех случаях, когда детали при работе подвергается ударной нагрузке.
Пластичность металлов дает возможность производить их обработку давлением (ковать, прокатывать).
Физические свойства. В авиа-, авто- и вагоностроении вес деталей часто является важнейшей характеристикой, поэтому сплавы алюминия и особенно магния являются здесь незаменимыми. Удельная прочность( отношение предела прочности к удельному весу) для некоторых, например алюминиевых, сплавов выше, чем для мягкой стали.
Плавкость используется для получения отливок путём заливки расплавленного металла в формы. Легкоплавкие металлы(например, свинец) используются в качестве закалочной среды для стали. Некоторые сложные сплавы имеют столь низкую температуру плавления, что расплавляется в горячей воде. Такие сплавы применяются для отливки типографических матриц, в приборах, служащих для предохранения от пожаров.
Металлы с высокой электропроводностью (медь, алюминий) используются в электромашиностроении, для устройства линий электропередач, а сплавы с высоким электросопротивлением – для ламп накаливания, электронагревательных приборов.
Магнитные свойства металлов играют первостепенную роль в электромашиностроении (динамомашины, мотора, трансформаторы),для приборов связи ( телефонные и телеграфные аппараты) и используются во многих других видах машин и приборов.
Теплопроводность металлов дает возможность производить их физические свойства. Теплопроводность используется также при производстве пайки и сварки металлов.
Некоторые сплавы металлов имеют коэффициент линейного расширения, близкий к нулю; такие сплавы применяются для изготовления точных приборов, радиоламп. Расширение металлов должно применяться во внимание при постройке длинных сооружений, например, мостов. Нужно также учитывать,что две детали, изготовленные из металлов с различным коэффициентом расширения и скрепленные между собой, при нагревании могут дать изгиб и даже разрушение.
Химические свойства. Коррозионная стойкость особенно важна для изделий, работающих в сильно окислительных средах (колосниковые решётки, детали химических машин и приборов). Для достижения высокой коррозионной стойкости производят специальные нержавеющие, кислостойкие и жаропрочные стали, а также применяются защитные покрытия.
Общие физические свойства мекталлов:
1) Пластичность — способность изменять форму при ударе, вытягиваться в проволоку, прокатываться в тонкие листы. В ряду — Au, Ag, Cu, Sn, Pb, Zn, Fe уменьшается.
2) Блеск, обычно серый цвет и непрозрачность. Это связано со взаимодействием свободных электронов с падающими на металл квантами света.
3) Электропроводность. Объясняется направленным движением свободных электронов от отрицательного полюса к положительному под влиянием небольшой разности потенциалов. В ряду — Ag, Cu, Al, Fe уменьшается. При нагревании электропроводность уменьшается, т. к. с повышением температуры усиливаются колебания атомов и ионов в узлах кристаллической решетки, что затрудняет направленное движение «электронного газа».
4) Теплопроводность. Закономерность та же. Обусловлена высокой подвижностью свободных электронов и колебательным движением атомов, благодаря чему происходит быстрое выравнивание температуры по массе металла. Наибольшая теплопроводность — у висмута и ртути.
5) Твердость. Самый твердый – хром (режет стекло) ; самые мягкие – щелочные металлы – калий, натрий, рубидий и цезий – режутся ножом.
6) Плотность. Она тем меньше, чем меньше атомная масса металла и чем больше радиус его атома (самый легкий — литий (r=0,53 г/см3); самый тяжелый – осмий (r=22,6 г/см3).
Металлы, имеющие r < 5 г/см3 считаются «легкими металлами».
7) Температуры плавления и кипения. Самый легкоплавкий металл – ртуть (т. пл. = -39°C), самый тугоплавкий металл – вольфрам (t°пл. = 3390°C).
Металлы с t°пл. выше 1000°C считаются тугоплавкими, ниже – низкоплавкими.
Все металлы являются восстановителями. Для металлов главных подгрупп восстановительная активность (способность отдавать электроны) возрастает сверху вниз и справа налево. Например, Натрий и кальций вытесняют водород из воды уже при обычных условиях:
Ca + 2H2O Ca(OH)2 + H2¬ ; 2Na + 2H2O 2NaOH + H20
А магний при повышении температуры:
Mg + H2O –t MgO + H2
Восстановительная способность и химическая активность элементов побочных подгрупп увеличивается снизу вверх по группе (например, серебро на воздухе окисляется, а золото нет; медь вытесняет серебро из его соли) :
Cu + 2AgNO3 → 2Ag ↓ + Cu(NO3)2
Cu0 -2 ē → Cu+2 1 О. О. В.
Ag+ + ē → Ag0 2 В. В. О.
Высшая положительная степень окисления для металлов главных подгрупп в их соединениях равна номеру группы (например, NaCl, MgCl2, AlCl3, SnCl4), а для металлов побочных подгрупп в их кислородосодержащих соединениях также часто совпадает с номером группы (например, ZnO, TiO2, V2O5, CrO3, KMnO4).
Свойства оксидов металлов слева направо по периоду и снизу вверх по группе изменяются от основных к амфотерным для металлов главных подгрупп (Na2O и MgO – основные оксиды, Al2O3 и BeO – амфотерные) . Для металлов побочных подгрупп свойства оксидов, в которых металлы проявляют свою высшую степень окисления, изменяются от основных через амфотерные к кислотным ( CuO — основной, ZnO — амфотерный, CrO3 — кислотный) .
Сила оснований, образуемых металлами главных подгрупп увеличивается справа налево по периоду и сверху вниз по группе ( Be(OH)2 и Al(OH)3– амфотерные гидроксиды, Mg(OH)2 — слабое основание, NaOHи – Ca(OH)2 сильные основания) . Гидраты оксидов металлов побочных подгрупп с высшими степенями окисления металла вдоль периода слева направо меняют свои свойства от оснований через амфотерные гидроксиды к кислотам ( Cu(OH)2 — основание, Zn(OH)2 — амфотерный гидроксид, H2CrO4 — кислота) .
В природе металлы встречаются в основном в виде соединений – оксидов или солей. Исключение составляют такие малоактивные металлы, как серебро, золото, платина, которые встречаются в самородном состоянии.
Все способы получения металлов основаны на процессах их восстановления из природных соединений.
Глава 2. Металлы
Из курса химии 9 класса вы уже имеете представление о природе химической связи, существующей в кристаллах металлов, — металлической связи. Напомним, что в узлах металлических кристаллических решёток располагаются атомы и положительные ионы металлов, связанные посредством обобществлённых внешних электронов, принадлежащих всему кристаллу. Эти электроны компенсируют силы электростатического отталкивания между положительными ионами и тем самым связывают их, обеспечивая устойчивость металлической решётки.
Металлическая связь обусловливает все важнейшие физические свойства металлов: пластичность, электро- и теплопроводность, металлический блеск и другие свойства, характерные для этого класса простых веществ.
Пластичность — это свойство вещества изменять форму под внешним воздействием и сохранять принятую форму после прекращения этого воздействия.
Способность расплющиваться от удара или вытягиваться в проволоку под действием силы составляет важнейшее механическое свойство металлов. Оно лежит в основе такой уважаемой большинством народов мира профессии, как профессия кузнеца. Недаром покровителем кузнечного дела у разных народов был бог огня: у греков — Гефест, у римлян — Вулкан, у славян — Сварог.
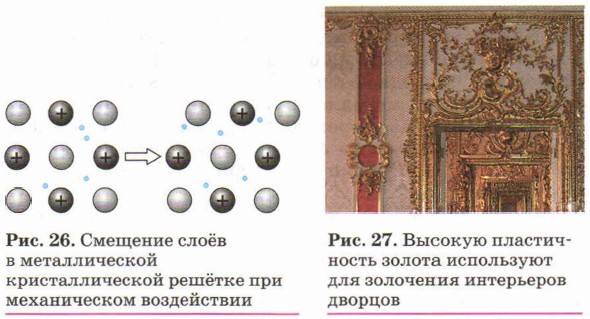
Пластичность металлов обусловлена способностью одних слоёв атом-ионов в кристаллах под внешним воздействием легко смещаться (как бы скользить) по отношению к другим слоям без разрыва связей между ними (рис. 26). Наиболее пластичны золото, серебро и медь. Например, из золота можно изготовить «золотую фольгу» толщиной 0,003 мм, которую используют для золочения изделий (рис. 27).
Высокая электропроводность большинства металлов обусловлена присутствием в их кристаллических решётках подвижных электронов, которые направленно перемещаются под действием электрического поля (рис. 28).
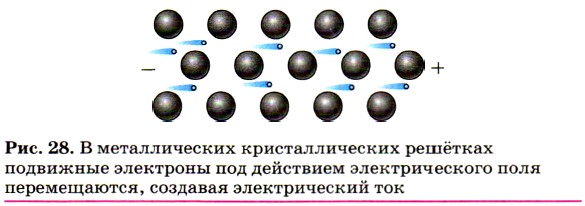
При нагревании колебательные движения ионов в кристалле усиливаются, что затрудняет направленное движение электронов и ведёт к снижению электрической проводимости. При охлаждении электропроводность металлов увеличивается и вблизи абсолютного нуля переходит в сверхпроводимость. Наибольшую электропроводность имеют серебро и медь, наименьшую — марганец, свинец, ртуть и вольфрам.
Такое свойство, как теплопроводность металлов, также связано с высокой подвижностью свободных электронов: сталкиваясь с колеблющимися в узлах решётки ионами, электроны обмениваются с ними энергией. С повышением температуры колебания ионов при посредстве электронов передаются другим ионам, и температура всего металлического предмета быстро выравнивается.
Для гладкой поверхности металлов характерен металлический блеск — результат отражения световых лучей. В порошкообразном состоянии большинство металлов теряет блеск, приобретая чёрную или серую окраску, и только алюминий и магний сохраняют блеск в порошке. Из алюминия, серебра и палладия, обладающих наиболее высокой отражательной способностью, изготовляют зеркала, в том числе и применяемые в прожекторах.
Для большинства металлов характерен белый или серый цвет. Золото и медь окрашены соответственно в жёлтый и жёлто-красный цвет.
Из других физических свойств металлов наибольший практический интерес представляют твёрдость, плотность и температура плавления.
Для большинства металлов характерен белый или серый цвет. Золото и медь окрашены соответственно в жёлтый и жёлто-красный цвет.
Из других физических свойств металлов наибольший практический интерес представляют твёрдость, плотность и температура плавления.
Для всех металлов (кроме ртути) при обычных условиях характерно твёрдое агрегатное состояние. Однако твёрдость их различна. Наиболее твёрдые — металлы побочной подгруппы VI группы (VIB группы) Периодической системы Д. И. Менделеева. Так, хром по твёрдости приближается к алмазу. Самые мягкие — металлы главной подгруппы I группы (IA группы) Периодической системы Д. И. Менделеева — щелочные металлы. Например, натрий и калий легко режутся ножом.

По плотности металлы делят на лёгкие (плотность меньше 5 г/см3) и тяжёлые (плотность больше 5 г/см3). К лёгким относят щелочные, щёлочноземельные металлы и алюминий. Из переходных металлов сюда включают скандий, иттрий и титан. Эти металлы, благодаря лёгкости и тугоплавкости, всё шире применяют в различных областях техники.
Самый лёгкий металл — это литий (р = 0,53 г/см3). Самый тяжёлый — осмий (р = 22,6 г/см3).
Лёгкие металлы обычно легкоплавки, галлий может плавиться уже на ладони руки, а тяжёлые металлы — тугоплавки. Наибольшей температурой плавления, которая равна 3380 °С, обладает вольфрам. Это свойство вольфрама используют для изготовления ламп накаливания (рис. 29, 2). Кроме него в конструкцию лампы входят ещё семь металлов.
В Российской Федерации в настоящее время, как и ранее в Евросоюзе и США, на государственном уровне принято решение о замене привычных ламп накаливания на более экономичные и долговечные современные лампы, например галогенные, люминесцентные и светодиодные. Галогенная лампа (рис. 29, 2) — это та же лампа накаливания с вольфрамовой нитью, заполненная инертными газами с добавкой паров галогенов (брома или иода).

Люминесцентные (рис. 29, 3) — это хорошо знакомые вам лампы дневного света, имеющие один существенный недостаток — они содержат ртуть, а потому нуждаются в соблюдении особых правил утилизации на специальных пунктах приёма. Светодиодные лампы (рис. 29, 4) — самые экономичные и самые долговечные (срок работы до 100 тыс. ч), но пока и самые дорогие из ламп.
В технике, как вы уже знаете, металлы делят на чёрные (железо и его сплавы) и цветные (все остальные, более подробно о них будет рассказано в следующем параграфе) (рис. 30). Золото, серебро, платину и некоторые другие металлы относят к драгоценным металлам (рис. 31). 1


1. Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания.
2. Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока — сделайте сообщение по ключевым словам и слово-сочетаниям следующего параграфа.

1. Назовите самый легкоплавкий металл.
2. Какие физические свойства металлов используют в технике?
3. Фотоэффект, т. е. свойство металлов испускать электроны под действием лучей света, характерен для щелочных металлов, например для цезия. Почему? Где это свойство находит применение?
4. Какие физические свойства вольфрама лежат в основе его применения в лампах накаливания?
5. Какие свойства металлов лежат в основе образных литературных выражений: «серебряный иней», «золотая заря», «свинцовые тучи»?
- Физические свойства металлов. Ответы
