Какие химические свойства у углекислого газа

Общие химические свойства углекислого газа: CO2 инертен, то есть химически не активен; при попадании в водный раствор легко вступает в реакции.
Большинство кислотных оксидов устойчивы к высоким температурам, но углекислота при их воздействии восстанавливается.
Взаимодействие с другими веществами:
1) Углекислота относится к кислотным оксидам, то есть в сочетании с водой образуется кислота. Однако угольная кислота неустойчива и распадается сразу. Эта реакция имеет обратимый характер:
СО2 + H2O ↔ CO2 × H2O (растворение) ↔ Н2СО3
Диоксид углерода + вода ↔ угольная кислота
Молекула угольной кислоты
2) При взаимодействии углекислого газа и соединений азота с водородом (аммиаком) в водном растворе происходит разложение до углеаммонийной соли.
2NH3 + CO2 + H2O = NH4HCO3
Аммиак + углекислота = гидрокарбонат аммония

Углеаммонийная соль
Полученное вещество часто используется в приготовлении хлеба и различных кондитерских изделий.
3) Ход некоторых реакций должен поддерживаться высокими температурами. Примером является производство мочевины при 130 °C и давлении 200 атм., схематически изображаемое так:
2NH3 + СО2 → (NH2)2СО + H2O
Аммиак + диоксид углерода → карбамид + вода
Также под воздействием температуры около 800 градусов протекает реакция образования оксида цинка:
Zn + CO2 → ZnO + CO

Оксид цинка
Цинк + двуокись углерода → оксид цинка + оксид углерода
4) Возможно уравнение с гидроксидом бария, при котором выделяется средняя соль.
Ba(OH)2+CO2 = BaCO3 + H2O
Гидроксид бария + углекислота = карбонат бария + оксид водорода.
Применяется для регулировки калориметров по теплоемкости. Также вещество используют в промышленности для производства красных кирпичей, синтетических тканей, фейерверков, гончарных изделий, плитки для ванн и туалетов.
5) Углекислый газ выделяется при реакциях горения.
Горение метана.
CH4 + 2O2 → CO2 + 2H2O + 891кДж

Горение газа на плите
Метан + кислород = углекислота + вода (в газообразном состоянии) + энергия
Горение этилена
C2H4 + 3O2 → 2CO2 + 2H2O + Q
Этилен + кислород = диоксид углерода + оксид водорода + энергия
Горение этана
2С2Н6 + 7О2 → 4CO2 + 6H2O + Q
Этан + кислород = двуокись углерода + вода + энергия
Горение этанола
C2H5OH + 3O2 = 3H2O + 2CO2 + Q
Молекула этанола
Этанол + кислород = вода + углекислота + энергия
6) Газ не поддерживает горения, этот процесс возможен только с некоторыми активными металлами, например, магнием.
2Mg + CO2 = C + 2MgO
Магний + углекислота = углерод + оксид магния.
MgO активно применяется при производстве косметических средств. Вещество используют в пищевой промышленности как пищевую добавку.
7) Двуокись углерода реагирует с гидроксидами с получением солей, которые существуют в двух формах, как карбонаты и бикарбонаты. Например, углекислый газ и гидроксид натрия, согласно формуле, образуют гидрокарбонат Na:
CO2 + NaOH → NaHCO3
диоксид углерода + гидроксид натрия → гидрокарбонат натрия.
Или же при большем количестве NaOH образуется карбонат Na с образованием воды:
CO2 + 2 NaOH → Na2CO3 + H2O
Диоксид углерода + гидроксид натрия → карбонат натрия + вода
Кислотно-щелочные реакции углекислоты используются на протяжении веков для затвердевания известкового раствора, что может быть выражено простым уравнением:
Ca(OH)2 + CO2 → CaCO3 + H2O
Гидроксид кальция + двуокись углерода → карбонат кальция + оксид водорода
8) В зелёных растениях играет важную роль в процессе фотосинтеза:
6CO2 + 6H2O → C6H12O6 + 6O2
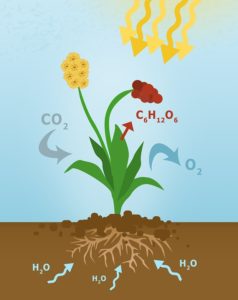
Образование глюкозы
Диоксид углерода + вода → глюкоза + кислород.
9) Химические свойства углекислоты используются в промышленности при производстве соды, суть этого процесса можно выразить суммарным уравнением:
NaCl + CO2 + NH3 + H2O → NaHCO3 + NH4Cl
Хлорид натрия + Диоксид углерода + аммиак + вода → гидрокарбонат натрия + хлорид аммония
10) Фенолят Na разлагается при взаимодействии с углекислым газом, при этом малорастворимый фенол выпадает в осадок:
C6H5ONa + CO2 + H2O = C6H5OH + NaHCO3
Фенолят натрия + двуокись углерода + оксид водорода = фенол + гидрокарбонат натрия
11) Пероксид натрия и углекислый газ, взаимодействуя, образуют среднюю соль карбоната Na с выделением кислорода.
2Na2O2 + 2CO2 → 2N2CO3 + O2
Пероксид натрия + углекислота → карбонат натрия + кислород

Колба с пероксидом натрия
Образование углекислоты происходит при растворении в воде кальцинированной соды (стиральной соды).
NaHCO3 + H2O → CO2 + H2O + NaOH
Гидрокарбонат натрия + вода → углекислота + вода + гидроксид натрия
При этой реакции (гидролиз по катиону) образуется сильнощелочная среда.
12) CO2 вступает в реакцию с гидроксидом калия, последний образуется путем электролиза хлористого калия.
2KOH + CO2 → K2CO3 + H2O
Гидроксид калия + углекислота → карбонат калия + вода
13) Газ в силу своего строения не реагирует с благородными газами, то есть гелием, неоном, аргоном, криптоном, ксеноном, радоном, оганесоном.
Заключение
Мы привели большую часть химических реакций, в которых участвует CO2. Ученые всего мира пытаются решить проблему увеличения концентрации углекислоты в воздухе, не без помощи реакций с другими веществами, которые известны химикам. А какие химические формулы взаимодействия углекислого газа знаете вы?
Оксид
углерода (IV) СO2 – углекислый газ
Физические свойства:
Углекислый газ, бесцветный, без запаха, растворимость в воде — в 1V H2O
растворяется 0,9V CO2 (при нормальных условиях); тяжелее воздуха;
t°пл.= -78,5°C (твёрдый CO2 называется «сухой лёд»); не
поддерживает горение.
Строение молекулы:
Углекислый газ имеет
следующие электронную и структурную формулы —
O=C=O |
Все четыре связи
ковалентые полярные.
Получение:
1.
Термическим разложением солей угольной кислоты (карбонатов). Обжиг известняка –
в промышленности:
CaCO3 t=1200˚C→ CaO + CO2
2.
Действием сильных кислот на карбонаты и гидрокарбонаты –
в лаборатории:
CaCO3 (мрамор) + 2HCl →
CaCl2 + H2O + CO2
NaHCO3
+ HCl
→
NaCl
+ H2O + CO2
Способы собирания
вытеснением воздуха |
3. Сгорание
углеродсодержащих веществ:
СН4 + 2О2→ 2H2O + CO2
4. При медленном
окислении в биохимических процессах (дыхание, гниение, брожение)
Химические свойства:
Видео «Химические свойства углекислого газа»
Кислотный оксид:
1)
с водой даёт непрочную угольную кислоту:
СО2 + Н2О
↔ Н2СО3
2)
реагирует с основными оксидами и основаниями, образуя соли угольной
кислоты
Na2O + CO2→ Na2CO3
2NaOH + CO2→ Na2CO3 + H2O
NaOH + CO2(избыток) → NaHCO3
3)
При повышенной температуре может проявлять окислительные свойства – окисляет
металлы — СO2
+ Me = MexOy
+ C
С+4O2
+ 2Mg t˚C→ 2Mg+2O
+ C0
Видео «Горение магния в углекислом газе»
Качественная
реакция на углекислый газ:
Помутнение известковой
воды Ca(OH)2 за счёт образования
белого осадка – нерастворимой соли CaCO3:
Ca(OH)2 + CO2 →
CaCO3
↓+ H2O
Применение углекислого
газа:

Видео «Тушение пламени углекислым газом»
Угольная
кислота и её соли
Химическая
формула — H2CO3
Структурная формула
– все связи ковалентные полярные:
Кислота слабая, существует
только в водном растворе, очень непрочная, разлагается на углекислый газ и воду:
CO2
+ H2O ↔ H2CO3
Опыт «Разложение угольной кислоты»
Опыт «Получение»
Опыт «Получение угольной кислоты»
Химические свойства:
Для угольной кислоты характерны
все свойства кислот.
1) Диссоциация – двухосновная
кислота, диссоциирует слабо в две ступени, индикатор — лакмус краснеет в водном
растворе:
H2CO3
↔ H+
+ HCO3-(гидрокарбонат-ион)
HCO3-
↔ H+
+ CO32- (карбонат-ион)
2) с активными металлами
H2CO3
+ Ca
= CaCO3
+ H2↑
3) с основными оксидами
H2CO3
+ CaO
= CaCO3
+ H2O
4) с основаниями
H2CO3(изб) + NaOH = NaHCO3 + H2O
H2CO3
+ 2NaOH = Na2CO3 + 2H2O
5) Очень непрочная
кислота – разлагается
Соли
угольной кислоты – карбонаты и гидрокарбонаты
Угольная кислота
образует два ряда солей:
·
Средние соли — карбонаты Na2СO3,
(NH4)2CO3
·
Кислые соли — бикарбонаты,
гидрокарбонаты NaHCO3
, Ca(HCO3)2
В природе встречаются:
CaCO3
мел

мрамор

известняк

NaHCO3 – питьевая сода


K2CO3(поташ,
в золе растений)
Na2CO3
– сода, кальцинированная сода
Na2CO3 x 10H2O – кристаллическая сода
Физические свойства:
Все карбонаты – твёрдые
кристаллические вещества. Большинство из них в воде не растворяются.
Гидрокарбонаты растворяются в воде.
Химические свойства
солей угольной кислоты:
Общие
свойства солей:
1) Вступают в реакции
обмена с другими растворимыми солями
Na2CO3
+ CaCl2
= CaCO3↓
+ 2NaCl
2) Разложение
гидрокарбонатов при нагревании
NaHCO3t˚C→Na2CO3
+ H2O + CO2↑
3) Разложение
нерастворимых карбонатов при нагревании
CaCO3t˚C→ CaO+ CO2↑
4) Карбонаты и гидрокарбонаты
могут превращаться друг в друга:
Опыт «Взаимопревращение карбонатов и гидрокарбонатов»
гидрокарбонатывкарбонаты
Me(HCO3)n + Me(OH)n →
MeCO3+H2O
Me(HCO3)nt˚C → MeCO3↓+H2O+CO2↑
карбонатывгидрокарбонаты
MeCO3+H2O+CO2= Me(HCO3)n
Специфические свойства:
1) Качественная реакция на CO32- карбонат – ион
«вскипание»
при действии сильной кислоты:
Na2CO3 + 2HCl =
2NaCl
+ H2O + CO2↑
ЗАДАНИЯ ДЛЯ ЗАКРЕПЛЕНИЯ
№ 1. Закончите уравнения осуществимых химических реакций:
CO 2+ KOH =
CO + Al =
H2CO3+ K2SO4 =
CO2( изб ) + NaOH =
С O2+ Na2O =
CaCO3+ CO2 + H2O =
CO2+ Ca(OH)2 =
CO + CaO =
CO2+ H2SO4 =
Ca(HCO3)2+ Ca(OH)2=
H2CO3+ NaCl =
C + ZnO =
№2.
Осуществите превращения по схеме:
1) Al 4 C 3→ CH 4→ CO 2→ CaCO 3→ Ca ( HCO 3)2→ CaCO 3
2) Ca → CaC 2→ Ca ( OH )2→ CaCO 3→ CO 2→ C
3) CO2 → H2CO3 → Na2CO3 → CO2
4) CaCO3 → CO2 → NaHCO3 → Na2CO3
№3. Решите задачи
1.Какой объём углекислого газа выделится при обжиге карбоната кальция массой 200 г
2. Сколько угольной кислоты можно получить при взаимодействии 2 л
углекислого газа (н.у.) с водой, если выход кислоты составил 90% по
сравнению с теоретическим
Составная часть атмосферы, основное сырье для процесса фотосинтеза зеленых растений, продукт жизнедеятельности живых организмов.
По систематической международной номенклатуре (IUPAC) вещество с формулой СО2 получило название – Оксид углерода(IV). Тривиальные (общепринятые названия) – двуокись или диоксид углерода, угольный ангидрид (солеобразующий оксид, обладающий кислотными свойствами).
Формула углекислого газа
СО2
Молекула углекислого газа образована двумя атомами кислорода и атомом углерода. Структурная формула – О=С=О. Валентность углерода равна 4. Степень окисления – (+4). Тип связи – ковалентная полярная.
Получение углекислого газа
Природные источники углекислого газа
Углекислый газ образуется при медленном окислении в процессах дыхания, брожения, гниения органических веществ. Выделяется при разложении природных карбонатов, сгорании топлива, образовании дымовых газов. Содержится в воздухе, минеральных источниках.
В сутки организм человека выделяет 1 кг СО2. В воздухе содержится 0,03% углекислого газа.
Лабораторные способы получения
В лаборатории газ можно получить взаимодействием соляной кислоты с мелом, мрамором, содой. Собирается газ методом вытеснения воздуха.
CaCO3 + 2HCl → CaCl2+ H2O + CO2,
NaHCO3+ HCl → NaCl + H2O + CO2.
Промышленные способы получения
- Обжиг известняка: CaCO3 → CaO + CO2.
- Как побочный продут разделения воздуха при получении кислорода, азота, аргона.
Свойства углекислого газа
Физические свойства
Вещество нетоксичное, негорючее.
| Свойство | Описание |
|---|---|
| Агрегатное состояние при н.у. | Газ |
| Цвет | Бесцветный |
| Запах | Без запаха |
| Температура плавления | -750оC |
| Температура кипения | -56,50оC |
| Растворимость в воде | Растворяется частично. При t +150оC в 1 литре воды может раствориться 1,7 л углекислого газа |
| Плотность | 1,977 г/л |
| Молярная масса | 44г/моль |
Вещество в твердом агрегатном состоянии называется «сухим льдом».
Высокую концентрацию диоксида углерода можно определить органолептически – во рту, на языке появляется кисловатый привкус. Повышенное содержание опасно для организма – вызывает удушье.
Химические свойства
- Качественная реакция: при взаимодействии углекислого газа с известковым молочком (гидроксидом кальция) образуется карбонат кальция – осадок белого цвета.
CO2 + Ca(OH)2 = CaCO3↓ + H2O.
- CO2, как кислотный оксид, реагирует с водой с образованием угольной кислоты. Эта кислота – соединение нестойкое, легко распадается на углекислый газ и воду. Тип реакции – реакция соединения, обратимая.
CO2 + H2O ↔ H2CO3.
При нагревании распадается на оксид углерода(II) и воду: 2CO2 = 2CO + O2.
Взаимодействует с основными оксидами, с образованием солей:
CaO + CO2 = CaCO3; Al2O3 + 3CO2 = Al2(CO3)3.
Тип реакции – реакция соединения.
- Взаимодействует со щелочами, с образованием кислых и средних солей:
CO2 + NaOH = NaHCO3;
CO2 + 2NaOH = Na2CO3 + H2O.
Средняя соль образуется при избытке щелочи. Кислая соль образуется при отношении количеств вещества оксида и щелочи – 1:1.
- При температуре реагирует с активными металлами:
CO2 + 2Mg = C + 2MgO
Углекислый газ в основном проявляет восстановительные свойства, но при взаимодействии с активными металлами является окислителем.
- Вступает в реакции взаимодействия с простыми веществами:
CO2 + 4H2 = CH4 + 2H2O (условия протекания реакции – высокая температура, катализатор Cu2O).
Применение углекислого газа
В пищевой промышленности:
- используется при производстве минеральной воды и газированных напитков;
- как пищевая добавка (Е290), повышает сроки хранения продуктов;
- в качестве разрыхлителя придает легкость и пышность кондитерским изделиям;
- как хладогент;
- для удаления из кофе кофеина.
В авиамоделировании используется как источник энергии для двигателей; применяется в пневматическом оружии; как заправка для углекислотных огнетушителей. Используется в качестве защитной среды при сварке.
Находит углекислый газ применение и в медицине – используется для криоабляции новообразований, служит стимулятором глубокого дыхания.
В химической промышленности газ используется в синтезе химических веществ, производстве солей угольной кислоты, процессах осушки и очистки полимеров, волокон растительного и животного происхождения. Применяется для очистки сточных вод, повышает проводимость сверхчистой воды.
Примеры решения задач
Задача 1
Найти массовую долю углерода в углекислом газе.
Решение
М(СО2) = 12+2х16 = 44 г/моль.
Аr(С) = 12 г/моль.
W(С) = 12/44 = 0,27 или 27%
Ответ: массовая доля углерода в углекислом газе равна 27%.
Задача 2
Вычислить объем углекислого газа, выделившегося при взаимодействии соляной кислоты с мрамором массой 100 г.
Решение
300 г — х л
CaCO3 + 2HCl → CaCl2+ H2O + CO2
1 моль — 1 моль
100 г/моль — 22,4 л/моль
100 г — 22,4 л
х(СО2) = 300х22,4/100 = 67, 2 (л).
Ответ: Объем углекислого газа равен 67, 2 л.
Физические и химические свойства углекислого газа
ОПРЕДЕЛЕНИЕ
Углекислый газ (двуокись углерода, угольный ангидрид, диоксид углерода) – оксид углерода (IV).
Формула – (
mathrm{CO}_{2}
). Молярная масса – 44 г/моль.
Химические свойства углекислого газа
Углекислый газ относится к классу кислотных оксидов, т.е. при взаимодействии с водой он образует кислоту, которая называется угольная. Угольная кислота химически неустойчива и в момент образования сразу же распадается на составляющие, т.е. реакция взаимодействия углекислого газа с водой носит обратимый характер:
(
mathrm{CO}_{2}+mathrm{H}_{2} mathrm{O} leftrightarrow mathrm{CO}_{2} times mathrm{H}_{2} mathrm{O}(text { solution }) leftrightarrow mathrm{H}_{2} mathrm{CO}_{3}
).
При нагревании углекислый газ распадается на угарный газ и кислород:
(
2 mathrm{CO}_{2}=2 mathrm{CO}+mathrm{O}_{2}
)
Как и для всех кислотных оксидов, для углекислого газа характерны реакции взаимодействия с основными оксидами (образованными только активными металлами) и основаниями:
(
mathrm{CaO}+mathrm{CO}_{2}=mathrm{CaCO}_{3}
);
(
mathrm{Al}_{2} mathrm{O}_{3}+3 mathrm{CO}_{2}=mathrm{Al}_{2}left(mathrm{CO}_{3}right)_{3}
);
(
mathrm{CO}_{2}+mathrm{NaOH}_{(text { dilute })}=mathrm{NaHCO}_{3}
);
(
mathrm{CO}_{2}+2 mathrm{NaOH}_{(mathrm{conc})}=mathrm{Na}_{2} mathrm{CO}_{3}+mathrm{H}_{2} mathrm{O}
).
Углекислый газ не поддерживает горения, в нем горят только активные металлы:
(
mathrm{CO}_{2}+2 mathrm{Mg}=mathrm{C}+2 mathrm{MgO}left(mathrm{t}^{circ}right)
);
(
mathrm{CO}_{2}+2 mathrm{Ca}=mathrm{C}+2 mathrm{CaO}left(mathrm{t}^{circ}right)
).
Углекислый газ вступает в реакции взаимодействия с простыми веществами, такими как водород и углерод:
(
mathrm{CO}_{2}+4 mathrm{H}_{2}=mathrm{CH}_{4}+2 mathrm{H}_{2} mathrm{O}left(mathrm{t}^{circ}, mathrm{kat}=mathrm{Cu}_{2} mathrm{O}right)
);
(
mathrm{CO}_{2}+mathrm{C}=2 mathrm{CO}left(mathrm{t}^{circ}right)
).
При взаимодействии углекислого газа с пероксидами активных металлов образуются карбонаты и выделяется кислород:
(
2 mathrm{CO}_{2}+2 mathrm{Na}_{2} mathrm{O}_{2}=2 mathrm{Na}_{2} mathrm{CO}_{3}+mathrm{O}_{2} uparrow
).
Качественной реакцией на углекислый газ является реакция его взаимодействия с известковой водой (молоком), т.е. с гидроксидом кальция, в которой образуется осадок белого цвета – карбонат кальция:
(
mathrm{CO}_{2}+mathrm{Ca}(mathrm{OH})_{2}=mathrm{CaCO}_{3 downarrow}+mathrm{H}_{2} mathrm{O}
).
Физические свойства углекислого газа
Углекислый газ – газообразное вещество без цвета и запаха. Тяжелее воздуха. Термически устойчив. При сжатии и охлаждении легко переходит в жидкое и твердое состояния. Углекислый газ в твердом агрегатном состоянии носит название «сухой лед» и легко возгоняется при комнатной температуре. Углекислый газ плохо растворим в воде, частично реагирует с ней. Плотность – 1,977 г/л.
Получение и применение углекислого газа
Выделяют промышленные и лабораторные способы получения углекислого газа. Так, в промышленности его получают обжигом известняка (1), а в лаборатории – действием сильных кислот на соли угольной кислоты (2):
(
mathrm{CaCO}_{3}=mathrm{CaO}+mathrm{CO}_{2}left(mathrm{t}^{circ}right)(1)
);
(
mathrm{CaCO}_{3}+2 mathrm{HCl}=mathrm{CaCl}_{2}+mathrm{CO}_{2} uparrow+mathrm{H}_{2} mathrm{O}(2)
).
Углекислый газ используется в пищевой (газирование лимонада), химической (регулировка температур при производстве синтетических волокон), металлургической (защита окружающей среды, например, осаждение бурого газа) и других отраслях промышленности.
Примеры решения задач
ПРИМЕР 1
Задание Какой объем углекислого газа выделится при действии 200 г 10%-го раствора азотной кислоты на 90 г карбоната кальция, содержащего 8% примесей, нерастворимых в кислоте?
Решение Молярные массы азотной кислоты и карбоната кальция, рассчитанные с использованием таблицы химических элементов Д.И. Менделеева – 63 и 100 г/моль, соответственно.
Запишем уравнение растворения известняка в азотной кислоте:
(
mathrm{CaCO}_{3}+2 mathrm{HNO}_{3} rightarrow mathrm{Ca}left(mathrm{NO}_{3}right)_{2}+mathrm{CO}_{2} uparrow+mathrm{H}_{2} mathrm{O}
).
Содержание чистого (без примесей) карбоната кальция в известняке:
(
omegaleft(mathrm{CaCO}_{3}right)_{mathrm{cl}}=100 %-omega_{text { admixture }}=100 %-8 %=92 %=0,92
).
Тогда, масса чистого карбоната кальция:
(
mleft(mathrm{CaCO}_{3}right)_{mathrm{cl}}=mathrm{m}_{text { limestone }} times omegaleft(mathrm{CaCO}_{3}right)_{mathrm{cl}} / 100 %
);
(
mathrm{m}left(mathrm{CaCO}_{3}right)_{mathrm{cl}}=90 times 92 / 100 %=82,8 mathrm{г}
).
Количество вещества карбоната кальция равно:
(
nleft(C a C O_{3}right)=mleft(C a C O_{3}right)_{C l} / Mleft(C a C O_{3}right)
);
(
nleft(mathrm{CaCO}_{3}right)=82,8 / 100=0,83 mathrm{моль}
)
Масса азотной кислоты в растворе будет равна:
(
mathrm{m}left(mathrm{HNO}_{3}right)=mathrm{m}left(mathrm{HNO}_{3}right)_{text { solution }} times omegaleft(mathrm{HNO}_{3}right) / 100 %
);
(
mathrm{m}left(mathrm{HNO}_{3}right)=200 times 10 / 100 %=20 mathrm{г}
)
Количество вещества азотной кислоты кальция равно:
(
mathrm{n}left(mathrm{HNO}_{3}right)=mathrm{m}left(mathrm{HNO}_{3}right) / mathrm{M}left(mathrm{HNO}_{3}right)
)
(
nleft(H N O_{3}right)=20 / 63=0,32
) моль
Сравнивая количества веществ, вступивших в реакцию, определяем, что азотная кислота находится в недостатке, следовательно дальнейшие расчеты производим по азотной кислоте. Согласно уравнению реакции (
n(H N O 3) : n(C O 2)=2 : 1
), следовательно n(CO2) = 1/2×n(HNO3) = 0,16 моль. Тогда, объем углекислого газа будет равен:
V(CO2) = n(CO2)×Vm ;
V(CO2) = 0,16×22,4 = 3,58 г.
Ответ Объем углекислого газа — 3,58 г.
ПРИМЕР 2
Задание Найдите объем углекислого газа массой 35 г.
Решение Масса вещества и его объем связаны между собой через количество вещества. Запишем формулы для вычисления количества вещества с помощью его массы и объема:
(
mathrm{n}=mathrm{m} / mathrm{M}
);
(
mathrm{n}=mathrm{V} / mathrm{V}_{mathrm{m}}
).
Приравняет выражения, записанные справа и выразим объем:
(
mathrm{m} / mathrm{M}=mathrm{V} / mathrm{V}_{mathrm{m}}
);
(
mathrm{V}=mathrm{m} times mathrm{V}_{mathrm{m}} / mathrm{M}
).
Вычислим по выведенной формуле объем углекислого газа. Молярная масса углекислого газа, рассчитанная с использованием таблицы химических элементов Д.И. Менделеева – 44 г/моль.
(
Vleft(C O_{2}right)=35 times 22,4 / 44=17,82
) л.
Ответ Объем углекислого газа — 17,82 л.
