Какие химические свойства у азота


Азот — первый представитель главной подгруппы пятой группы, представитель пниктогенов. Именно поэтому эти элементы называют подгруппой азота. Однако азот имеет ряд особенностей:
Число ковалентных связей, образуемых атомом азота по обменному механизму, не может быть больше 3-х, так как у атома азота на внешнем электронном слое отсутствует d-орбиталь.
Электронная конфигурация атома азота: $1s^22s^22p^3$Атом азота может образовывать ковалентную связь по донорно-акцепторному механизму за счет наличия неподеленной электронной пары на 2s-подуровне. Подробнее эта тема раскрыта в разделе «Валентные возможности азота»

Высшая валентность N равна IV.
3. В соединениях с кислородом азот проявляет степени окисления: +1; +2; +3; +4; +5.
Степени окисления азота в его соединениях
| $N^{-3}$ | $N^0$ | $N^{+1}$ | $N^{+2}$ | $N^{+3}$ | $N^{+4}$ | $N^{+5}$ |
|---|---|---|---|---|---|---|
$NH_3$ аммиак летучее водородное соединение | $N_2$ свободный азот | $N_2O$ $NO$ низшие оксиды, несолеобразующие | $N_2O_3$ $to$ $NO$ + $NO_2$ неустойчивый кислотный оксид | $NO_2$ $leftrightarrow$ $N_2O_4$ кислотный оксид | $2N_2O_5$ → $4NO_2$ + $O_2$ неустойчивый кислотный оксид | |
| В воздухе | $HNO_2$ азотистая кислота | $HNO_3$ азотная кислота | ||||
$NH_4K$ соли аммония $Me_xN_y$ нитриды | $Me(NO_2)_х$ нитриты | $Me(NO_3)_х$ нитраты | ||||
История открытия азота
Соединения азота — селитра, азотная кислота, аммиак — были известны задолго до получения азота в свободном состоянии.

В 1772 г. Д.Резерфорд, сжигая фосфор и другие в-ва в стеклянном колоколе, показал, что остающийся газ не поддерживает дыхания и горения. Д.Резерфорд назвал его «удушливым воздухом».
 К.Шееле назвал этот элемент, извлеченный из воздуха, «дурным воздухом».
К.Шееле назвал этот элемент, извлеченный из воздуха, «дурным воздухом».
В 1787 г. А.Лавуазье установил, что «жизненный» и «удушливый» газы, входящие в состав воздуха, это простые вещества, и предложил название «азот». «А» — отсутствие, «зоо» — жизнь. «Безжизненный» — азот.
И не случайно: испытания проводили на лабораторных мышах, помещая их под колпак с азотом, где они погибали.


ФИЗИЧЕСКИЕ СВОЙСТВА АЗОТА
Входит в состав воздуха: $varphi$ $(N_2)$ = 78%. Также входит в состав других неорганических соединений и состав живой материи.
Азот
немного легче воздуха; плотность 1,2506 $textrm{$кг/м^3$}$ (при н.у.),
$t_{textrm{пл.}}$ = — 209,8 $^circ C$, $t_{textrm{кип.}}$ = -195,8 $^circ C$
азот сжижается с трудом: плотность жидкого азота 800 $textrm{$кг/м^3$}$.
Жидкий азот используют для охлаждения различного оборудования и техники; для охлаждения компонентов компьютера при экстремальном разгоне. В химии жидкий азот применяют при работе с вакуумными линиями, для охлаждения веществ и проведения реакций при низких температурах, для создания инертной атмосферы. При этом транспортировка азота осуществляется в сосудах Дьюара:


В воде азот менее растворим чем кислород: при 0 $^circ C$ в 1$textrm{$м^3$}$ $H_2O$ растворяется 23,3 г азота.
Азот не поддерживает дыхание и горение; он чрезвычайно инертен. Малая реакционная способность азота обусловлена строением его молекулы.

N≡N — это самая прочная (из всех двухатомных) молекула. Молекула азота очень устойчива: энергия диссоциации ее на атомы составляет 942,9 кДж/моль, поэтому даже при температуре 3300 $^circС$ степень диссоциации азота составляет 0,1%.
Азот – один из распространенных элементов на Земле.

— в атмосфере — 4$cdot10^{15}$ тонн по массе и 78% газообразного азота по объёму;
— литосфере – 1,9$cdot10^{-3}$% по массе;
— в живых организмах — 0,3% по массе.
В белке животных и человека — 16–17% азота. В организмах человека и плотоядных животных белок образуется за счёт потребляемых белковых веществ травоядных животных и в растениях. “Жизнь — есть способ существования белковых тел на Земле” — по определению Ф.Энгельса.
СПОСОБЫ ПОЛУЧЕНИЯ АЗОТА
Промышленные способы:
Ректификация (разделение) жидкого воздуха:
сначала улетучивается $N_2$ (t$_{textrm{кип.}}$= -196$ ^circ C$);
затем $О_2$ (t$_{textrm{кип.}}$ = -183,0 $^circ C$)
Лабораторные способы:
Окислительно-восстановительное разложение некоторых солей аммония:
$NH_4NO_2$ = $N_2$ + $2H_2O$
$(NH_4)_2Cr_2O_7$ = $Cr_2O_3$ + $N_2$ + $4H_2O$
Окисление аммиака и солей аммония:
$4NH_3$ + $3O_2$ = $2N_2$ + $6H_2O$
$8NH_3$+ $3Br_2$ = $N_2$ + $6NH_4Br$
$NaNO_2 + NH_4Cl xrightarrow[]{t, ^circ C} NaCl + N_2 + 2H_2O$
ХИМИЧЕСКИЕ СВОЙСТВА АЗОТА
Молекулярный азот — химически инертное вещество (см.выше строение азота), поэтому легко реагирует только с металлами:
$N_2 + 6Lixrightarrow[]{t_textrm{комн.}}2Li_3N$
Магний горит с образованием не только оксида, но и нитрида магния:
$3N_2 + 6Mg xrightarrow{}2Mg_3N_2$
$N_2 + 2Al xrightarrow{t} 2AlN$
Азот при взаимодействии с металлами проявляет окислительные свойства: образуются нитриды металлов, в которых степень окисления азота равна -3.
С неметаллами азот реагирует тяжелее: для инициирования и ускорения реакций необходимо применять высокие температуры, искровые электрические разряды, ионизирующее излучение, катализаторы (Fe, Cr, V, Ti и их соединения):
$N_2 + 3H_2 xrightarrow{textrm{ t; кат; Р}}2NH_3$
$3F_2 + N_2 xrightarrow{textrm{эл. разряд}} 2NF_3$
$Cl_2 + N_2 ne$
$S$ + $N_2$ $ne$
Реакция горения азота идет при высокой температуре, в электрическом разряде или в присутствии катализатора:
$N_2 + O_2 = 2NO -Q$
Обратите внимание: реакция эндотермическая!
Азот не реагирует со сложными веществами.
Химические свойства азота
Химический элемент азот образует только одно простое вещество. Данное вещество является газообразным и образовано двухатомными молекулами, т.е. имеет формулу N2. Не смотря то, что химический элемент азот имеет высокую электроотрицательность, молекулярный азот N2 является крайне инертным веществом. Обусловлен данный факт тем, что в молекуле азота имеет место крайне прочная тройная связь (N≡N). По этой причине практически все реакции с азотом протекают только при повышенных температурах.
Взаимодействие азота с металлами
Единственное вещество, которое реагирует с азотом в обычных условиях – литий:
Интересным является тот факт, что с остальными активными металлами, т.е. щелочными и щелочноземельными, азот реагирует только при нагревании:
Взаимодействие азота с металлами средней и низкой активности (кроме Pt и Au) также возможно, однако требует несравнимо более высоких температур.
Нитриды активных металлов легко гидролизуются водой:
А также растворами кислот, например:
Взаимодействие азота с неметаллами
Азот реагирует с водородом при нагревании в присутствии катализаторов. Реакция является обратимой, поэтому для повышения выхода аммиака в промышленности процесс ведут при высоком давлении:
Как восстановитель азот реагирует со фтором и кислородом. Со фтором реакция идет при действии электрического разряда:
С кислородом реакция идет под действием электрического разряда или при температуре более 2000 оС и является обратимой:
Из неметаллов азот не реагирует с галогенами и серой.
Взаимодействие азота со сложными веществами
В рамках школьного курса ЕГЭ можно считать, что азот не реагирует ни с какими сложными веществами кроме гидридов активных металлов:
Химические свойства фосфора
Существует несколько аллотропных модификаций фосфора., в частности белый фосфор, красный фосфор и черный фосфор.
Белый фосфор образован четырехатомными молекулами P4, не является устойчивой модификацией фосфора. Ядовит. При комнатной температуре мягкий и подобно воску легко режется ножом. На воздухе медленно окисляется, и из-за особенностей механизма такого окисления светится в темноте (явление хемилюминесценции). Даже при слабом нагревании возможно самопроизвольное воспламенение белого фосфора.
Из всех аллотропных модификаций белый фосфор наиболее активен.
Красный фосфор состоит из длинных молекул переменного состава Pn. В некоторых источниках указывается то, что он имеет атомное строение, но корректнее все-таки считать его строение молекулярным. Вследствие особенностей строения является менее активным веществом по сравнению с белым фосфором, в частности в отличие от белого фосфора на воздухе окисляется значительно медленнее и для его воспламенения требуется поджиг.
Черный фосфор состоит из непрерывных цепей Pn и имеет слоистую структуру схожую со структурой графита, из-за чего и внешне похож на него. Данная аллотропная модификация имеет атомное строение. Самый устойчивый из всех аллотропных модификаций фосфора, наиболее химически пассивен. По этой причине, рассмотренные ниже химические свойства фосфора следует относить прежде всего к белому и красному фосфору.
Взаимодействие фосфора с неметаллами
Реакционная способность фосфора является более высокой, чем у азота. Так, фосфор способен гореть после поджига при обычных условиях, образуя кислотный оксид Р2O5:
а при недостатке кислорода оксид фосфора (III):
Реакция с галогенами также протекает интенсивно. Так, при хлорировании и бромировании фосфора в зависимости от пропорций реагентов образуются тригалогениды или пентагалогениды фосфора:
Ввиду существенно более слабых окислительных свойства йода по сравнению с остальными галогенами, возможно окисление фосфора йодом только до степени окисления +3:
В отличие от азота фосфор с водородом не реагирует.
Взаимодействие фосфора с металлами
Фосфор реагирует при нагревании с активными металлами и металлами средней активности образуя фосфиды:
Фосфиды активных металлов подобно нитридам гидролизуются водой:
А также водными растворами кислот-неокислителей:
Взаимодействие фосфора со сложными веществами
Фосфор окисляется кислотами окислителями, в частности, концентрированными азотной и серной кислотами:
Следует знать, что белый фосфор реагирует с водными растворами щелочей. Однако, ввиду специфичности умение записывать уравнения таких взаимодействий на ЕГЭ по химии пока еще не требовалось.
Тем не менее, тем, кто претендует на 100 баллов, для собственного спокойствия, можно запомнить следующие особенности взаимодействия фосфора с растворами щелочей на холоду и при нагревании.
На холоду взаимодействие белого фосфора с растворами щелочей протекает медленно. Реакция сопровождается образованием газа с запахом тухлой рыбы — фосфина и соединения с редкой степенью окисления фосфора +1:
При взаимодействии белого фосфора с концентрированным раствором щелочи при кипячении выделяется водород и образуется фосфит:
Азот — неметаллический элемент Va группы периодической таблицы Д.И. Менделеева. Составляет 78% воздуха. Входит в состав
белков, являющихся важной частью живых организмов.
Температура кипения азота составляет -195,8 °C. Однако быстрого замораживания объектов, которое часто демонстрируют в
кинофильмах, не происходит. Даже для заморозки растения нужно продолжительное время, это связано с низкой теплоемкостью
азота.
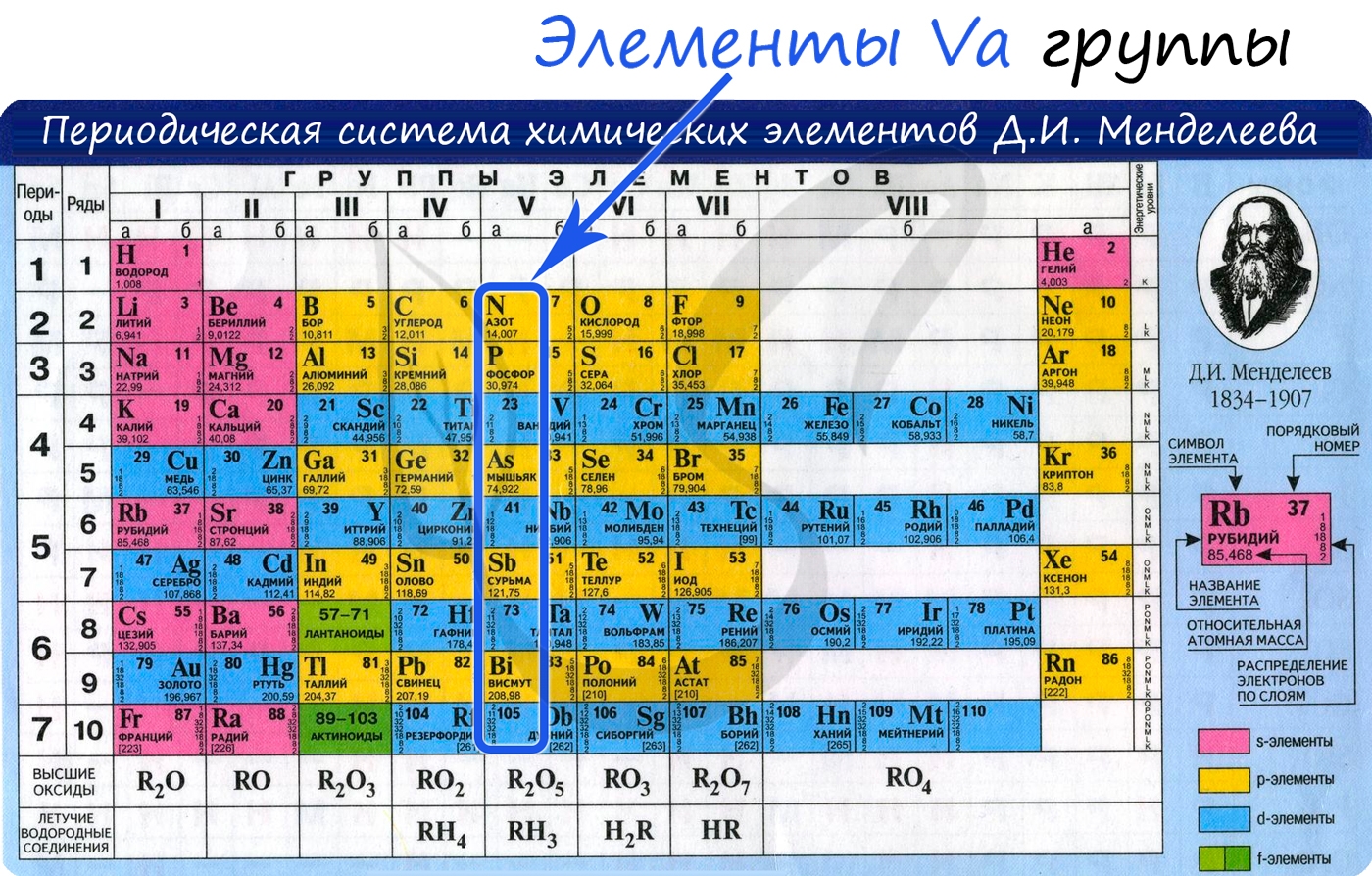
Общая характеристика элементов Va группы
От N к Bi (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств.
Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Азот, фосфор и мышьяк являются неметаллами, сурьма — полуметалл, висмут — металл.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns2np3:
- N — 2s22p3
- P — 3s23p3
- As — 4s24p3
- Sb — 5s25p3
- Bi — 6s26p3
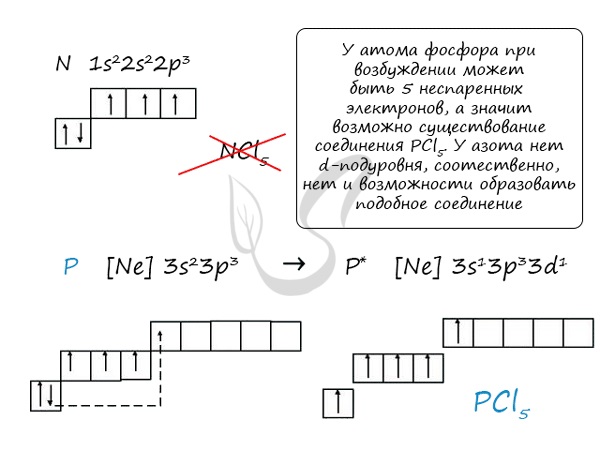
Основное и возбужденное состояние азота
При возбуждении атома азота электроны на s-подуровне распариваются и переходят на p-подуровень. Поскольку азот находится во втором периоде, то
3ий уровень у него отсутствует, что проявляется в особенностях электронной конфигурации возбужденного состояния.
Сравнивая возможности перемещения электронов у азота и фосфора, разница становится очевидна.
Природные соединения
В природе азот встречается в виде следующих соединений:
- Воздух — во вдыхаемом нами воздухе содержится 78% азота
- Азот входит в состав нуклеиновых кислот, белков
- KNO3 — индийская селитра, калиевая селитра
- NaNO3 — чилийская селитра, натриевая селитра
- NH4NO3 — аммиачная селитра (искусственный продукт, в природе не встречается)
Селитры являются распространенными азотными удобрениями, которые обеспечивают быстрый рост и развитие растений, повышают урожайность. Однако,
следует строго соблюдать правила их применения, чтобы не превысить допустимые концентрации.

Получение
В промышленности азот получают путем сжижения воздуха. В дальнейшем путем испарения их сжиженного воздуха получают азот.
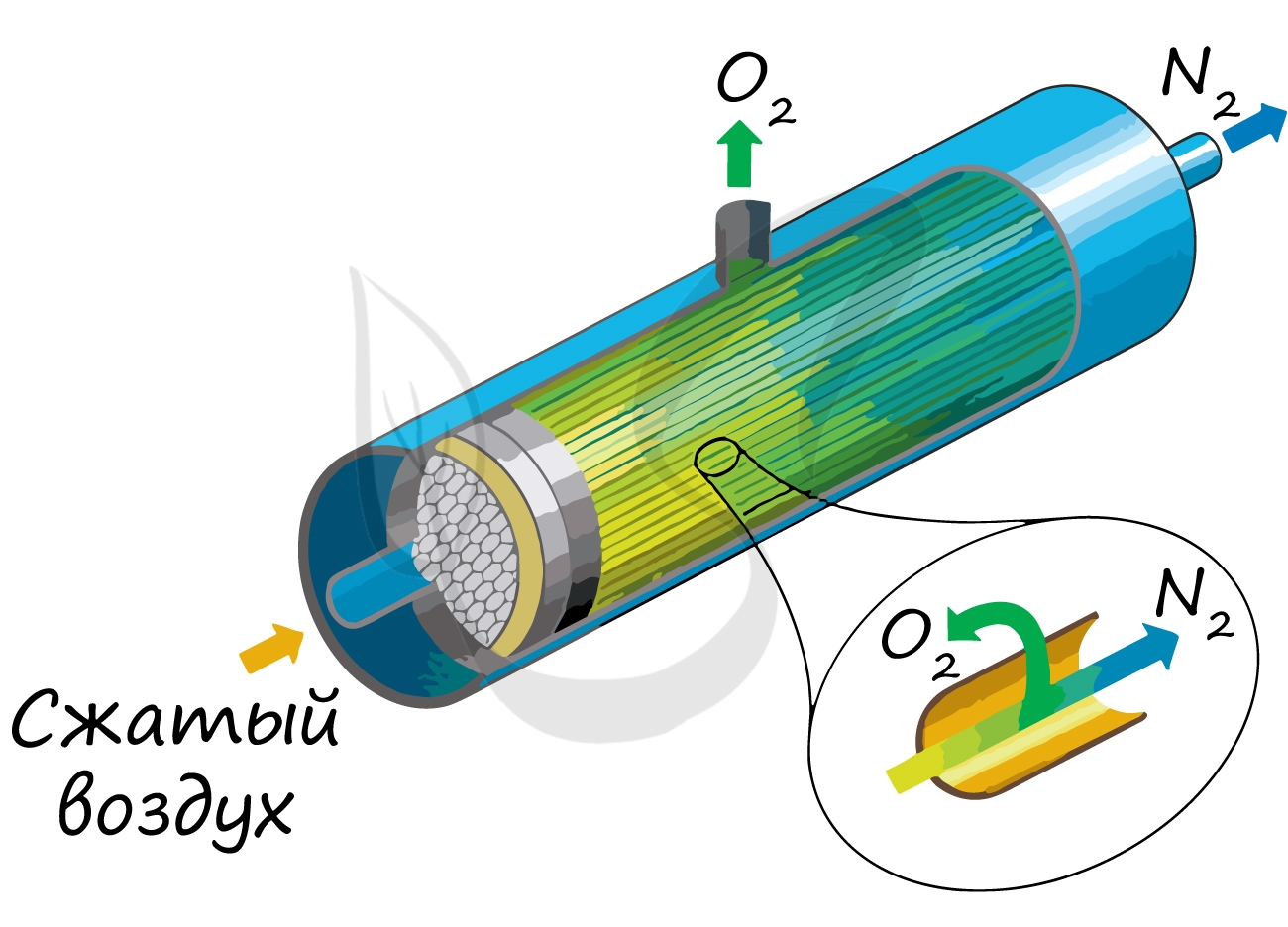
Применяют и метод мембранного разделения, при котором через специальный фильтр из сжатого воздуха удаляют кислород.
В лаборатории методы не столь экзотичны. Чаще всего получают азот разложением нитрита аммония
NH4NO2 → (t) N2 + H2O
Также азот можно получить путем восстановления азотной кислоты активными металлами.
HNO3(разб.) + Zn → Zn(NO3)2 + N2 + H2O

Химические свойства
Азот восхищает — он принимает все возможные для себя степени окисления от -3 до +5.

Молекула азота отличается большой прочностью из-за наличия тройной связи. Вследствие этого многие реакции эндотермичны: даже горение
азота в кислороде сопровождается поглощением тепла, а не выделением, как обычно бывает при горении.

- Реакция с металлами
- Реакция с неметаллами
Без нагревания азот взаимодействует только с литием. При нагревании реагирует и с другими металлами.
N2 + Li → Li3N (нитрид лития)
N2 + Mg → (t) Mg3N2
N2 + Al → (t) AlN
Важное практическое значение имеет синтез аммиака, который применяется в дальнейшим при изготовлении удобрений, красителей, лекарств.
N2 + H2 ⇄ (t, p) NH3
Аммиак
Бесцветный газ с резким едким запахом, раздражающим слизистые оболочки. Раствор концентрацией 10% аммиака применяется в медицинских целях,
называется нашатырным спиртом.
Получение
В промышленности аммиак получают прямым взаимодействием азота и водорода.
N2 + H2 ⇄ (t, p) NH3
В лабораторных условиях сильными щелочами действуют на соли аммония.
NH4Cl + NaOH → NH3 + NaCl + H2O
Химические свойства
Аммиак проявляет основные свойства, окрашивает лакмусовую бумажку в синий цвет.
- Реакция с водой
- Основные свойства
- Восстановительные свойства
Образует нестойкое соединение — гидроксид аммония, слабое основание. Оно сразу же распадается на воду и аммиак.
NH3 + H2O ⇄ NH4OH
Как основание аммиак способен реагировать с кислотами с образованием солей.
NH3 + HCl → NH4Cl (хлорид аммония)
NH3 + HNO3 → NH4NO3 (нитрат аммония)

Поскольку азот в аммиаке находится в минимальной степени окисления -3 и способен только ее повышать, то аммиак проявляет выраженные
восстановительные свойства. Его используют для восстановления металлов из их оксидов.
NH3 + FeO → N2↑ + Fe + H2O
NH3 + CuO → N2↑ + Cu + H2O
Горение аммиака без катализатора приводит к образованию азота в молекулярном виде. Окисление в присутствии катализатора сопровождается
выделением NO.
NH3 + O2 → (t) N2 + H2O
NH3 + O2 → (t, кат) NO + H2O

Соли аммония
Получение
NH3 + H2SO4 → NH4HSO4 (гидросульфат аммония, избыток кислоты)
3NH3 + H3PO4 → (NH4)3PO4
Химические свойства
Помните, что по правилам общей химии, если по итогам реакции выпадает осадок, выделяется газ или образуется вода — реакция идет.
- Реакции с кислотами
- Реакции с щелочами
- Реакции с солями
- Реакция гидролиза
- Реакции разложения
NH4Cl + H2SO4 → (NH4)2SO4 + HCl↑
В реакциях с щелочами образуется гидроксид аммония — NH4OH. Нестойкое основание, которое легко распадается на воду и аммиак.
NH4Cl + KOH → KCl + NH3 + H2O
(NH4)2SO4 + BaCl2 = BaSO4↓ + NH4Cl
В воде ион аммония подвергается гидролизу с образованием нестойкого гидроксида аммония.
NH4+ + H2O ⇄ NH4OH + H+
NH4OH ⇄ NH3 + H2O
NH4Cl → (t) NH3↑ + HCl↑
(NH4)2CO3 → (t) NH3↑ + H2O + CO2↑
NH4NO2 → (t) N2↑ + H2O
NH4NO3 → (t) N2O↑ + H2O
(NH4)3PO4 → (t) NH3↑ + H3PO4

Оксид азота I — N2O
Закись азота, веселящий газ — N2O — обладает опьяняющим эффектом. Несолеобразующий оксид. При н.у. является бесцветным газом с приятным
сладковатым запахом и привкусом. В медицине применяется в больших концентрациях для ингаляционного наркоза.

Получают N2O разложением нитрата аммония при нагревании:
NH4NO3 → N2O + H2O
Оксид азота I разлагается на азот и кислород:
N2O → (t) N2 + O2
Оксид азота II — NO
Окись азота — NO. Несолеобразующий оксид. При н.у. бесцветный газ, на воздухе быстро окисляется до оксида азота IV.
Получение
В промышленных масштабах оксид азота II получают при каталитическом окислении аммиака.
NH3 + O2 → (t, кат) NO + H2O
В лабораторных условиях — в ходе реакции малоактивных металлов с разбавленной азотной кислотой.
Cu + HNO3(разб.) → Cu(NO3)2 + NO + H2O
Химические свойства
На воздухе быстро окисляется с образованием бурого газа — оксида азота IV — NO2.
NO + O2 → NO2

Оксид азота III — N2O3
При н.у. жидкость синего цвета, в газообразной форме бесцветен. Высокотоксичный, приводит к тяжелым ожогам кожи.

Получение
Получают N2O3 в две стадии: сначала реакцией оксида мышьяка III с азотной кислотой, затем
охлаждением полученной смеси газов до температуры — 36 °C.
As2O3 + HNO3 → H3AsO 3 + NO↑ + NO2↑
При охлаждении газов образуется оксид азота III.
NO + NO2 → N2O3
Химические свойства
Является кислотным оксидом. соответствует азотистой кислота — HNO2, соли которой называются нитриты (NO2-).
Реагирует с водой, основаниями.
H2O + N2O3 → HNO2
NaOH + N2O3 → NaNO2 + H2O
Оксид азота IV — NO2
Бурый газ, имеет острый запах. Ядовит.

Получение
В лабораторных условиях данный оксид получают в ходе реакции меди с концентрированной азотной кислотой. Также NO2 выделяется при
разложении нитратов.
Cu + HNO3(конц) → Cu(NO3)2 + NO2 + H2O

Cu(NO3)2 → (t) CuO + NO2 + O2
Pb(NO3)2 → (t) PbO + NO2 + O2
Химические свойства
Проявляет высокую химическую активность, кислотный оксид.
- Окислительные свойства
- Реакции с водой и щелочами
Как окислитель NO2 ведет себя в реакциях с фосфором, углеродом и серой, которые сгорают в нем.
NO2 + C → CO2 + N2
NO2 + P → P2O5 + N2
Окисляет SO2 в SO3 — на этой реакции основана одна из стадий получения серной кислоты.
SO2 + NO2 → SO3 + NO
Оксид азота IV соответствует сразу двум кислотам — азотистой HNO2 и азотной HNO3. Реакции с
водой и щелочами протекают по одной схеме.
NO2 + H2O → HNO3 + HNO2
NO2 + LiOH → LiNO3 + LiNO2 + H2O
Если растворение в воде оксида проводить в избытке кислорода, образуется азотная кислота.
NO2 + H2O + O2 → HNO3

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
