Какие физические свойства углекислого газа

Оксид
углерода (IV) СO2 – углекислый газ
Физические свойства:
Углекислый газ, бесцветный, без запаха, растворимость в воде — в 1V H2O
растворяется 0,9V CO2 (при нормальных условиях); тяжелее воздуха;
t°пл.= -78,5°C (твёрдый CO2 называется «сухой лёд»); не
поддерживает горение.
Строение молекулы:
Углекислый газ имеет
следующие электронную и структурную формулы —
O=C=O |
Все четыре связи
ковалентые полярные.
Получение:
1.
Термическим разложением солей угольной кислоты (карбонатов). Обжиг известняка –
в промышленности:
CaCO3 t=1200˚C→ CaO + CO2
2.
Действием сильных кислот на карбонаты и гидрокарбонаты –
в лаборатории:
CaCO3 (мрамор) + 2HCl →
CaCl2 + H2O + CO2
NaHCO3
+ HCl
→
NaCl
+ H2O + CO2
Способы собирания
вытеснением воздуха |
3. Сгорание
углеродсодержащих веществ:
СН4 + 2О2→ 2H2O + CO2
4. При медленном
окислении в биохимических процессах (дыхание, гниение, брожение)
Химические свойства:
Видео «Химические свойства углекислого газа»
Кислотный оксид:
1)
с водой даёт непрочную угольную кислоту:
СО2 + Н2О
↔ Н2СО3
2)
реагирует с основными оксидами и основаниями, образуя соли угольной
кислоты
Na2O + CO2→ Na2CO3
2NaOH + CO2→ Na2CO3 + H2O
NaOH + CO2(избыток) → NaHCO3
3)
При повышенной температуре может проявлять окислительные свойства – окисляет
металлы — СO2
+ Me = MexOy
+ C
С+4O2
+ 2Mg t˚C→ 2Mg+2O
+ C0
Видео «Горение магния в углекислом газе»
Качественная
реакция на углекислый газ:
Помутнение известковой
воды Ca(OH)2 за счёт образования
белого осадка – нерастворимой соли CaCO3:
Ca(OH)2 + CO2 →
CaCO3
↓+ H2O
Применение углекислого
газа:

Видео «Тушение пламени углекислым газом»
Угольная
кислота и её соли
Химическая
формула — H2CO3
Структурная формула
– все связи ковалентные полярные:
Кислота слабая, существует
только в водном растворе, очень непрочная, разлагается на углекислый газ и воду:
CO2
+ H2O ↔ H2CO3
Опыт «Разложение угольной кислоты»
Опыт «Получение»
Опыт «Получение угольной кислоты»
Химические свойства:
Для угольной кислоты характерны
все свойства кислот.
1) Диссоциация – двухосновная
кислота, диссоциирует слабо в две ступени, индикатор — лакмус краснеет в водном
растворе:
H2CO3
↔ H+
+ HCO3-(гидрокарбонат-ион)
HCO3-
↔ H+
+ CO32- (карбонат-ион)
2) с активными металлами
H2CO3
+ Ca
= CaCO3
+ H2↑
3) с основными оксидами
H2CO3
+ CaO
= CaCO3
+ H2O
4) с основаниями
H2CO3(изб) + NaOH = NaHCO3 + H2O
H2CO3
+ 2NaOH = Na2CO3 + 2H2O
5) Очень непрочная
кислота – разлагается
Соли
угольной кислоты – карбонаты и гидрокарбонаты
Угольная кислота
образует два ряда солей:
·
Средние соли — карбонаты Na2СO3,
(NH4)2CO3
·
Кислые соли — бикарбонаты,
гидрокарбонаты NaHCO3
, Ca(HCO3)2
В природе встречаются:
CaCO3
мел

мрамор

известняк

NaHCO3 – питьевая сода


K2CO3(поташ,
в золе растений)
Na2CO3
– сода, кальцинированная сода
Na2CO3 x 10H2O – кристаллическая сода
Физические свойства:
Все карбонаты – твёрдые
кристаллические вещества. Большинство из них в воде не растворяются.
Гидрокарбонаты растворяются в воде.
Химические свойства
солей угольной кислоты:
Общие
свойства солей:
1) Вступают в реакции
обмена с другими растворимыми солями
Na2CO3
+ CaCl2
= CaCO3↓
+ 2NaCl
2) Разложение
гидрокарбонатов при нагревании
NaHCO3t˚C→Na2CO3
+ H2O + CO2↑
3) Разложение
нерастворимых карбонатов при нагревании
CaCO3t˚C→ CaO+ CO2↑
4) Карбонаты и гидрокарбонаты
могут превращаться друг в друга:
Опыт «Взаимопревращение карбонатов и гидрокарбонатов»
гидрокарбонатывкарбонаты
Me(HCO3)n + Me(OH)n →
MeCO3+H2O
Me(HCO3)nt˚C → MeCO3↓+H2O+CO2↑
карбонатывгидрокарбонаты
MeCO3+H2O+CO2= Me(HCO3)n
Специфические свойства:
1) Качественная реакция на CO32- карбонат – ион
«вскипание»
при действии сильной кислоты:
Na2CO3 + 2HCl =
2NaCl
+ H2O + CO2↑
ЗАДАНИЯ ДЛЯ ЗАКРЕПЛЕНИЯ
№ 1. Закончите уравнения осуществимых химических реакций:
CO 2+ KOH =
CO + Al =
H2CO3+ K2SO4 =
CO2( изб ) + NaOH =
С O2+ Na2O =
CaCO3+ CO2 + H2O =
CO2+ Ca(OH)2 =
CO + CaO =
CO2+ H2SO4 =
Ca(HCO3)2+ Ca(OH)2=
H2CO3+ NaCl =
C + ZnO =
№2.
Осуществите превращения по схеме:
1) Al 4 C 3→ CH 4→ CO 2→ CaCO 3→ Ca ( HCO 3)2→ CaCO 3
2) Ca → CaC 2→ Ca ( OH )2→ CaCO 3→ CO 2→ C
3) CO2 → H2CO3 → Na2CO3 → CO2
4) CaCO3 → CO2 → NaHCO3 → Na2CO3
№3. Решите задачи
1.Какой объём углекислого газа выделится при обжиге карбоната кальция массой 200 г
2. Сколько угольной кислоты можно получить при взаимодействии 2 л
углекислого газа (н.у.) с водой, если выход кислоты составил 90% по
сравнению с теоретическим
Газировка, вулкан, Венера, рефрижератор – что между ними общего? Углекислый газ. Мы собрали для Вас самую интересную информацию об одном из самых важных химических соединений на Земле.
Что такое диоксид углерода
Диоксид углерода известен в основном в своем газообразном состоянии, т.е. в качестве углекислого газа с простой химической формулой CO2. В таком виде он существует в нормальных условиях – при атмосферном давлении и «обычных» температурах. Но при повышенном давлении, свыше 5 850 кПа (таково, например, давление на морской глубине около 600 м), этот газ превращается в жидкость. А при сильном охлаждении (минус 78,5°С) он кристаллизуется и становится так называемым сухим льдом, который широко используется в торговле для хранения замороженных продуктов в рефрижераторах.
Жидкая углекислота и сухой лед получаются и применяются в человеческой деятельности, но эти формы неустойчивы и легко распадаются.
А вот газообразный диоксид углерода распространен повсюду: он выделяется в процессе дыхания животных и растений и является важной составляющей частью химического состава атмосферы и океана.
Свойства углекислого газа
Углекислый газ CO2 не имеет цвета и запаха. В обычных условиях он не имеет и вкуса. Однако при вдыхании высоких концентраций диоксида углерода можно почувствовать во рту кисловатый привкус, вызванный тем, что углекислый газ растворяется на слизистых и в слюне, образуя слабый раствор угольной кислоты.
Кстати, именно способность диоксида углерода растворяться в воде используется для изготовления газированных вод. Пузырьки лимонада – тот самый углекислый газ. Первый аппарат для насыщения воды CO2 был изобретен еще в 1770 г., а уже в 1783 г. предприимчивый швейцарец Якоб Швепп начал промышленное производство газировки (торговая марка Schweppes существует до сих пор).
Углекислый газ тяжелее воздуха в 1,5 раза, поэтому имеет тенденцию «оседать» в его нижних слоях, если помещение плохо вентилируется. Известен эффект «собачьей пещеры», где CO2 выделяется прямо из земли и накапливается на высоте около полуметра. Взрослый человек, попадая в такую пещеру, на высоте своего роста не ощущает избытка углекислого газа, а вот собаки оказываются прямо в густом слое диоксида углерода и подвергаются отравлению.
CO2 не поддерживает горение, поэтому его используют в огнетушителях и системах пожаротушения. Фокус с тушением горящей свечки содержимым якобы пустого стакана (а на самом деле — углекислым газом) основан именно на этом свойстве диоксида углерода.
Углекислый газ в природе: естественные источники
Углекислый газ в природе образуется из различных источников:
- Дыхание животных и растений.
Каждому школьнику известно, что растения поглощают углекислый газ CO2 из воздуха и используют его в процессах фотосинтеза. Некоторые хозяйки пытаются обилием комнатных растений искупить недостатки приточной вентиляции. Однако растения не только поглощают, но и выделяют углекислый газ в отсутствие света – это часть процесса дыхания. Поэтому джунгли в плохо проветриваемой спальне – не очень хорошая идея: ночью уровень CO2 будет расти еще больше. - Вулканическая деятельность.
Диоксид углерода входит в состав вулканических газов. В местностях с высокой вулканической активностью CO2 может выделяться прямо из земли – из трещин и разломов, называемых мофетами. Концентрация углекислого газа в долинах с мофетами столь высока, что многие мелкие животные, попав туда, умирают. - Разложение органических веществ.
Углекислый газ образуется при горении и гниении органики. Объемные природные выбросы диоксида углерода сопутствуют лесным пожарам.
Углекислый газ «хранится» в природе в виде углеродных соединений в полезных ископаемых: угле, нефти, торфе, известняке. Гигантские запасы CO2 содержатся в растворенном виде в мировом океане.
Выброс углекислого газа из открытого водоема может привести к лимнологической катастрофе, как это случалось, например, в 1984 и 1986 гг. в озерах Манун и Ньос в Камеруне. Оба озера образовались на месте вулканических кратеров – ныне они потухли, однако в глубине вулканическая магма все еще выделяет углекислый газ, который поднимается к водам озер и растворяется в них. В результате ряда климатических и геологических процессов концентрация углекислоты в водах превысила критическое значение. В атмосферу было выброшено огромное количество углекислого газа, который наподобие лавины спустился по горным склонам. Жертвами лимнологических катастроф на камерунских озерах стали около 1 800 человек.
Искусственные источники углекислого газа
Основными антропогенными источниками диоксида углерода являются:
- промышленные выбросы, связанные с процессами сгорания;
- автомобильный транспорт.
Несмотря на то, что доля экологичного транспорта в мире растет, подавляющая часть населения планеты еще не скоро будет иметь возможность (или желание) перейти на новые автомобили.
Активное сведение лесов в промышленных целях также ведет к повышению концентрации углекислого газа СО2 в воздухе.
Углекислый газ в организме человека
CO2 – один из конечных продуктов метаболизма (расщепления глюкозы и жиров). Он выделяется в тканях и переносится при помощи гемоглобина к легким, через которые выдыхается. В выдыхаемом человеком воздухе около 4,5% диоксида углерода (45 000 ppm) – в 60-110 раз больше, чем во вдыхаемом.
Углекислый газ играет большую роль в регуляции кровоснабжения и дыхания. Повышение уровня CO2 в крови приводит к тому, что капилляры расширяются, пропуская большее количество крови, которое доставляет к тканям кислород и выводит углекислоту.
Дыхательная система тоже стимулируется повышением содержания углекислого газа, а не нехваткой кислорода, как может показаться. В действительности нехватка кислорода долго не ощущается организмом и вполне возможна ситуация, когда в разреженном воздухе человек потеряет сознание раньше, чем почувствует нехватку воздуха. Стимулирующее свойство CO2 используется в аппаратах искусственного дыхания: там углекислый газ подмешивается к кислороду, чтобы «запустить» дыхательную систему.
Углекислый газ и мы: чем опасен СO2
Углекислый газ необходим человеческому организму так же, как кислород. Но так же, как с кислородом, переизбыток углекислого газа вредит нашему самочувствию.
Большая концентрация CO2 в воздухе приводит к интоксикации организма и вызывает состояние гиперкапнии. При гиперкапнии человек испытывает трудности с дыханием, тошноту, головную боль и может даже потерять сознание. Если содержание углекислого газа не снижается, то далее наступает черед гипоксии – кислородного голодания. Дело в том, что и углекислый газ, и кислород перемещаются по организму на одном и том же «транспорте» – гемоглобине. В норме они «путешествуют» вместе, прикрепляясь к разным местам молекулы гемоглобина. Однако повышенная концентрация углекислого газа в крови понижает способность кислорода связываться с гемоглобином. Количество кислорода в крови уменьшается и наступает гипоксия.
Такие нездоровые для организма последствия наступают при вдыхании воздуха с содержанием CO2 больше 5 000 ppm (таким может быть воздух в шахтах, например). Справедливости ради, в обычной жизни мы практически не сталкиваемся с таким воздухом. Однако и намного меньшая концентрация диоксида углерода отражается на здоровье не лучшим образом.
Согласно выводам некоторых исследований, уже 1 000 ppm CO2 вызывает у половины испытуемых утомление и головную боль. Духоту и дискомфорт многие люди начинают ощущать еще раньше. При дальнейшем повышении концентрации углекислого газа до 1 500 – 2 500 ppm критически снижается работоспособность, мозг «ленится» проявлять инициативу, обрабатывать информацию и принимать решения.
И если уровень 5 000 ppm почти невозможен в повседневной жизни, то 1 000 и даже 2 500 ppm легко могут быть частью реальности современного человека. Наш эксперимент в школе показал, что в редко проветриваемых школьных классах уровень CO2 значительную часть времени держится на отметке выше 1 500 ppm, а иногда подскакивает выше 2 000 ppm. Есть все основания предполагать, что во многих офисах и даже квартирах ситуация похожая.
Безопасным для самочувствия человека уровнем углекислого газа физиологи считают 800 ppm.
Еще одно исследование обнаружило связь между уровнем CO2 и окислительным стрессом: чем выше уровень диоксида углерода, тем больше мы страдаем от окислительного стресса, который разрушает клетки нашего организма.
Углекислый газ в атмосфере Земли
В атмосфере нашей планеты всего около 0,04% CO2 (это приблизительно 400 ppm), а совсем недавно было и того меньше: отметку в 400 ppm углекислый газ перешагнул только осенью 2016 года. Ученые связывают рост уровня CO2 в атмосфере с индустриализацией: в середине XVIII века, накануне промышленного переворота, он составлял всего около 270 ppm.
Несмотря на такое ничтожное процентное содержание диоксида углерода в атмосфере, он оказывает огромное влияние на климат планеты. Углекислый газ – один из парниковых газов. Он поглощает и удерживает инфракрасное излучение с поверхности Земли, что в конечном итоге способствует повышению температуры на планете. Этот процесс называется парниковым эффектом. Без парникового эффекта температура на земном шаре была бы примерно на 30°С ниже.
Атмосфера Венеры на 96,5% состоит из углекислого газа, и, по-видимому, тоже подвержена парниковому эффекту. Из-за него Венера является самой жаркой планетой Солнечной системы, она горячее даже ближайшего к Солнцу Меркурия. Температура на Венере около 464°С – этого хватит, чтобы расплавить свинец и олово.
Рост уровня СО2 в атмосфере Земли ведет к усилению парникового эффекта, а тот, в свою очередь – к необратимым изменениям климата. Уже сейчас можно наблюдать таяние ледников. Например, знаменитая снежная шапка Килиманджаро уменьшилась за последние 100 лет на 80%.
Что и говорить, без углекислого газа наш мир был бы совершенно другим. Он участвует в важнейших химических, биологических, климатических и геологических процессах на Земле. И чем больше мы о них знаем, тем проще нам принимать важные решения: выбирать образ жизни и создавать свою среду – свой здоровый и комфортный микроклимат.
Summary
Article Name
Что такое CO2
Description
Углекислый газ. Мы собрали для Вас самую интересную информацию об одном из самых важных химических соединений на Земле.
Author
Марина Гесс
Publisher Name
Tion.ru
Publisher Logo
Подпишись на наш Instagram и будь в курсе
самых интересных новостей и акций!
Углекислый газ, свойства, получение и применение.
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Углекислый газ – бинарное химическое соединение углерода и кислорода, имеющее формулу CO2.
Углекислый газ, формула, молекула, строение, состав, вещество
Физические свойства углекислого газа. Сухой лёд
Получение углекислого газа
Химические свойства углекислого газа. Химические реакции (уравнения) углекислого газа
Применение углекислого газа
Углекислый газ, формула, молекула, строение, состав, вещество:
Углекислый газ (диоксид углерода, двуокись углерода, углекислота, оксид углерода (IV), угольный ангидрид) – бесцветный газ, почти без запаха (в больших концентрациях с кисловатым «содовым» запахом).
Углекислый газ – бинарное химическое соединение углерода и кислорода, имеющее формулу CO2.
Химическая формула углекислого газа CO2.
Строение молекулы углекислого газа, структурная формула углекислого газа:
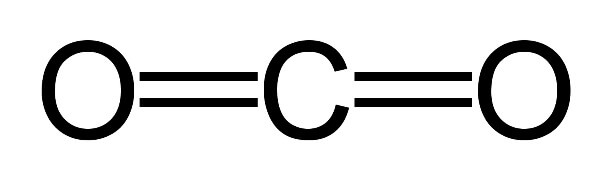
Углекислый газ тяжелее воздуха приблизительно в 1,5 раза. Его плотность при нормальных условиях составляет 1,98 кг/м3, по отношении к воздуху – 1,524. Поэтому скапливается в низких непроветриваемых местах.
Концентрация углекислого газа в воздухе (в атмосфере Земли) составляет в среднем 0,046 % (по массе) и 0,0314 % (по объему).
Углекислый газ вырабатывается в органах и тканях человека образуется в качестве одного из конечных продуктов метаболизма. Он переносится от тканей по венозной системе и затем выделяется с выдыхаемым воздухом через лёгкие. Таким образом, содержание углекислого газа в крови велико в венозной системе, уменьшается в капиллярной сети лёгких, и содержание его мало в артериальной крови. В выдыхаемом человеком воздухе содержится около 4,5% диоксида углерода, что в 60-110 раз больше, чем во вдыхаемом. Организм человека выделяет приблизительно 1 кг углекислого газа в сутки.
Углекислый газ растворяется в воде. В 100 граммах воды растворяется 0,3803 грамма CO2 при 16 °C, 0,3369 грамма CO2 – при 20 °C, 0,2515 грамма CO2 – при 30 °C. Растворяясь в воде, образует угольную кислоту Н2CO3. Растворим также в ацетоне, бензоле, метаноле и этаноле.
Термически устойчив при температурах менее 1000 °C. При температуре 1000 °C восстанавливается углем до оксида углерода (II).
При нормальном атмосферном давлении диоксид углерода не существует в жидком состоянии, существует только в твердом или газообразном состоянии. Твердая двуокись углерода при повышении температуры не плавится, а переходит (возгоняется) непосредственно из твёрдого состояния в газообразное. Твёрдую двуокись углерода также называют сухим льдом. Внешний вид сухого льда напоминает обычный лед, снегоподобную массу. При сублимации сухой лед поглощает около 590 кДж/кг (140 ккал/кг) теплоты.
Под давлением 35 000 атм. твердая углекислота становится проводником электрического тока.
Жидкий углекислый газ можно получить при повышении давления. Так, при температуре 20 °С и давлении свыше 6 МПа (~60 атм.) газ сгущается в бесцветную жидкость. При нормальных условиях (20 °С и 101,3 кПа) при испарении 1 кг жидкой углекислоты образуется 509 л углекислого газа. Хранят и транспортируют углекислый газ, как правило, в жидком состоянии
Двуокись углерода негорюча, но в ее атмосфере может поддерживаться горение активных металлов, например, щелочных металлов и щелочноземельных – магния, кальция, бария.
Двуокись углерода нетоксична, невзрывоопасна.
Предельно допустимая концентрация двуокиси углерода в воздухе рабочей зоны не установлена, при оценке этой концентрации можно ориентироваться на нормативы для угольных и озокеритовых шахт, установленные в пределах 0,5% (об.) или 9,2 г/м (см. ГОСТ 8050-85 «Двуокись углерода газообразная и жидкая. Технические условия»).
По степени воздействия на организм человека двуокись углерода относится к 4-му классу опасности по ГОСТ 12.1.007-76.
При концентрациях более 5% (92 г/м) двуокись углерода оказывает вредное влияние на здоровье человека, так как она тяжелее воздуха в полтора раза и может накапливаться в слабопроветриваемых помещениях у пола и в приямках, а также во внутренних объемах оборудования для получения, хранения и транспортирования газообразной, жидкой и твердой двуокиси углерода. При этом снижается объемная доля кислорода в воздухе, что может вызвать явление кислородной недостаточности и удушья.
Углекислый газ образуется при гниении и горении органических веществ, в результате вулканической деятельности. Содержится в воздухе и минеральных источниках, выделяется при дыхании животных и растений. Искусственными источниками образования углекислого газа являются промышленные выбросы и выхлопные газы автомобильного транспорта.
Углекислый газ легко пропускает излучение в ультрафиолетовой и видимой частях спектра, которое поступает на Землю от Солнца и обогревает её. В то же время он поглощает испускаемое Землёй инфракрасное излучение и является одним из парниковых газов, вследствие чего участвует в процессе глобального потепления.
Физические свойства углекислого газа:
| Наименование параметра: | Значение: |
| Химическая формула | CO2 |
| Синонимы и названия иностранном языке | углерода двуокись (рус.) углерода диоксид (рус.) угольный ангидрид (рус.) оксид углерода (IV) carbon dioxide (англ.) |
| Тип вещества | неорганическое |
| Внешний вид | бесцветный газ |
| Цвет | бесцветный |
| Вкус | кисловатый вкус |
| Запах | почти без запаха (в больших концентрациях с кисловатым «содовым» запахом) |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | газ |
| Плотность (состояние вещества – твердое вещество, при -79 °C и атмосферном давлении 1 атм.), кг/м3 | 1561 |
| Плотность (состояние вещества – твердое вещество, при -79 °C и атмосферном давлении 1 атм.), г/см3 | 1,561 |
| Плотность (состояние вещества – жидкость, при -60 °C и атмосферном давлении 1 атм.), кг/м3 | 1190 |
| Плотность (состояние вещества – жидкость, при -60 °C и атмосферном давлении 1 атм.), г/см3 | 1,19 |
| Плотность (состояние вещества – жидкость, при -37 °C и атмосферном давлении 1 атм.), кг/м3 | 1101 |
| Плотность (состояние вещества – жидкость, при -37 °C и атмосферном давлении 1 атм.), г/см3 | 1,101 |
| Плотность (состояние вещества – жидкость, при 0 °C и атмосферном давлении 35,5 атм.), кг/м3 | 925 |
| Плотность (состояние вещества – жидкость, при 0 °C и атмосферном давлении 35,5 атм.), г/см3 | 0,925 |
| Плотность (состояние вещества – газ, при 0 °C и атмосферном давлении 1 атм.), кг/м3 | 1,9768 |
| Плотность (состояние вещества – газ, при 0 °C и атмосферном давлении 1 атм.), г/см3 | 0,0019768 |
| Температура сублимации (возгонки), °C | -78,5 |
| Критическая температура*, °C | 31 |
| Критическое давление, МПа | 7,387 |
| Критический удельный объём, м3/кг | 0,468 |
| Критическая точка | 31 °C, 7,38 МПа |
| Тройная точка | −56,6 °C, 0,52 МПа |
| Молярная масса, г/моль | 44,01 |
| Растворимость в воде, г/100 г | 0,3803 при 16 °C, 0,3369 при 20 °C, 0,2515 при 30 °C |
| Теплопроводность, Вт/(м·K) | 0,0166 |
| Удельная теплоемкость, Дж/(кг·К) | 849 |
| Удельная теплота испарения, кДж/кг | 379,5 |
| Удельная теплота плавления, кДж/кг | 205 |
| Стандартная энтальпия образования ΔH (при 298 К, для состояния вещества – газ), кДж/моль | -393,51 |
| Стандартная энергия Гиббса образования ΔG (при 298 К, для состояния вещества – газ), кДж/моль | -394,38 |
| Стандартная энтропия вещества S (при 298 К, для состояния вещества – газ) | 213,68 |
| Стандартная мольная теплоемкость Cp (298 К, для состояния вещества – газ), Дж/(моль·K) | 37,11 |
| Энтальпия плавления ΔHпл, кДж/моль | 8,37 |
| Энтальпия возгонки ΔHвозг, кДж/моль | 25,23 |
| Скорость звука в веществе (при 20°C, состояние среды – газ), м/с | 274,6 |
| Давление паров, мм.рт.ст. | 0,000001 (при -186,4°C), 0,00001 (при -180,7°C), 0,0001 (при -174,3°C), 0,001 (при -166,8°C), 0,01 (при -158°C), 2,31 (при -130°C), 9,81 (при -120°C), 34,63 (при -110°C), 104,81 (при -100°C), 279,5 (при -90°C), 672,2 (при -80°C), 1486,1 (при -70°C), 3073,1 (при -60°C), 5127,8 (при -50°C), 7545 (при -40°C), 10718 (при -30°C), 14781 (при -20°C), 19872 (при -10°C), 26142 (при 0°C), 33763 (при 10°C), 42959 (при 20°C), 54086 (при 30°C) |
* при температуре выше критической температуры газ невозможно сконденсировать ни при каком давлении.
Получение углекислого газа:
В промышленности углекислый газ образуется в дымовых газах при сжигании различных органических и неорганических веществ или как побочный продукт химических процессов, например, при разложении природных карбонатов (доломита, известняка). Также углекислый газ как побочный продукт получают на установках разделения воздуха с целью получения чистого кислорода, азота и аргона.
В лабораторных условиях углекислый газ получают, например, в результате следующих химических реакций:
1. взаимодействия карбоната кальция и азотной кислоты:
CaCO3 + 2HNO3 → Ca(NO3)2 + CO2 + H2O,
2. в результате взаимодействия карбоната кальция с другими минеральными кислотами,
3. взаимодействия пищевой соды с лимонной кислотой или с кислым лимонным соком,
4. реакции горения углерода:
С + O2 → CO2.
Химические свойства углекислого газа. Химические реакции (уравнения) углекислого газа:
Диоксид углерода относится к кислотным оксидам, поэтому для него характерны следующие химические реакции:
1. реакция взаимодействия оксида углерода (IV) и водорода:
CO2 + 4H2 → CH4 + 2H2O (t ~ 200 °C, kat = Cu2O).
В результате реакции образуются метан и вода.
2. реакция взаимодействия оксида углерода (IV) и углерода:
CO2 + C ⇄ 2CO (t = 700-1000 °C).
В результате реакции образуется оксид углерода (II). Реакция протекает при взаимодействии углекислого газа с раскаленными углями.
3. реакция взаимодействия оксида углерода (IV) и магния:
CO2 + 2Mg → 2MgO + C (t ~ 500 °C).
В результате реакции образуются оксид магния и углерод.
4. реакция взаимодействия оксида углерода (IV) и гафния:
Hf + CO2 → HfC + HfO2 (t = 800-1000 °C).
В результате реакции образуются карбид гафния и оксид гафния.
5. реакция взаимодействия оксида углерода (IV) и германия:
Ge + CO2 → GeO + CO (t = 700-900 °C).
В результате реакции образуются оксид германия и оксид углерода (II).
6. реакция взаимодействия оксида углерода (IV) и цинка:
Zn + CO2 → ZnO + CO (t = 800-950 °C).
В результате реакции образуются оксид цинка и оксид углерода (II).
7. реакция взаимодействия оксида углерода (IV) и индия:
2In + CO2 → In2O + CO (t ~ 850 °C).
В результате реакции образуются оксид индия и оксид углерода (II).
8. реакция взаимодействия оксида углерода (IV) и циркония:
2Zr + CO2 → ZrC + ZrO2 (t = 800-100 °C).
В результате реакции образуются карбид циркония и оксид циркония.
9. реакция взаимодействия оксида углерода (IV) и вольфрама:
W + 2CO2 → WO2 + 2CO (t ~ 1200 °C).
В результате реакции образуются оксид вольфрама и оксид углерода (II).
10. реакция взаимодействия оксида углерода (IV) и оксида лития:
Li2O + CO2 → Li2CO3.
В результате реакции образуется карбонат лития.
11. реакция взаимодействия оксида углерода (IV) и оксида натрия:
Na2O + CO2 → Na2CO3 (t = 450-550 °C).
В результате реакции образуется карбонат натрия.
12. реакция взаимодействия оксида углерода (IV) и оксида калия:
K2O + CO2 → K2CO3 (t ~ 400 °C).
В результате реакции образуется карбонат калия.
13. реакция взаимодействия оксида углерода (IV) и оксида бария:
BaO + CO2 → BaCO3.
В результате реакции образуется карбонат бария.
14. реакция взаимодействия оксида углерода (IV) и оксида кальция:
CaO + CO2 → CaCO3.
В результате реакции образуется карбонат кальция.
15. реакция взаимодействия карбоната кальция, оксида углерода (IV) и воды:
CaCO3 + CO2 + H2O → Ca(HCO3)2.
В результате реакции образуется гидрокарбонат кальция.
16. реакция взаимодействия оксида углерода (IV) и оксида магния:
MgO + CO2 → MgCO3.
В результате реакции образуется карбонат магния.
17. реакция взаимодействия оксида углерода (IV) и оксида кремния (II):
SiO + CO2 → SiO2 + CO (t ~ 500 °C).
В результате реакции образуются оксид кремния (IV) и оксид углерода (II).
18. реакция взаимодействия оксида углерода (IV) и воды:
CO2 + H2O ⇄ H2CO3.
В результате реакции образуется угольная кислота.
19. реакция взаимодействия оксида углерода (IV) и гидроксида лития:
2LiOH + CO2 → Li2CO3 + H2O.
В результате реакции образуются карбонат лития и вода. В ходе реакции используется концентрированный раствор гидроксида лития.
20. реакция взаимодействия оксида углерода (IV) и гидроксида калия:
KOH + CO2 → KHCO3,
2KOH + CO2 → K2CO3 + H2O.
В первом случае в результате реакции образуются гидрокарбонат калия, во втором случае – карбонат калия и вода. Реакция протекает в первом случае в этаноле и используется разбавленный раствор гидроксида калия, во втором используется концентрированный раствор гидроксида калия.
21. реакция взаимодействия оксида углерода (IV) и гидроксида натрия:
NaOH + CO2 → NaHCO3,
2NaOH + CO2 → Na2CO3 + H2O.
В первом случае в результате реакции образуются гидрокарбонат натрия, во втором – карбонат натрия и вода. В ходе первой реакции используется разбавленный раствор гидроксида натрия, в ходе второй – концентрированный раствор гидроксида натрия.
22. реакция взаимодействия оксида углерода (IV) и гидроксида кальция:
Ca(OH)2 + CO2 → CaCO3 + H2O.
В результате реакции образуются карбонат кальция и вода.
23. реакция взаимодействия оксида углерода (IV) и гидроксида бария:
Ba(OH)2 + CO2 → BaCO3 + H2O.
В результате реакции образуются карбонат бария и вода.
24. реакция взаимодействия оксида углерода (IV) и метана:
CH4 + CO2 → 2CO + 2H2 (t = 800-900 °C, kat = NiO, нанесенный на Al2O3).
В результате реакции образуются оксид углерода (II) и вода.
25. реакция термического разложения оксида углерода (IV):
2CO2 → 2CO + O2 (t > 2000 °C).
В результате реакции образуются оксид углерода (II) и кислород.
26. реакция фотосинтеза:
6CO2 + 6H2O → C6H12O6 + 6O2 (hv, kat = хлорофилл).
В результате реакции образуются глюкоза и кислород.
Применение углекислого газа:
Углекислый газ используется во многих отраслях промышленности и быту:
– как пищевая добавка Е290 в качестве разрыхлителя в пищевом производстве и консерванта в алкогольных и безалкогольных газированных напитках, а также для газирования лимонада, газированной воды и других напитков;
– в системах пожаротушения и в огнетушителях;
– для создания защитной среды при сварке металлов;
– для охлаждения, замораживания и хранения пищевых продуктов при прямом и косвенном контакте с сухим льдом;
– для сушки литейных форм;
– в качестве активной среды углекислотного лазера.
Примечание: © Фото https://www.pexels.com, https://pixabay.com.
карта сайта
Коэффициент востребованности
929
