Какая масса серной кислоты содержится в 10 мл раствора


Весовая процентная концентрация показывает, какой процент от общего веса раствора составляет растворенное вещество.
■ 18. Сколько нитрата калия нужно взять для приготовления 300 г 2% раствора соли?
19? Сколько воды и сахара требуется для приготовления 250 г 10% раствора?
20. Сколько хлорида бария потребуется для приготовления 50 г 0,5% раствора? (См. Ответ)
В лабораторной практике часто приходится иметь дело с кристаллогидратами — солями, содержащими кристаллизационную воду, например CuSО4 ·5H2O, FeSО4 · 7H2О и т. д. В этом случае следует уметь учитывать кристаллизационную воду.
Пример 1. Сколько соли нужно для приготовления 500 г 3% ее раствора? | |
Дано: 500 г. 3% раствора соли | Решение: Если сказано, что имеется 3% раствор, это значит, что в любом количестве этого раствора содержится 3% соли. Чтобы рассчитать, сколько нужно соли для приготовления 500 г такого раствора, следует найти 3% от 500 г: (500 · 3) : 100 = 15г Следовательно, соли нужно 15 г, а воды 500— 15 = 485 г. |
Пример 2. Сколько кристаллогидрата медного купороса нужно взвесить, чтобы получить 200 г 5% раствора сульфата меди? Сколько воды нужно для этого взять? | |
Решение: Сначала требуется определить, сколько сульфата меди CuSО4 нужно для приготовления заданного количества раствора: (200 · 5) :100 = 10 г. CuSO4. Далее делаем пересчет на кристаллогидрат: грамм-молекула CuSO4 весит 160 г, а грамм-молекула CuSO4 · 5H2О весит 250 г. Следовательно, мы можем составить пропорцию: 160 г CuSO4— в 250 г CuSO4 · 5H2О 10» CuSО4 — » х » CuSO4· 5Н2О X=(250 · 10) : 160 = 15,625 г. Воды для приготовления раствора требуется 200— 16,6 15= 184,375 г. | |
■ 21. Сколько кристаллогидрата Na2SO4 · 10H2O понадобится для приготовления 2 кг 34 раствора Na2SО4?
22. Сколько кристаллогидрата железного купороса FeSO4·7H2O потребуется для приготовления 30 кг 0,5% раствора FeSO4?
23. Сколько кристаллогидрата CaCl2 · 6H2O потребуется для приготовления 500 г 10% раствора СаСl2?
24. Сколько кристаллогидрата ZnSO4· 7H2O потребуется для приготовления 400 г 0,1 % раствора ZuSО4? (См. Ответ)
Иногда приходится приготовлять растворы определенной процентной концентрации, пользуясь для этого другими, более концентрированными растворами. Особенно часто с этим приходится сталкиваться в лаборатории при получении растворов кислот разной концентрации.
Пример 3. Сколько требуется 80% серной кислоты для приготовления 200 г 10% раствора этой кислоты?. Обозначим массу первого раствора m1, массу второго — m2, концентрацию первого раствора С1, концентрацию второго раствора C2. | |
Дано: m1 = 200г C1 = 10% C2 = 80% | Прежде всего нужно выяснить, сколько чистой безводной серной кислоты потребуется для приготовления 200 г. 10% раствора: (200 · 10) : 100 = 20 г. Определяем, в каком количестве 80% серной кислоты содержится 20 г чистой кислоты, рассуждая так: в 100 г 80% H2SО4 — 80 г чистой H2SО4 » х » 80% H2SО4 —20 » »H2SО4. Отсюда х = (100 · 20) : 80 = 25 г 80% раствора. Следовательно, для нашей цели нужно 25 г 80% раствора H2SО4 и 200—25 = 175 г воды. |
■ 25. Сколько потребуется 80% фосфорной кислоты для приготовления 2 кг 5% раствора?
26. Сколько потребуется 20% щелочи для приготовления 5 кг. 1 % раствора?
27. Сколько потребуется 15% азотной кислоты для приготовления 700 г 5% раствора?
28. Сколько потребуется 40% серной кислоты для приготовления 4 кг 2% раствора?
29. Сколько потребуется 10% соляной кислоты для приготовления 500 г 0,5% раствора? (См. Ответ)
Однако произвести правильный расчет — это для лаборанта еще не все. Нужно уметь не только рассчитать, но и приготовить раствор кислоты. Но кислоты нельзя взвешивать на весах, их можно только отмерять при помощи мерной посуды. Мерная же посуда предназначена для измерений объема, а не веса. Поэтому нужно суметь вычислить объем найденного количества раствора. Этого нельзя сделать, не зная удельного веса (плотности) раствора.
Обратимся снова к примеру 3, приведен ному на стр 67. Из таблицы (приложение III, п. 3, стр. 394) видно, что 80% серная кислота имеет плотность d=1,7, а масса раствора Р =25 г. Следовательно, по формуле
V = P : d находим: V = 25 : 1,7 = 14,7 мл.
Плотность воды практически считаем равной единице. Следовательно, 175 г воды займут объем 175 мл. Таким образом, чтобы приготовить 200 г 10% раствора из 80% серной кислоты, следует взять 175 мл воды и налить в нее 14,7 мл 80% серной кислоты. Смешивание можно производить в любой химической посуде.
■ 30. Сколько миллилитров 50% серной кислоты следует взять для приготовления 2 кг 10% раствора этой кислоты?
31. Сколько миллилитров 40% серной кислоты следует взять для приготовления 5 л 4% серной кислоты?
32. Сколько миллилитров 34% едкого кали потребуется для приготовления 10 л 10% раствора?
33. Сколько миллилитров 30% соляной кислоты потребуется для приготовления 500 мл 2% соляной кислоты? (См. Ответ)
Примеры расчетов, которые мы разбирали до сих пор, были посвящены определению веса или объема раствора, а также количества вещества, содержащегося в нем. Однако бывают случаи, когда нужно определить концентрацию раствора. Рассмотрим простейший случай.
Пример 4, Рассчитайте, какова процентная концентрация раствора, если смешано 45 г воды и 5 г соли. | |
Дано: mH2O = 45г mсоли = 5г | Решение: Сначала определяем общее количество раствора: 45 г + 5 г = 50 г. Затем определяем процентную концентрацию: (5 : 50) · 100 = 10% Следовательно раствор 10%. |
■ 34 Смешано 25 г соли и 35 г воды. Какова процентная концентрация раствора?
35. Смешано 5 г кислоты и 75 г воды. Какова процентная концентрация раствора? (См. Ответ)
Довольно часто приходится разбавлять, упаривать и смешивать растворы, после чего определять их концентрацию.
Пример 5. К 250 г 10% раствора добавили 150 г воды Какой стала концентрация раствора? | |
Дано: m1 = 250г C1 = 10% mH2O = 150г | Решение: Сначала рассчитываем содержи ние вещества в 250 г раствора: (250 · 10) : 100 = 25 г. Определяем общее количество получившегося раствора: 250 + 150 = 400 г. Поскольку мы к раствору приливали только воду, а растворенное вещество не добавляли, то его количество осталось, очевидно, таким же. Следовательно, в 400 г полученного раствора содержится 25 г вещества, а его процентная концентрация (25 : 400) · 100 = 6,25% |
■ 36. К 2 кг 20% раствора прилили 500 г воды. Какой стала концентрация раствора?
37. К 5 а 36% соляной кислоты прилили 1 л воды. Какой стала концентрация раствора?
38. Смешали 40 кг 2% и 10 кг 3% растворов одного и того же вещества. Какой стала концентрация полученного раствора?
39. Смешали 4 л 28% серной кислоты и 500 мл 60% серной кислоты. Какова концентрация полученного раствора?
40. 3 кг 20% раствора едкого натра упарили до 2 кг. Какова концентрация полученного раствора?
41. Сколько воды нужно прибавить к 500 мл 30% раствора (плотность 1,224 г/см3), чтобы получить 5% раствор? (См. Ответ)
Для определения, в каком соотношении следует смешать растворы разных концентраций, чтобы получить раствор искомой концентрации, можно применять так называемое «правило смешивания», или «диагональную
схему»
Пример 6. В каком весовом соотношении следует смешать 40% и 15% растворы, чтобы получить 35% раствор? |
Решение. Для решения составляют диагональную схему: 40→20 / 35 / 15→5 В центре пишут искомую концентрацию. У левого конца каждой диагонали пишут данные концентрации. Затем по диагонали производят вычитание: 35—15 = 20 40 — 35 = 5 (вычитают всегда из большей величины меньшую). Результат вычитания проставляют у правого конца соответствующей диагонали. Получилось, что смешать требуется 5 в. ч. 15% и 20 в. ч. 40% раствора, т. е. в соотношении 1:4. Если в смешивании участвует вода, ее концентрация берется равной 0%. |
■ 42. Рассчитайте по диагональной схеме, в каком соотношении следует смешать растворы:
а) 20% и 3% для получения 10%;
б) 70% и 17% для получения 25%;
в) 25% и воду для получения 6% (См. Ответ)
Объемная концентрация растворов. Молярная концентрация
При определении объемной концентрации растворов расчеты производят применительно к 1 л раствора. Молярная концентрация, например, показывает сколько грамм-молекул (молей) растворенного вещества содержится в 1 л раствора.
Если вы не помните, что такое грамм-молекула, обратитесь к приложению на стр. 374.
Например, если в 1л раствора содержится 1 моль вещества, то такой раствор называется одномолярным (1 М), если 2 моля, то двумолярным(2 М), если 0,1 моля, тo раствор децимолярный (0,1 М), если 0,01 моля, то раствор сантимолярный (0,01 М) и т. д. Для приготовления растворов молярной концентрации необходимо знать формулу вещества.
Пример 7. Сколько нужно взять едкого натра, чтобы приготовить 200 мл 0,1 М раствора едкого натра NaOH. | |
Дано: V = 200 мл С = 0,1 М | Решение: Прежде; всего вычислим вес грамм-молекулы едкого натра NaOH. 23 + 16 + 1 = 40 г. Так как раствор 0,1 М, то в 1 л раствора содержится 0,1 грамм-молекулы NaOH, т. е. 4 г, а в 200 мл или в 0,2 л, раствора будет содержаться неизвестное количество NaOH. Составляем пропорцию: в 1 л 0,1 М раствора — 4 г NaOH » 0.2 » » — х » NaOH Отсюда 1 : 0,2 = 4 : x x = (4 · 0,2) : 1 = 0,8 г. т. е. для приготовления 200 мл 0,1 М раствора нужно 0,8 г NaOH. |
Молярная концентрация очень удобна тем, что в равных объемах растворов с одинаковой молярностью содержится одинаковое количество молекул, так как в грамм-молекуле любого вещества содержится одно и то же число молекул.
Готовят раствор молярной концентрации в мерных колбах определенного объема. На шейке такой колбы имеется отметка, точно ограничивающая нужный объем, а надпись на колбе указывает, на какой объем рассчитана данная мерная колба.
■ 43. Рассчитайте, какое количество вещества требуется для приготовления следующих растворов:
а) 5 л 0,1 М раствора серной кислоты;
б) 20 мл 2 М раствора соляной кислоты;
в) 500 мл 0,25 М раствора сульфата алюминия;
г) 250 мл 0,5 М раствора хлорида кальция. (См. Ответ)
Растворы кислот молярной концентрации нередко приходится готовить из процентных растворов.
Пример 8. Сколько требуется 98 % серной кислоты для приготовления 5 л 0,1 М раствора. | |
Дано: V1= 5 л С1= 0,1 М С2 = 98% | Решение: Определяем содержание чистой серной кислоты в 5 л 0,1 М раствора. 1 моль H2SО4 = 98 г; 0,1 моля H2SО4 = 9,8 г. Для приготовления 5 л 0,1 М раствора H2SО4 необходимо 9,8 · 5 = 49 г чистой H2SО4. Далее найдем, сколько 98% раствора серной кислоты потребуется для приготовления 5 л 0,1 М раствора. Составим пропорцию: в 100 г раствора содержится 98 г H2SО4 » х » » » 49 » H2SO4. Отсюда х = (49 · 100) : 98 = 50 г. |
■ 44. Сколько потребуется 50% азотной кислоты для приготовления 500 мл 0,5 М раствора.
45. Какой объем 98% серной кислоты необходим для приготовления 10 л 3 М раствора?
46. Вычислите молярность следующих растворов:
а) 20% серной кислоты;
б) 4% едкого натра;
в) 10% азотной кислоты;
г) 50% едкого кали. (См. Ответ)
Нормальная концентрация растворов
Нормальная концентрация растворов выражается количеством грамм-эквивалентов растворенного вещества в 1 л раствора. Для того чтобы произвести расчет для Приготовления раствора нормальной концентрации, нужно знать, что такое эквивалент. Слово «эквивалентный» означает «равноценный».
Эквивалентом называется весовое количество элемента, которое может соединяться с 1 весовой частью водорода или замещать ее в соединениях.
Если в молекуле воды Н2О содержится два атома водорода, весящих в сумме 2 у. е., и один атом кислорода, весящий 16 у. е., то на 1 у. е. водорода приходится 8 у. е. кислорода, что и будет эквивалентом кислорода. Если мы возьмем какой-нибудь окисел, например закись железа FeO, то в нем водорода нет, но зато есть кислород, а мы нашли из предыдущего расчета, что 8 у. е. кислорода эквивалентны 1 у. е. водорода. Следовательно, достаточно найти количество железа, способное соединиться с 8 у. е. кислорода, и это также будет его эквивалентом. Атомный вес железа 56. В окисле 56 у. е. Fe приходится на 16 у. е. кислорода, а на 8 у. е. кислорода железа придется вдвое меньше.
Можно найти эквивалент и для сложных веществ, например для серной кислоты H2SО4. В серной кислоте на 1 у. е. водорода приходится половина молекулы кислоты (включая, конечно, и водород), так как кислота двухосновная, т. е. эквивалент серной кислоты равен ее молекулярному весу (98 у. е.), деленному на 2, т. е. 49 у. е.
Эквивалент для основания можно найти, разделив его молекулярный вес на валентность металла Например, эквивалент NaOH равен молекулярному весу (40 у. е.), деленному на 1, т. е. на валентность натрия. Эквивалент NaOH равен 40 у. е. Эквивалент гидроокиси кальция Са(ОН)2 равен молекулярному весу (74 у. е.), деленному на валентность кальция, а именно на 2, т. е. 37 у, е.
Для того чтобы найти эквивалент для какой-нибудь соли, нужно молекулярный вес ее разделить на валентность металла и количество его атомов. Так, молекулярный вес сульфата алюминия Al2(SO4)3 равен 342 у. е. Эквивалент его равен: 342 : (3 · 2) = 57 у.е. где 3 — валентность алюминия, а 2 — количество атомов алюминия.
■ 47. Рассчитайте эквиваленты следующих соединений; а) фосфорной кислоты; б) гидроокиси бария; в) сульфата натрия;г) нитрата алюминия. (См. Ответ)
Грамм-эквивалентом называется количество граммов вещества, численно равное эквиваленту.
Если в 1 л раствора содержится 1 грамм-эквивалент (г-экв) растворенного вещества, то раствор является одно-нормальным (1 н.), если 0,1 грамм-эквивалента, то деци-нормальным (0,1 н.), если 0,01 грамм-эквивалента, то сантинормальным (0,01 н.) и т. д. Для расчета нормальной концентрации растворов также необходимо знать формулу вещества.
Пример 9. Приготовить 300 мл 0,1 н. раствора серной кислоты H2SО4. | |
Дано: V = 300 мл С = 0,1 н. | Решение: Молекулярный вес H2SО4 равен 98 у. е., эквивалент H2SО4 равен 98 : 2 = 49 у. е., грамм-эквивалент равен 49 г. Так как раствор 0,1 н., то в 1 л его содержится 0,1 г-экв т. е. 4,9 г, нужно же приготовить 300 мл или 0,3 л этого раствора. Поэтому составим пропорцию: 1 : 0,3 = 4,9 : x x = (4,9 · 0,3) : 5 = 1,47 г. т. е. на приготовление 300 мл 0,1 н. раствора серной кислоты пойдет 1,47 г H2SО4. |
Растворы нормальной концентрации, как и молярные, готовят в мерных колбах.
■ 48. Сколько серной кислоты необходимо для приготовления 2 л 0,1 н. раствора?
49. Сколько нужно взять нитрата алюминия, чтобы приготовить 200 мл 0,5 н. раствора? (См. Ответ)
Нередко приходится готовить растворы нормальной концентрации из концентрированных растворов процентной концентрации. Это делается так же, как и при приготовлении растворов молярной концентрации, но рассчитывается не грамм-молекулярный, а грамм-эквивалентный вес .
Сколько нужно взять 60% азотной кислот, чтобы приготовить 200 мл 3 н. раствора? 61. Какой объем 20% серной кислоты необходим для приготовления 20 л 0,1 н. раствора?
Нормальная концентрация очень удобна, так как если растворы имеют одинаковую нормальность, то в равных объемах этих растворов содержатся эквивалентные количества растворенных веществ. Поэтому вещества, содержащиеся в равных объемах таких растворов, реагируют нацело (если, разумеется, вообще могут между собой реагировать). Например, если взять 1,5 л 0,1 н. раствора едкого натра и 0,1 н. раствор соляной кислоты, то для реакции с едким натром потребуется также 1,5 л раствора соляной кислоты.
Чем выше концентрация раствора, тем меньший его объем требуется для реакции, т. е. между объемами растворов реагирующих веществ и их концентрациями существует обратная зависимость, которую можно выразить формулой:

где V — объем, а С — концентрация раствора.
Исходя из этой формулы, можно определить любую из четырех величин, если известны три остальные.
Пример 10. Какова нормальность соляной кислоты, если на нейтрализацию 20 мл ее пошло 30 мл 0,1 и. едкого натра. | |
Дано: V1 = 20 мл V2 = 30 мл С2 = 0,1 н. | Решение: Подставляя данные задачи в фор мулу, получаем V1 : V2 = C2 : C1 20 : 30 = 0,1 : C1 ; C1 = (0,1 · 30) : 20 = 0,15 н. Следовательно, концентрация соляной кислоты 0,15 н. |
■ 52. На нейтрализацию 10 мл 0,2 н. раствора кислоты пошло 8 мл раствора едкого кали. Какова нормальность раствора едкого кали?
53. Какой объем 0,1 н. раствора едкого натра будет затрачен на реакцию с 25 мл 0,5 н. раствора хлорида железа (III)?
54. Сколько граммов серной кислоты содержится в 300 мл раствора, если на нейтрализацию 5 мл его израсходовано 8 мл 1 н. раствора едкого натра? (См. Ответ)
Подобные расчеты широко применяются в количественном анализе.
Нередко лаборанту нужно знать процентное содержание вещества в растворе той или иной объемной концентрации. В этом случае необходимо научиться производить перерасчет раствора объемной концентрации на весовую и наоборот.
Пример 11. Рассчитать нормальность 10% раствора едкого натра. Плотность раствора 1,115 г/см3. | |
Дано: CNaOH = 10% dNaOH = 1,115 | Решение: Грамм-эквивалент NaOH = 40 : 1 = 40 г. В 100 г раствора содержится 10 г NaOH, что равно = 0,25 г·экв. Объем 100 раствора равен 100 : 1,115 мл, следовательно в 100 : 1,115 мл — 0,25 г · экв NaOH » 1000 » -x » NaOH Отсюда х = (0,25 · 1000 · 1,115) : 100 = 2,7875 н. |
■ 55. Рассчитайте нормальность следующих растворов:
а) 28% раствора едкого кали;
б) 8% раствора едкого натра;
в) 18% раствора соляной кислоты.
56. Смешано 500 мл 20%, 20 мл 0,2 н. и 300 мл 0,5 М растворов серной кислоты. Рассчитайте нормальность и молярность образовавшегося раствора.
57. Какова молярность 40% раствора едкого натра?
58. Какова нормальность 6% раствора едкого кали?
59. Какова нормальность соляной кислоты, если на нейтрализацию 20 мл ее израсходовано 40 мл 0,2 н. раствора гидроокиси кальция?
60. В каких соотношениях надо смешать 20% и 5% растворы одного и того же вещества, чтобы получился 12% раствор?
61. Какой объем 80% раствора серной Кислоты нужно взять, чтобы приготовить 2 л 2н. раствора этой кислоты? (См. Ответ)
Статья на тему Концентрация раствора
Задача 421.
Сколько миллилитров 96%-ного (по массе) раствора H2SO4 (р = 1,84 г/мл) нужно взять для приготовления 1л 0,25 н. раствора?
Решение:
Определим молярную массу эквивалента H2SO4 из соотношения:

где
MЭ(В) — молярная масса эквивалента соли, г/моль; М(В) — молярная масса соли; n — коэффициент при атоме металла; A — валентность металла.
Отсюда

Рассчитаем массу H2SO4 в 1л 0,25н раствора по формуле:

где
m(B) — масса вещества; mЭ(В) — молярная масса эквивалента вещества, г; СЭ(В) — эквива-лентная концентрация или нормальность; V — объём раствора.
Отсюда

Теперь рассчитаем массу раствора, если известны массовая доля H2SO4 (96%) и масса H2SO4 (12,25г) по формуле:

где — массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
— массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
Тогда

Определим объём раствора H2SO4, необходимого для приготовления 1л 0,25н раствора по формуле: m = pV, где p — плотность раствора, V — объём раствора.
Тогда

Ответ: 6,93 мл.
Задача 422.
Сколько миллилитров 0,5М раствора H2SO4 можно приготовить из 15 мл 2,5М раствора?
Решение:
Для нахождения массы серной кислоты, содержащейся в 15мл 2,5М раствора, можно определить по формуле:

где
С(В) – молярная концентрация вещества (В), m(B) – масса растворённого вещества (В), М(В) – молярная масса вещества (В), V – объём раствора.
Тогда

По этому же уравнению рассчитаем объём раствора, который можно приготовить из 3,675г H2SO4:

Ответ: 75мл.
Задача 423.
Какой объем 0,1М раствора H3PO4 можно приготовить из 75 мл 0,75н. раствора?
Решение:
Для решения задачи используем формулы:

где
СЭ(В) – молярная концентрация эквивалента вещества (В);
С(В) — молярная концентрация вещества (В);
МЭ(В) – молярная масса эквивалента вещества (В);
M(B) — молярная масса вещества (В);
m(B) – масса растворённого вещества (В);
V(мл) – объём раствора.
Определим молярную массу эквивалента H3PO4 из соотношения:
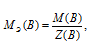
МЭ(В) — молярная масса эквивалента кислоты, г/моль; М(В) — молярная масса кислоты; Z(В) — эквивалентное число; Z(кислоты) равно числу ионов H+ в H3PO4 → 3.
Отсюда

Рассчитаем массу ортофосфорной кислоты:

Определим объём раствора H3PO4, необходимого для приготовления раствора:

Ответ: 185,7мл.
Задача 424.
Какой объем 6,0М раствора НСI нужно взять для приготовления 25 мл 2,5М раствора НСI?
Решение:
Для нахождения массы соляной кислоты, содержащейся в 25 мл 2,5М раствора, а также объёма 6,0М раствора можно использовать формулу:

С(В) — молярная концентрация вещества (В);
M(B) — молярная масса вещества (В);
m(B) – масса растворённого вещества (В);
V(мл) – объём раствора.
Тогда

Ответ: 10,42мл.
Задача 425.
Плотность 40%-ного (по массе) раствора HNO3 равна 1,25г/мл. Рассчитать молярность и моляльность этого раствора.
Решение:
Молярная(объёмно-молярная) концентрация показывает число молей растворённого вещества, содержащихся в 1 литре раствора.
Массу HNO3, содержащуюся в 1 литре раствора, рассчитаем по формуле:

где — массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
— массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
Тогда

Молярную концентрацию раствора (CM) получим делением числа граммов HNO3 в 1л раствора на молярную массу HCl (36,5г/моль):

Моляльная концентрация (или моляльность) показывает число молей растворённого вещества, содержащихся в 1000г растворителя.
Находим, сколько граммов HNO3 приходится на 1000г воды, составив пропорцию:

Теперь рассчитаем моляльность раствора:

Ответ: 7,94 моль/л; 10б=,58 моль/л.
Задача 426.
Вычислить массовую долю гидроксида натрия в 9,28н. растворе NaOН (р = 1,310г/мл).
Решение:
Найдём массу NaOН, содержащуюся в 1000 мл раствора из пропорции:

Масса 1 литра раствора NaOН (р = 1,310г/мл) равна 1310г (1000 . 1,310 = 1310).
Массовую долю гидроксида натрия вычислим по формуле:

где — массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
— массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
Тогда

Ответ: 28,34%.
