Какая масса этилового спирта и воды содержится в 1 кг 40 раствора
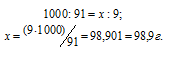
Задача 427.
Вычислить мольные доли спирта и воды в 96%-ном (по массе) растворе этилового спирта.
Решение:
Мольная доля (Ni) – отношение количества растворённого вещества (или растворителя) к сумме количеств всех
веществ, находящихся в растворе. В системе, состоящей из спирта и воды, мольная доля воды (N1) равна
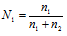 , а мольная доля спирта
, а мольная доля спирта 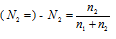 , где n1 — количество спирта; n2 — количество воды.
, где n1 — количество спирта; n2 — количество воды.
Рассчитаем массу спирта и воды, содержащихся в 1 литре раствора, при условии, что их плотности равны единице из пропорций:
а) масса спирта:
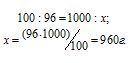
б) масса воды:
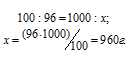
Находим количество веществ по формуле: 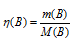 , где m(В) и М(В) – масса и количество вещества.
, где m(В) и М(В) – масса и количество вещества.
Тогда
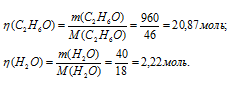
Теперь рассчитаем мольные доли веществ:
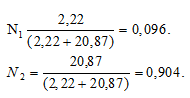
Ответ: 0,904; 0,096.
Задача 428.
В 1кг воды растворено 666г КОН; плотность раствора равна 1,395 г/мл. Найти: а) массовую долю КОН; б) молярность; в) моляльность; г) мольные доли щелочи и воды.
Решение:
а) Массовая доля – процентное отношение массы растворённого вещества к общей массе раствора определяется по формуле:

где — массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
— массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
m(р-ра) = m(H2O) + m(KOH) = 1000 + 666 = 1666 г.
Тогда
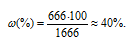
б) Молярная(объёмно-молярная) концентрация показывает число молей растворённого вещества, содержащихся в 1 литре раствора.
Найдём массу КОН, приходящуюся на 100 мл раствора по формуле: формуле: m = p V, где p — плотность раствора, V — объём раствора.
Тогда
m(KOH) = 1,395 .1000 = 1395 г.
Отсюда
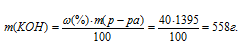
Теперь рассчитаем молярность раствора:
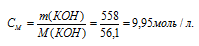
в) Моляльная концентрация (или моляльность) показывает число молей растворённого вещества, содержащихся в 1000г растворителя.
Находим, сколько граммов HNO3 приходится на 1000г воды, составив пропорцию:
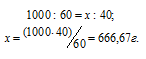
Теперь рассчитаем моляльность раствора:
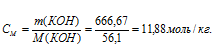
г) Мольная доля (Ni) – отношение количества растворённого вещества (или растворителя) к сумме количеств всех веществ, находящихся в растворе. В системе, состоящей из спирта и воды, мольная доля воды (N1) равна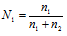 а мольная доля спирта
а мольная доля спирта 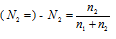 , где n1 — количество щёлочи; n2 — количество воды.
, где n1 — количество щёлочи; n2 — количество воды.
В 100г данного раствора содержится 40г КОН 60г Н2О.
Откуда
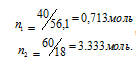
Тогда
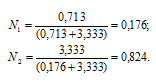
Ответ: а) 40%; б) 9,95 моль/л; в) 11,88 моль/кг; г) 0,176; 0,824.
Задача 429.
Плотность 15%-ного (по массе) раствора H2SO4 равна 1,105 г/мл. Вычислить: а) нормальность; б) молярность; в) моляльность раствора.
Решение:
Найдём массу раствора по формуле: m = p V, где p — плотность раствора, V — объём раствора.
Тогда
m(H2SO4) = 1,105 . 1000 = 1105 г.
Массу H2SO4, содержащуюся в 1000 мл раствора, находим из пропорции:
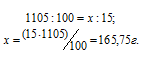
Определим молярную массу эквивалента H2SO4 из соотношения:
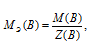
МЭ(В) — молярная масса эквивалента кислоты, г/моль; М(В) — молярная масса кислоты; Z(В) — эквивалентное число; Z(кислоты) равно числу ионов H+ в H2SO4 → 2.
Отсюда
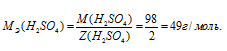
а) Молярная концентрация эквивалента (или нормальность) показывает число эквивалентов растворённого вещества, содержащегося в 1 литре раствора.
Тогда
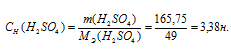
б) Моляльная концентрация (или моляльность) показывает число молей растворённого вещества, содержащихся в 1000г растворителя.
Теперь рассчитаем моляльность раствора:
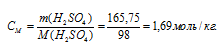
в) Моляльная концентрация (или моляльность) показывает число молей растворённого вещества, содержащихся в 1000г растворителя.
Находим, сколько граммов H2SO4 содержится в 1000г воды, составив пропорцию:
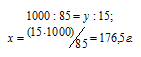
а) Массу , содержащуюся в растворе, вычислим по формуле:
Теперь рассчитаем моляльность раствора:
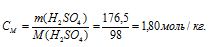
Ответ: а) 3,38н; б) 1,69 моль/л; 1,80 моль/кг.
Задача 430.
Плотность 9%-ного (по массе) раствора сахарозы С12Н22О11 равна 1,035 г/мл. Вычислить: а) концентрацию сахарозы в г/л; б) молярность; в) моляльность раствора.
Решение:
М(С12Н22О11) = 342г/моль. Найдём массу раствора по формуле: m = p V, где p — плотность раствора, V — объём раствора.
Тогда
m(С12Н22О11) =1,035 . 1000 = 1035 г.
а) Массу С12Н22О11, содержащуюся в растворе, вычислим по формуле:

где — массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
— массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
Тогда
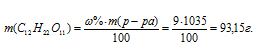
Концентрация вещества в г/л показывает число граммов (единиц массы), содержащихся в 1л раствора. Следовательно, концентрация сахарозы составляет 93,15г/л.
б) Молярная(объёмно-молярная) концентрация (СМ) показывает число молей растворённого вещества, содержащихся в 1 литре раствора.
Тогда
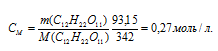
в) Моляльная концентрация (или моляльность) показывает число молей растворённого вещества, содержащихся в 1000г растворителя.
Находим, сколько граммов С12Н22О11 содержится в 1000 г воды, составив пропорцию:
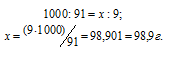
Теперь рассчитаем моляльность раствора:
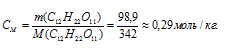
Ответ: а) 93,15 г/л; б) 0,27 моль/л; в) 0,29 моль/кг.
Задача 427.
Вычислить мольные доли спирта и воды в 96%-ном (по массе) растворе этилового спирта.
Решение:
Мольная доля (Ni) – отношение количества растворённого вещества (или растворителя) к сумме количеств всех
веществ, находящихся в растворе. В системе, состоящей из спирта и воды, мольная доля воды (N1) равна
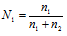 , а мольная доля спирта
, а мольная доля спирта 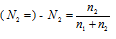 , где n1 — количество спирта; n2 — количество воды.
, где n1 — количество спирта; n2 — количество воды.
Рассчитаем массу спирта и воды, содержащихся в 1 литре раствора, при условии, что их плотности равны единице из пропорций:
а) масса спирта:
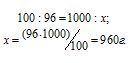
б) масса воды:
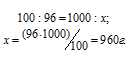
Находим количество веществ по формуле: 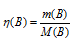 , где m(В) и М(В) – масса и количество вещества.
, где m(В) и М(В) – масса и количество вещества.
Тогда
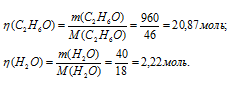
Теперь рассчитаем мольные доли веществ:
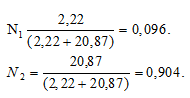
Ответ: 0,904; 0,096.
Задача 428.
В 1кг воды растворено 666г КОН; плотность раствора равна 1,395 г/мл. Найти: а) массовую долю КОН; б) молярность; в) моляльность; г) мольные доли щелочи и воды.
Решение:
а) Массовая доля – процентное отношение массы растворённого вещества к общей массе раствора определяется по формуле:

где — массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
— массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
m(р-ра) = m(H2O) + m(KOH) = 1000 + 666 = 1666 г.
Тогда
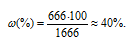
б) Молярная(объёмно-молярная) концентрация показывает число молей растворённого вещества, содержащихся в 1 литре раствора.
Найдём массу КОН, приходящуюся на 100 мл раствора по формуле: формуле: m = p V, где p — плотность раствора, V — объём раствора.
Тогда
m(KOH) = 1,395 .1000 = 1395 г.
Отсюда
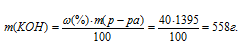
Теперь рассчитаем молярность раствора:
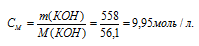
в) Моляльная концентрация (или моляльность) показывает число молей растворённого вещества, содержащихся в 1000г растворителя.
Находим, сколько граммов HNO3 приходится на 1000г воды, составив пропорцию:
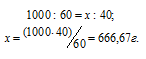
Теперь рассчитаем моляльность раствора:
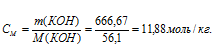
г) Мольная доля (Ni) – отношение количества растворённого вещества (или растворителя) к сумме количеств всех веществ, находящихся в растворе. В системе, состоящей из спирта и воды, мольная доля воды (N1) равна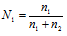 а мольная доля спирта
а мольная доля спирта 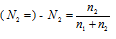 , где n1 — количество щёлочи; n2 — количество воды.
, где n1 — количество щёлочи; n2 — количество воды.
В 100г данного раствора содержится 40г КОН 60г Н2О.
Откуда
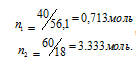
Тогда
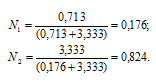
Ответ: а) 40%; б) 9,95 моль/л; в) 11,88 моль/кг; г) 0,176; 0,824.
Задача 429.
Плотность 15%-ного (по массе) раствора H2SO4 равна 1,105 г/мл. Вычислить: а) нормальность; б) молярность; в) моляльность раствора.
Решение:
Найдём массу раствора по формуле: m = p V, где p — плотность раствора, V — объём раствора.
Тогда
m(H2SO4) = 1,105 . 1000 = 1105 г.
Массу H2SO4, содержащуюся в 1000 мл раствора, находим из пропорции:
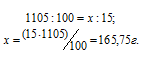
Определим молярную массу эквивалента H2SO4 из соотношения:
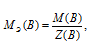
МЭ(В) — молярная масса эквивалента кислоты, г/моль; М(В) — молярная масса кислоты; Z(В) — эквивалентное число; Z(кислоты) равно числу ионов H+ в H2SO4 → 2.
Отсюда
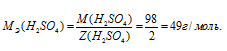
а) Молярная концентрация эквивалента (или нормальность) показывает число эквивалентов растворённого вещества, содержащегося в 1 литре раствора.
Тогда
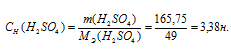
б) Моляльная концентрация (или моляльность) показывает число молей растворённого вещества, содержащихся в 1000г растворителя.
Теперь рассчитаем моляльность раствора:
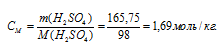
в) Моляльная концентрация (или моляльность) показывает число молей растворённого вещества, содержащихся в 1000г растворителя.
Находим, сколько граммов H2SO4 содержится в 1000г воды, составив пропорцию:
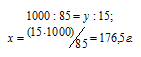
а) Массу , содержащуюся в растворе, вычислим по формуле:
Теперь рассчитаем моляльность раствора:
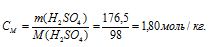
Ответ: а) 3,38н; б) 1,69 моль/л; 1,80 моль/кг.
Задача 430.
Плотность 9%-ного (по массе) раствора сахарозы С12Н22О11 равна 1,035 г/мл. Вычислить: а) концентрацию сахарозы в г/л; б) молярность; в) моляльность раствора.
Решение:
М(С12Н22О11) = 342г/моль. Найдём массу раствора по формуле: m = p V, где p — плотность раствора, V — объём раствора.
Тогда
m(С12Н22О11) =1,035 . 1000 = 1035 г.
а) Массу С12Н22О11, содержащуюся в растворе, вычислим по формуле:

где — массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
— массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
Тогда
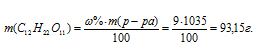
Концентрация вещества в г/л показывает число граммов (единиц массы), содержащихся в 1л раствора. Следовательно, концентрация сахарозы составляет 93,15г/л.
б) Молярная(объёмно-молярная) концентрация (СМ) показывает число молей растворённого вещества, содержащихся в 1 литре раствора.
Тогда
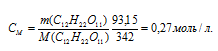
в) Моляльная концентрация (или моляльность) показывает число молей растворённого вещества, содержащихся в 1000г растворителя.
Находим, сколько граммов С12Н22О11 содержится в 1000 г воды, составив пропорцию:
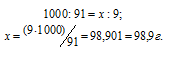
Теперь рассчитаем моляльность раствора:
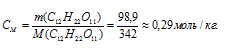
Ответ: а) 93,15 г/л; б) 0,27 моль/л; в) 0,29 моль/кг.

Для удобства пользователей и возможности быстрого нахождения решения типовых (и не очень) задач на растворы.
Часть задач на процентную концентрацию раствора, а также на массовые/объёмные доли и выход продукта — находятся в теме «Задачи на массовые и объёмные доли», задачи на коллигативные свойста растворов, буферные смеси, жесткость воды, титриметрические расчеты находятся в соответствующих темах.
Кроме того, задачи на растворы, относящиеся к определенному разделу химии частично находятся в этих темах (напр., задачи на кислотно-основной баланс, расчеты с рН и рОН — в теме «Кислоты, основания, соли»).
©Для некоммерческого использования. При перепечатке решений обязательна ссылка на источник.
Всем успеха!
ПРОИЗВЕДЕНИЯ РАСТВОРИМОСТИ:
https://www.novedu.ru/katpr.htm
Предельные подвижности ионов:
https://www.chemport.ru/data/data139.shtml
КОЭФФИЦИЕНТЫ АКТИВНОСТИ ИОНОВ:
https://www.novedu.ru/aktiv.htm
КОНСТАНТЫ ИОНИЗАЦИИ КИСЛОТ:
https://www.novedu.ru/ionkisl.htm
КОНСТАНТЫ ИОНИЗАЦИИ ОСНОВАНИЙ:
https://www.novedu.ru/ionosn.htm
ФОРМУЛЫ ДЛЯ ПРИБЛИЖЕННОГО ВЫЧИСЛЕНИЯ pН:
https://www.novedu.ru/2000/ferric.htm
ЭБУЛИОСКОПИЧЕСКИЕ (Kэ) И КРИОСКОПИЧЕСКИЕ (Kк) КОНСТАНТЫ:
https://www.novedu.ru/2000/krio.htm
СВОЙСТВА ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ (Tпл, Ткип, ρ, растворимость):
https://www.novedu.ru/solv1.htm
Плотность водных растворов кислот и щелочей:
https://fptl.ru/spravo4nik/plotnost-1.html
Электронная справочная таблица «Плотность водных растворов кислот. Плотность олеума.»:
https://techemy.com/handbook/tab0001.php
ПЛОТНОСТЬ ВОДНЫХ РАСТВОРОВ КИСЛОТ:
https://www.novedu.ru/sprav/plot.htm
Электронная справочная таблица «Плотность водных растворов щелочей. Плотность известкового молока.»:
https://techemy.com/handbook/tab0002.php
Электронная справочная таблица «Плотность водных растворов неорганических солей.»:
https://techemy.com/handbook/tab0003.php
Электронная справочная таблица «Плотность водных растворов органических веществ.»:
https://techemy.com/handbook/tab0004.php
ПЛОТНОСТЬ ВОДЫ В ИНТЕРВАЛЕ -10÷100°С:
https://www.chemport.ru/data/data35.shtml
Краткий справочник физико-химических величин» под редакцией К.П. Мищенко и А.А. Равделя:
https://eugene980.narod.ru/fh.htm
Методичка по аналитике: https://anchem.pro/sites/files/user_files/user4/doc/mu..
Пример расчета аналитической концентрации — см. задачу 85.
Закон разбавления Оствальда: Cм = Kд ∙ (1 — α) / α², для слабых электролитов α→0, Кд=α²С
Степень диссоциации α равна отношению числа (конц-и) распавшихся (диссоциировавших) молекул к общему числу (конц-и) молекул α=N/No=С/Сo
Формулы расчета и пересчета концентраций:
Масс. доля ω%= m(в-ва, г) ∙100 / m(р-ра, г)= m(в-ва, г) ∙ 100 / (ρ г/л ∙ V(р-ра, л)) =100См ∙ М / ρ, г/л = Cн ∙ М/ (10z ∙ ρ, г/мл)
Моляр. конц-я (моль/л, М) См=n(в-ва, моль) / V (р-ра, л) =1000ρ(г/мл)ω/М = Т ∙ 1000 /М
Норм. конц-я, или моляр. конц-я эквивалентов (моль/л, н) Сн (или N)=n/(ƒэкв·V)=См/ƒэкв.=См ∙ z
Моляльная конц-я (моль/кг) Cm = n(в-ва) / m(р-ля, кг) = 1000Cм / (1000ρ — Cм ∙ М)
Титр раствора (г/мл) Т=m (в-ва, г) /V (р-ра, мл) = 0,001См ∙ М
Титр по определяемому веществу, или условный титр (г/мл) T(A/B) = T(A) ∙ M(1/z B) / M(1/z A)
Мольная (молярная) доля — отношение числа молей растворенного вещества к общему числу молей всех веществ, имеющихся в растворе: χ(А) = n(А) / Σn
Правило смешивания двух р-ров с С1>С2 и объемами V: V1/V2=(C треб.-C2)/(C1-C треб.), или
двух р-ров с массами m: m1/m2=(С треб.- С2)/(С1- С треб.)
C получ.= (C1m1+C2m2)/(m1+ m2) = (C1V1ρ1+C2V2ρ2)/(V1+ V2)
Отредактировал администратор, 14 июл 2019 в 16:24.

Задача 1
Kакую молярность и нормальность имеет 40% раствор серной кислоты (p=1,307 г/мл)?
Решение:
См=1000pw/М = 1000 мл/л ∙ 1,307 г/мл ∙ 0,40 / 98,08 г/моль = 5,330 моль/л
Сн=См ∙ z
Число эквивалентности равно основности кислоты, отсюда: Сн=5,330 моль/л ∙ 2 = 10,66 моль/л

Задача 2
Найти массу раствора с массовой долей спирта 96%, который можно приготовить из этанола объемом 20 мл ( р=0,8 г/мл).
Решение:
масса чистого этанола m(C2H5OH)=V*p=20 мл * 0,8 г/мл = 16 г
масса раствора: m(раствора)=m(C2H5OH)*100% : w% = 16 г * 100% / 96% = 16,7 г

Задача 3
Вычислить нормальность раствора, если Т NaOH/SO3 = 0.02174.
Решение:
Т (NaOH/SO3) = 0.02174, нормальность, следует понимать, NaOH
Т (NaOH/SO3) = T(NaOH) x M(1/2 SO3) / M(NaOH)
0.02174= T(NaOH) x 40/40 = T(NaOH)
T(NaOH)=C(NaOH) x M(NaOH) / 1000
C(NaOH) = T(NaOH) / M(NaOH) х 1000
C(NaOH) =0.02174 / 40 х 1000
ответ: С(NaOH)=0,5431 N

Задача 4
Чему равно кол-во обменных эквивалентов в 1 моль вещества (z) для Na2СО3? (для определения нормальной концентрации рас-ра)
Ответ:
Фактор эквивалентности Na2CO3 в обменной реакции равен 1/2

Задача 5
Сколько граммов карбоната натрия потребуется для приготовления 2 л раствора с молярной концентрацией эквивалента 0,2 моль/ л?
Решение:
Молярная конц-я эквивалента (или нормальная конц-я) измеряется в моль-экв/л, а не в моль/л.
Но это так, в порядке примечания 🙂
Сн = 0,2 моль-экв/л
Сн = n/(ƒэкв·V) = m/(М · ƒэкв · V)
m = Сн · М ·ƒэкв · V
Для соли фактор эквивалентности ƒэкв = 1/произведение числа катионов на их заряд, т.о.
ƒэкв (Na2CO3)= ½
m (Na2CO3) = 0,2 моль-экв/л · 106 г/моль ·½ экв^-1 · 2 л = 21,2 г

Задача 6
Решение:
В 100 г р-ра 0,01 г соли, тогда в 200 г: 0,02 г соли и 200-0,02 = 199,98 г воды

Задача 7
При нагревании 120г 10%-ного раствора хлорида калия массовая доля растворенного вещества увеличилась в 1,2 раза. Сколько воды испарилось? (20г)
Решение:
Масса выпаренной воды m(воды)= m1(р-ра до выпаривания) — m2(р-ра после выпаривания)
При выпаривании воды масса соли не изменилась. Из формулы массовой доли:
ω%= m(соли) ∙ 100 / m(раствора),
m(соли)= m(раствора) ∙ ω% / 100 , поэтому:
ω1 ∙ m1(р-ра) = ω2 ∙ m2(р-ра)
ω2 = 1,2ω1
⇒ m2(р-ра) = ω1 ∙ m1(р-ра) / ω2 = ω1 ∙ m1(р-ра) / 1,2ω1 = m1(р-ра) / 1,2 = 120/1,2 = 100 г
⇒m(воды) = 120-100=20 г

Задача 8
Сколько граммов нитрата бария и 10 %- ного раствора нитрата бария нужно взять для приготовления 180 г 20 %-ного раствора этой соли? ( 20 г соли и 160 г раствора)
Решение:
m(соли в новом р-ре)= m(раствора) ∙ ω% / 100 = 180 ∙ 20 / 100 = 36 г
⇒ нужна масса воды 180-36 = 144 г
В 100 г 10% раствора 10 г соли и 90 г воды,
в Х г 10% раствора 144 г воды
Х = 144 ∙ 100 / 90 = 160 г 10%-го р-ра
В этом количестве содержится m(соли)= 160 ∙ 0,1 = 16 г
Значит нужно в раствор добавить еще 36-16=20 г соли.

Задача 9
Какова процентная концентрация раствора, полученного в результате растворения 18 г едкого натра в 180 г воды?
Решение:
Процентная концентрация раствора ω% = m(едкого натра) ∙ 100 / m(раствора)
m(раствора) = m(едкого натра) + m(воды)
ω% = 18 ∙ 100 / (180 + 18) = 9,1%

Задача 10
Определите нормальную концентрацию раствора, содержащего 33 г сульфида калия в 200 мл раствора.
Ответ: 1) 6Н; 2) 0,3Н; 3) 1,5Н; 4) 3Н.
Решение:
Нормальная конц-я Сн = Э/V = m/(Mэ ∙М)
Мэ = М / z
z = произведение заряда катиона на число катионов (или произведение заряда аниона на число анионов)
Для K2S z =2
Сн = 33 / (110/2 ∙ 0,2) = 3Н
Можно перевести молярную конц-ю в нормальную (и обратно): Сн = См ∙ z

Задача 11
40 г гидроксида натрия содержится следующем количестве 5% раствора:
А)800г Б)300г В)200 г.
Решение:
ω%= m (в-ва) ∙ 100/ m(p-pa) ⇒ m(p-pa) = m (в-ва) ∙ 100/ ω% = 40 ∙ 100/ 5 = 800 г

Задача 12
В растворе содержится 2кг воды и 400 г NaOH . Моляльная концентрация раствора равна 8 или 5?
Решение:
Моляльная конц-я — число молей в-ва в 1 кг (1000 г) растворителя (здесь — воды).
Cm = n (NaOH) / m (воды, кг) = m(NaOH) / [M (NaOH) ∙ m (воды, кг)] = 400 / (40 ∙ 2) = 5 моль/кг

Задача 13
В 2 литрах децимолярного раствора серной кислоты содержится растворенного вещ-ва:
1)4,9 г 2)9,8 г 3)9,6 г
Решение:
m = n ∙ M = Cм ∙ V ∙ M = 2 ∙ 0,1 ∙ 98 = 19,6 г

Задачa 14
Смешали 10 см3 10%-ного раствора HNO3 (пл. 1,056 г/см3) и 100 см3 30%-ного раствора HNO3 (пл. 1,184 г/см3). Вычислите массовую (процентную) долю полученного раствора. Ответ: 28.38%
Решение:
w%(раствора) = [m1(HNO3) + m2(HNO3)] / [m(раствора1) + m(раствора2)] x 100
m(раствора1)=V(раствора1) x p1 = 10 x 1,056 = 10,56 г
m(раствора2)=V(раствора2) x p2 = 100 x 1,184 = 118,4 г
m1(HNO3)=m(раствора1) x w1 = 10,56 x 0,1= 1,056 г
m2(HNO3)=m(раствора2) x w2 = 118,4 x 0,3= 35,52 г
w%(раствора) = (1,056+35,52) / (10,56+118,4) x 100 = 28,36%

Задачa 15
Какую навеску гидроксида натрия следует взять для приготовления 0,5 литра 0,2 N р-ра?
Решение:
n=CV=0,5 x 0,2=0,1 mol
m=nxM=0,1×40=4 gr

Задачa 16
Решение:
m=n∙M
M=98
n1=Cм∙V ⇒m=Cм∙V∙M = 0,1∙0,25∙98 = … г
n2=Cн∙V∙fэ ⇒ m=Cм∙V∙fэ∙M = 0,1∙0,25∙½∙98 = … г
(fэ — фактор эквивалентности, для кислоты=1/основность, т.е. для Н2SO4 = ½)

Задача 17
Решение:
Фактор эквивалентности щелочи равен числу ОН-, поэтому для NaОН См= Сн
См1∙ V1 = См2∙ V2 ⇒ V1= См2∙ V2/ См1 = 2,8 ∙ 20 / 18 = 3,11 л
В 1 л получ. р-ра 2,8 моль NaОН.
ω%(NaОН) = m(NaОН)∙100/m(p-pa)
m(p-pa) = V(мл) ∙ ρ = 1000 ∙ 1,11 = 1110 г
m(NaОН) = n(NaОН) ∙ M(NaОН)
M(NaОН)=40 г/моль
n(NaОН) = См2∙ V2 (л) = 2,8 ∙ 1 = 2,8 моль
⇒ ω%(NaОН) = 2,8 ∙ 40 ∙ 100 / 1110 = 10,1%

Задача 18
Во сколько раз концентрация ионов водорода в 0,1 н растворе азотистой кислоты больше, чем в 0,1 н растворе циановодородной кислоты? Константа диссоциации HNO2 равна 5 10^-4, константа диссоциации HCN равна 7,9∙10^-10.
Решение:
Обе кислоты одноосновные, поэтому нормальность равна молярности.
Cм = [H+]²/Кд ⇒ [H+]=√ (Cм ∙ Кд)
Для HNO2: [H+ в р-ре HNO2]=√ (0,1 ∙ 5 ∙10^-4)
Для HCN: [H+ в р-ре HCN]=√ (0,1 ∙ 7,9 ∙10^-10)
[H+ в р-ре HNO2] / [H+ в р-ре HCN] =
√ ( 5 ∙10^-4) / √ ( 7,9 ∙10^-10) = 796
Т.е. [H+] в 0,1 н. HNO2 больше в 796 раз, чем в 0,1 н. HCN.

Задача 19
Решение:
По закону разбавления Оствальда:
Cм = Kд ∙ (1 — α) / α²
где Cм — молярная концентрация, Kд — константа диссоциации кислоты, α — степень диссоциации.
Поскольку уксусная кислота — слабый электролит (Кд « 1), можно воспользоваться законом разбавления для слабых электролитов:
Кд = α²С, тогда α=√(Кд/С) = √(1,75 ∙ 10^-5 / 0,2) = 9,35 ∙ 10^-3 (0,94%)
При разведении спирта необходимо помнить, что его концентрация выражается как процентом по объему, так и процентом по массе.
Объемная концентрация спирта обозначается: %, °, % (об/об).
Массовая концентрация спирта обозначается: % (м), % (м/м).
При решении задач на разведение или укрепление спирта пользуются расчетными формулами, правилом «креста», а также алкоголеметрическими таблицами.
Алкоголеметрические таблицы (Государственная фармакопея Республики Беларусь, том I, с 556 – 568):
Таблица 5.5.-1 – Соотношение между плотностью водно-спиртового раствора
Пользуясь данной таблицей, можно определить по плотности спирта его концентрацию в процентах по массе и по объему и, наоборот, зная концентрацию спирта, определить его плотность; перевести концентрацию спирта из массового процента в объемный или из объемного в массовый; найти количество граммов безводного спирта в 100 мл водно-спиртового раствора или количество миллилитров безводного спирта в 100 г водно-спиртового раствора (при 20 °С).
Примеры задач.
1. Показание плотности водно-спиртового раствора при температуре 20оС по ареометру составило 0,9736. Определить концентрацию данного раствора.
Решение:
По таблице 5.5.-1 в столбце «плотность ρ20» находим заданное значение плотности, затем в столбце «содержание этанола в водно-спиртовом растворе в процентах по объему» находим соответствующее ей значение концентрации процентах: 0,9736 – 20%.
Ответ: концентрация спирта 20% (при 20 оС).
2. Концентрация спирта равна 20%. Определите концентрацию данного спирта в процентах по массе.
Решение:
По таблице 5.5.-1 находим концентрацию данного спирта в процентах по объему и соответствующее ей значение концентрации процентах по массе: 20% — 16,21% (м/м).
Ответ: концентрация спирта 20% в процентах по массе составляет 16,21% (м/м) (при 20 оС).
Таблица 5.5.-2 – Количество (в граммах при 20 °С) воды и спирта разной концентрации, которые необходимо смешать, чтобы получить 1 кг спирта концентрации 30%, 40%, 50%,60%, 70%, 80%, 90% и 92%
Пример задачи:
Какое количество спирта 96% и воды надо взять, чтобы получить 10 кг спирта 70%?
Решение:
По таблице 5.5.-2 на пересечении строки «крепость взятого спирта в %» и столбца «70%» находим, что для получения 1 кг спирта 70% надо взять 665 г спирта 96% и 335 г воды. По условию задачи необходимо получить 10 кг спирта 70%, значит, составляем следующие пропорции:
665 — 1 335 — 1
х — 10 у — 10
х = 6650 у = 3350
Ответ: чтобы получить 10 кг спирта 70% необходимо взять 6,65 кг спирта 96% и 3,35 кг воды.
Таблица 5.5.-3 – Количество (в миллилитрах при 20 °С) воды и спирта разной концентрации, которые необходимо смешать, чтобы получить 1 л спирта концентрации 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%
Пример задачи:
Какое количество спирта 90% и воды надо взять, чтобы получить 500 мл спирта 40%?
Решение:
По таблице 5.5.-3 на пересечении строки «концентрация взятого спирта в %» и столбца «40%» находим, что для получения 1 л спирта 40% надо взять 444 мл спирта 90% и 581 мл воды. По условию задачи необходимо получить 500 мл спирта 40%, значит, составляем следующие пропорции:
444 — 1 581 — 1
х — 0,5 у — 0,5
х = 222 у = 290,5
Ответ: чтобы получить 500 мл спирта 40% необходимо взять 222 мл спирта 90% и 290,5 мл воды.
Таблица 5.5.-4 – Количество (в миллилитрах при 20 °С) воды и спирта разной концентрации, которые необходимо смешать, чтобы получить 1 л (при 20 °С) спирта концентрации 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%
Таблица аналогична таблице 5.5.-3, за исключением того, что концентрация разводимого спирта составляет от 95,1% до 96,5%.
Пример задачи:
Какое количество спирта 96,5% и воды надо взять, чтобы получить 2 л спирта40%?
Решение:
По таблице 5.5.-4 на пересечении строки «концентрация взятого спирта в %» и столбца «40%» находим, что для получения 1 л спирта 40% надо взять 414,5 мл спирта 96,5% и 615,3 мл воды. По условию задачи необходимо получить 2 л спирта 40%, значит, составляем следующие пропорции:
414,5 — 1 615,3 — 1
х — 2 у — 2
х = 829 у = 1230,6
Ответ: чтобы получить 2 л спирта 40% необходимо взять 829 мл спирта 96,5% и 1230,6 мл воды.
Таблица 5.5.-5 – Таблица для получения спирта различной крепости при 20°С
С помощью данной таблицы можно найти объем воды, который необходимо прилить к данному объему крепкого спирта, чтобы получить водно-спиртовой раствор требуемой концентрации.
Пример задачи:
Какое количество воды надо прилить к 50 мл спирта 95%, чтобы получить спирт 40%?
Решение:
По таблице 5.5.-5 на пересечении строки «концентрация взятого спирта в %» и столбца «40%» находим, что для получения спирта 40% надо прилить 1443 мл воды к 1000 мл спирта 95%. По условию задачи объем спирта 95% 50 мл, значит, составляем следующие пропорции:
1443 — 1000
х — 0,05
х = 72,15
Ответ: чтобы получить спирт 40% необходимо прилить 72,15 мл воды к 50 мл спирта 95%.
Таблица 5.5.-6 – Количество (в миллилитрах при 20 °С) воды и спирта концентрации 96,6% — 97,0%, которые необходимо смешать, чтобы получить 1 л (при 20 °С) спирта концентрации 40%, 70%, 80%, 90%, 95%
Таблица практически представляет собой продолжение таблицы 5.5.-4, задачи решаются по аналогии с вышеприведенным решением.
