Какая функциональная группировка придает аминокислоте кислые свойства


Химический состав клетки Семинар

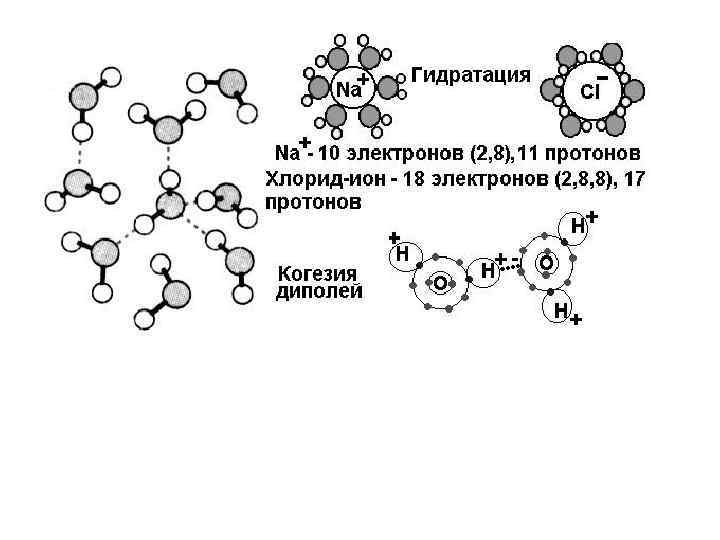
1. Какие элементы называются биогенными? Сколько их? 2. На какие группы делятся макроэлементы? 3. Чем ковалентные связи отличаются от водородных? 4. Почему лед образуется на поверхности воды? 5. Какие вещества называются гидрофобными? Гидрофильными? 6. Какой заряд на атоме кислорода и на атомах водорода в молекуле воды? Почему? 7. Сколько водородных связей может образовывать одна молекула воды? 8. Почему ион натрия имеет положительный заряд? 9. Почему ион хлора имеет отрицательный заряд?

1. К моносахаридам относятся: 1. Крахмал. 5. Свекловичный сахар (сахароза). 2. Гликоген. 6. Мальтоза. 3. Глюкоза. 7. Молочный сахар (лактоза). 4. Дезоксирибоза. 8. Рибоза. 2. К полисахаридам относятся: 1. Крахмал. 5. Рибоза. 2. Гликоген. 6. Мальтоза. 3. Глюкоза. 7. Молочный сахар (лактоза). 4. Дезоксирибоза. 8. Целлюлоза. 3. К дисахаридам относятся: 1. Крахмал. 2. Свекловичный сахар (сахароза). 3. Глюкоза. 4. Дезоксирибоза. 5. Хитин. 6. Мальтоза. 7. Молочный сахар (лактоза). 8. Целлюлоза.
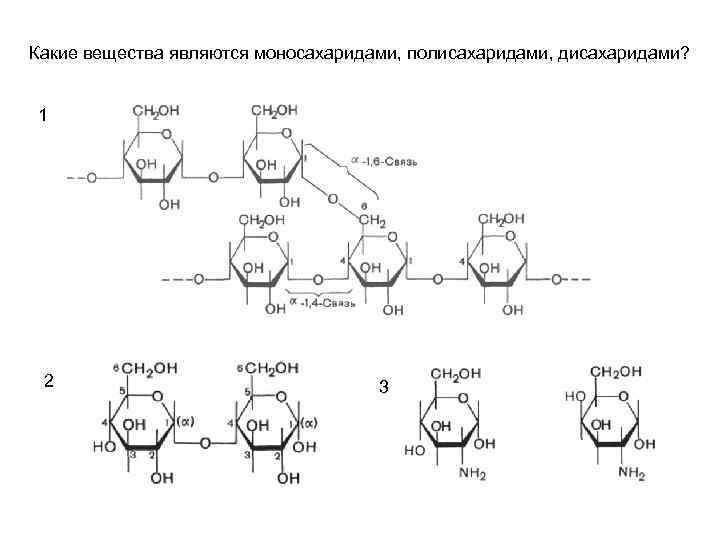
Какие вещества являются моносахаридами, полисахаридами, дисахаридами? 1 2 3
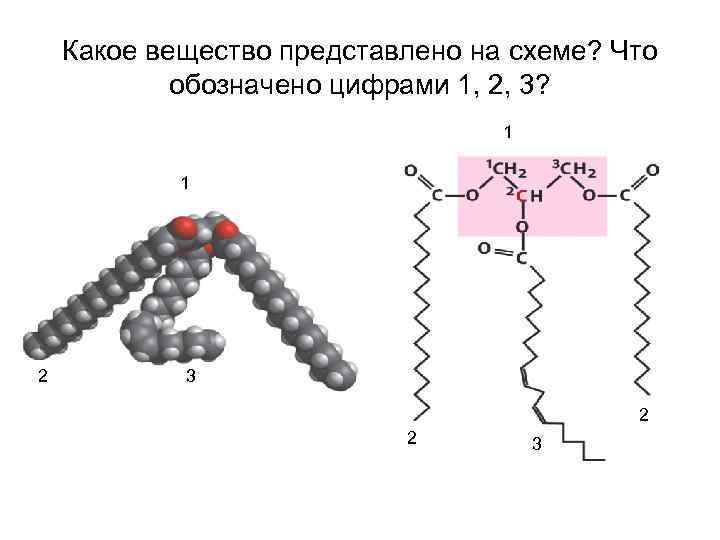
Какое вещество представлено на схеме? Что обозначено цифрами 1, 2, 3? 1 1 2 3 2 2 3

1. При полном сгорании 1 г. вещества выделилось 38, 9 к. Дж энергии. Это вещество относится: 1. К углеводам. 2. К жирам. 3. Или к углеводам, или к липидам. 4. К белкам. 2. Основу клеточных мембран образуют: 1. Жиры. 2. Фосфолипиды. 3. Воска. 4. Липиды. 3. Утверждение: «Фосфолипиды — сложные эфиры глицерина (глицерола) и жирных кислот»: Верно. Ошибочно.

4. Липиды выполняют в организме следующие функции: 1. Структурную. 5. Некоторые являются ферментами. 2. Энергетическую. 6. Источник метаболической воды 3. Теплоизолирующую. 7. Запасающую. 4. Некоторые — гормоны. 8. К ним относятся витамины A, D, E, K. 5. Молекула жира состоит из остатков: 1. Аминокислот. 2. Нуклеотидов. 3. Глицерина. 4. Жирных кислот. 6. Гликопротеины — это комплекс: 1. Белков и углеводов. 2. Нуклеотидов и белков. 3. Глицерина и жирных кислот. 4. Углеводов и липидов.
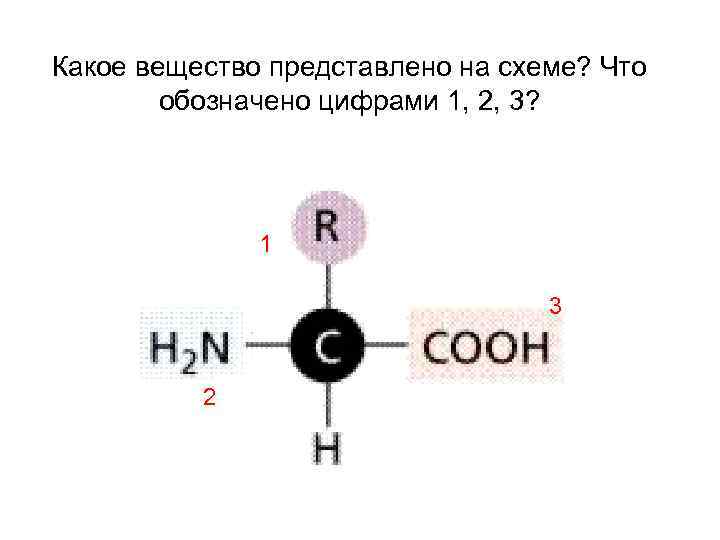
Какое вещество представлено на схеме? Что обозначено цифрами 1, 2, 3? 1 3 2
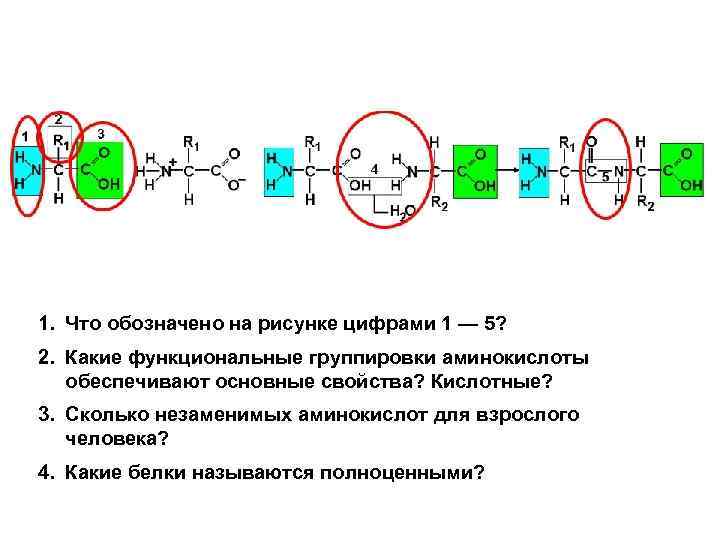
1. Что обозначено на рисунке цифрами 1 — 5? 2. Какие функциональные группировки аминокислоты обеспечивают основные свойства? Кислотные? 3. Сколько незаменимых аминокислот для взрослого человека? 4. Какие белки называются полноценными?

1. На первом месте по массе из органических веществ в клетке находятся: 1. Углеводы. 2. Белки. 3. Липиды. 4. Нуклеиновые кислоты. 2. В состав простых белков входят следующие элементы: 1. Углерод. 5. Фосфор. 2. Водород. 6. Азот. 3. Кислород. 7. Железо. 4. Сера. 8. Хлор. 3. Количество различных стандартных аминокислот, встречающихся в белках: 1. 170. 2. 26. 3. 20. 4. 10.

4. Количество незаменимых для человека аминокислот: 1. Таких аминокислот нет. 2. 20. 3. 10. 4. 7. 5. Неполноценные белки — белки: 1. В которых отсутствуют некоторые аминокислоты. 2. В которых отсутствуют некоторые незаменимые аминокислоты. 3. В которых отсутствуют некоторые заменимые аминокислоты. 4. Все известные белки являются полноценными. 6. Придают аминокислотам свойства: 1. Кислые — радикал, щелочные — аминогруппа. 2. Кислые — аминогруппа, щелочные — радикал. 3. Кислые — карбоксильная группа, — щелочные — радикал. 4. Кислые — карбоксильная группа, щелочные — аминогруппа.

7. Пептидная связь образуется в результате: 1. Реакции гидролиза. 2. Реакции гидратации. 3. Реакции конденсации. 4. Все выше перечисленные реакции могут привести к образованию пептидной связи. 8. Пептидная связь образуется: 1. Между карбоксильными группами соседних аминокислот. 2. Между аминогруппами соседних аминокислот. 3. Между аминогруппой одной аминокислоты и радикалом другой. 4. Между аминогруппой одной аминокислоты и карбоксильной группой другой. 9. Вторичную структуру белков стабилизируют: 1. Ковалентные. 2. Водородные. 3. Ионные. 4. Такие связи отсутствуют.

10. Третичную структуру белков стабилизируют: 1. Ковалентные. 2. Водородные. 3. Ионные. 4. Гидрофильно-гидрофобное взаимодействие. 5. Все выше перечисленные виды связей. 11. Верные суждения: 1. Ферменты специфичны, каждый фермент обеспечивает реакции одного типа. 2. Ферменты универсальны и могут катализировать реакции разных типов. 3. Каталитическая активность ферментов не зависит от р. Н и температуры. 4. Каталитическая активность ферментов напрямую зависит от р. Н и температуры. 12. Верное суждение: 1. Все белки являются биологическими катализаторами, ферментами. 2. Ренатурация — утрата трехмерной конфигурации белка без изменения первичной структуры. 3. Витамины являются коферментами многих ферментов.

Какое вещество представлено на рисунке? Что обозначено цифрами 1, 2, 3, 4? 3 4 2 1
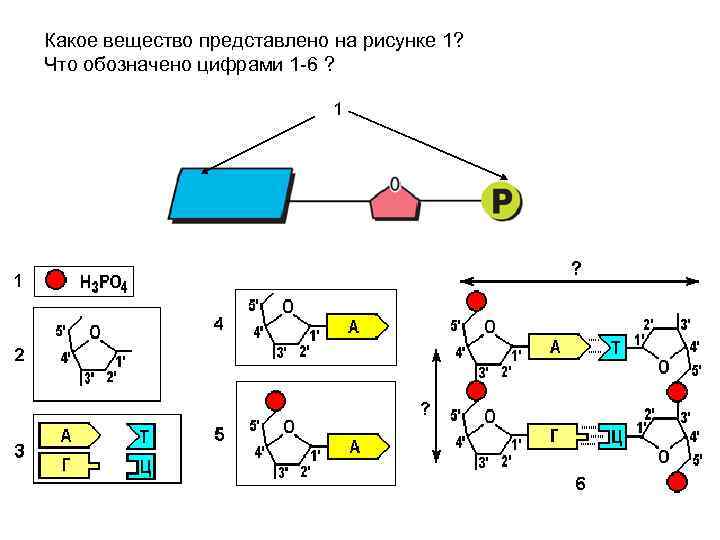
Какое вещество представлено на рисунке 1? Что обозначено цифрами 1 -6 ? 1

1. ДНК в клетках эукариот содержится: 1. В цитоплазме. 5. В пластидах. 2. В ядре. 6. В комплексе Гольджи. 3. В рибосомах. 4. В митохондриях. 2. Размеры молекулы ДНК у человека: 1. Ширина 20 мкм, длина до 8 см. 2. Ширина 2 мкм, длина до 8 см. 3. Ширина 20 нм, длина до 8 см. 4. Ширина 2 нм, длина до 8 см. 3. В состав молекулы ДНК входят пуриновые основания: 1. Аденин. 2. Гуанин. 3. Тимин. 4. Цитозин.

4. Фрагмент ДНК содержит 30000 нуклеотидов. Для удвоения фрагмента потребуется свободных нуклеотидов: 1. 60000. 2. 45000. 3. 30000. 4. 15000. 5. Нуклеотиды ДНК соединены в одну цепь: 1. Через остаток фосфорной кислоты одного нуклеотида и 3′ атом дезоксирибозы другого. 2. Через остаток фосфорной кислоты одного нуклеотида и азотистое основание другого. 3. Через остатки фосфорной кислоты соседних нуклеотидов. 4. Через дезоксирибозы соседних нуклеотидов.

6. Фрагмент ДНК содержит 30000 А-нуклеотидов. Для удвоения фрагмента потребуется: 1. А — 60000, Т — 60000. 2. А — 30000, Т — 30000. 3. А — 15000, Т — 15000. 4. Данных для ответа недостаточно. 7. Фрагмент ДНК содержит 30000 А-нуклеотидов и 40000 Цнуклеотидов. В данном фрагменте Т- и Г-нуклеотидов: 1. Т — 40000, Г — 30000. 2. Т — 30000, Г — 40000. 3. Т — 60000, Г — 80000. 4. Данных для ответа недостаточно. 8. Предложили модель строения молекулы ДНК в 1953 году: 1. Ф. Крик. 2. Г. Мендель. 3. Т. Морган. 4. Д. Уотсон.

9. Функции ДНК в клетке: 1. Один из основных источников энергии. 2. Принимает непосредственное участие в синтезе белков. 3. Обеспечивает синтез углеводов и липидов в клетке. 4. Участвует в хранении и передаче наследственной информации. 10. Верные суждения: 1. Цепи нуклеотидов в молекуле ДНК антипараллельны. 2. Между А- и Т-нуклеотидами 2 водородные связи, между Г- и Цнуклеотидами 3 водородные связи. 3. А- и Т-нуклеотиды относятся к пиримидиновым нуклеотидам. 4. В состав нуклеотидов ДНК входит сахар рибоза.
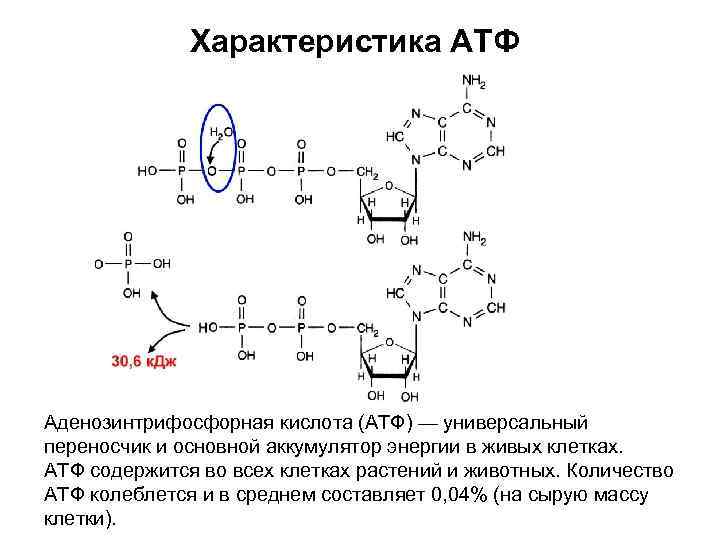
Характеристика АТФ Аденозинтрифосфорная кислота (АТФ) — универсальный переносчик и основной аккумулятор энергии в живых клетках. АТФ содержится во всех клетках растений и животных. Количество АТФ колеблется и в среднем составляет 0, 04% (на сырую массу клетки).
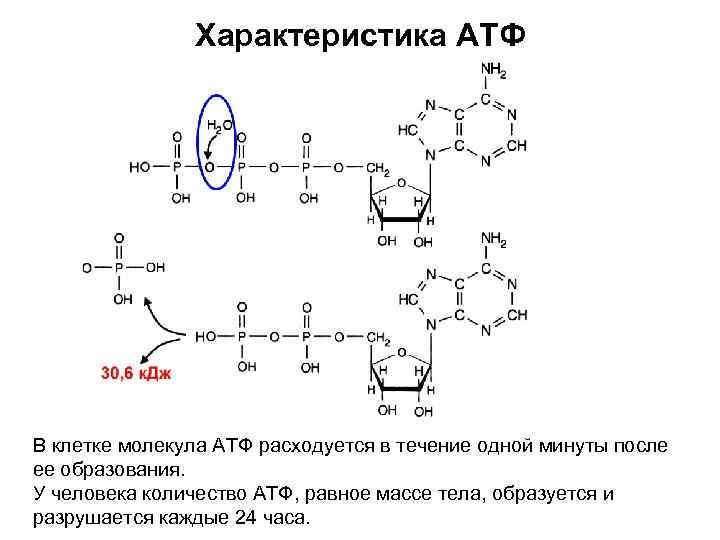
Характеристика АТФ В клетке молекула АТФ расходуется в течение одной минуты после ее образования. У человека количество АТФ, равное массе тела, образуется и разрушается каждые 24 часа.
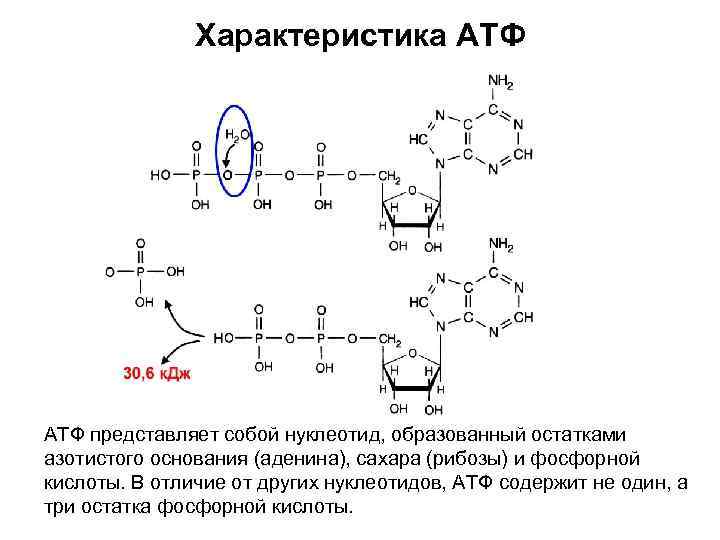
Характеристика АТФ представляет собой нуклеотид, образованный остатками азотистого основания (аденина), сахара (рибозы) и фосфорной кислоты. В отличие от других нуклеотидов, АТФ содержит не один, а три остатка фосфорной кислоты.
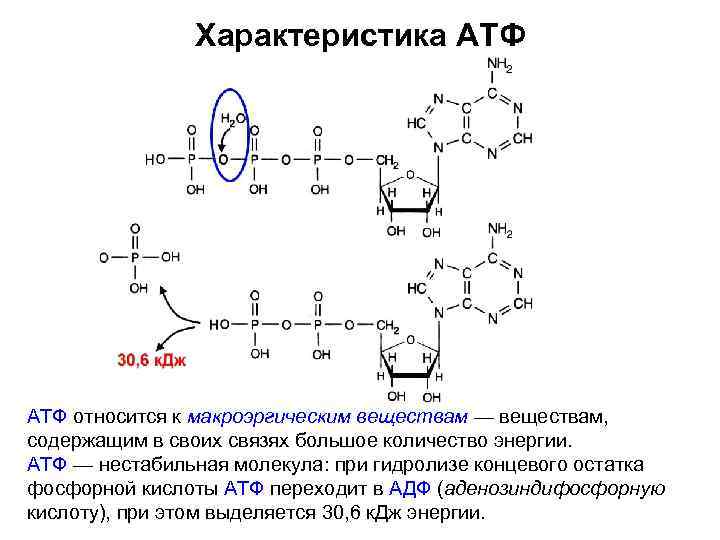
Характеристика АТФ относится к макроэргическим веществам — веществам, содержащим в своих связях большое количество энергии. АТФ — нестабильная молекула: при гидролизе концевого остатка фосфорной кислоты АТФ переходит в АДФ (аденозиндифосфорную кислоту), при этом выделяется 30, 6 к. Дж энергии.
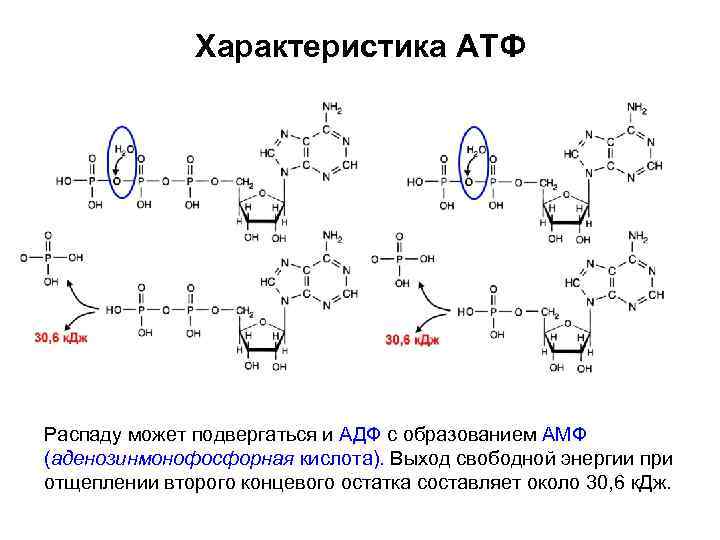
Характеристика АТФ Распаду может подвергаться и АДФ с образованием АМФ (аденозинмонофосфорная кислота). Выход свободной энергии при отщеплении второго концевого остатка составляет около 30, 6 к. Дж.
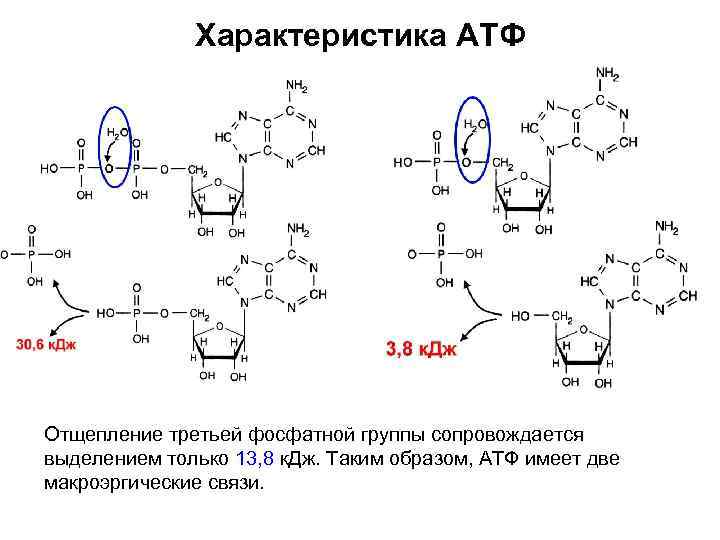
Характеристика АТФ Отщепление третьей фосфатной группы сопровождается выделением только 13, 8 к. Дж. Таким образом, АТФ имеет две макроэргические связи.

Какие суждения верны: • Молекула РНК представляет собой неразветвленную полинуклеотидную цепь. • В состав нуклеотидов РНК входит сахар рибоза. • Азотистые основания в РНК представлены аденином, гуанином, тимином и цитозином. • Самые крупные молекулы РНК содержатся в рибосомах, р. РНК. • Нуклеотиды РНК способны образовывать водородные связи между собой, но это внутрицепочечные, а не межцепочечные соединения комплементарных нуклеотидов. • Цепи РНК значительно длиннее молекул ДНК. • РНК обеспечивают синтез белков в клетке.

Какие суждения верны: 8. Молекула РНК состоит из двух комплементарно связанных и антипараллельно направленных полинуклеотидных цепей. 9. Молекулы РНК образуются в результате самоудвоения, репликации. 10. АТФ представляет собой нуклеотид, образованный остатками азотистого основания (аденина), сахара (дезоксирибозы) и фосфорной кислоты. 11. При гидролизе макроэргических связей двух моль АТФ до АМФ выделяется около 160 к. Дж энергии.
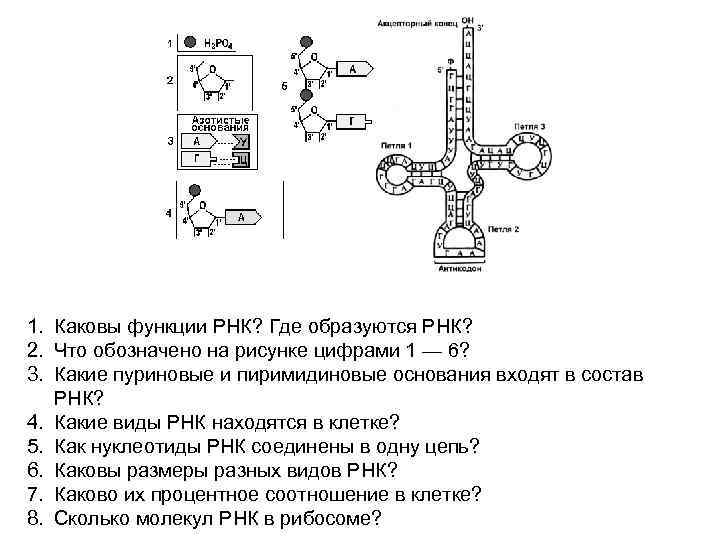
1. Каковы функции РНК? Где образуются РНК? 2. Что обозначено на рисунке цифрами 1 — 6? 3. Какие пуриновые и пиримидиновые основания входят в состав РНК? 4. Какие виды РНК находятся в клетке? 5. Как нуклеотиды РНК соединены в одну цепь? 6. Каковы размеры разных видов РНК? 7. Каково их процентное соотношение в клетке? 8. Сколько молекул РНК в рибосоме?
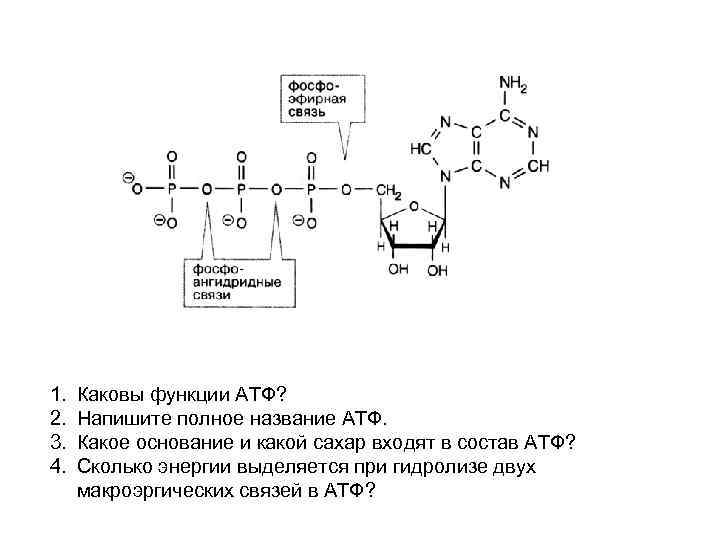
1. 2. 3. 4. Каковы функции АТФ? Напишите полное название АТФ. Какое основание и какой сахар входят в состав АТФ? Сколько энергии выделяется при гидролизе двух макроэргических связей в АТФ?
Инфоурок
›
Химия
›Презентации›Презентация к уроку химии в 10 классе на тему Белки
Описание презентации по отдельным слайдам:
1 слайд

Описание слайда:
Белки. Строение, функции, свойства Муниципальное бюджетное общеобразовательное учреждение средняя общеобразовательная школа №1 г. Задонска Разработала: Родионова Д.О Руководитель практики: Писарева И.М. Задонск, 2017 г.
2 слайд

Описание слайда:
«Жизнь – это способ существования белковых тел» Ф. Энгельс Биологические полимеры Нуклеиновые кислоты Жиры Углеводы БЕЛКИ
3 слайд

Описание слайда:
Актуализация опорных знаний по теме: «Аминокислоты» Что называется аминокислотой? Какая функциональная группировка придает аминокислоте – кислотные, а какая – щелочные свойства? Каким особым свойством обладают аминокислоты? В результате какой реакции образуется пептидная связь? Как называют соединение, образованное при взаимодействии трех аминокислот? Сколько видов аминокислот входит в состав белков?
4 слайд

Описание слайда:
Что такое «белки»? Белки – это высокомолекулярные природные полимеры, молекулы которых построены из остатков α-аминокислот, соединенных амидной (пептидной) связью. 20 остатков аминокислот теоретически дают возможность составить около 2 • 1018 вариантов белковых молекул, различающихся порядком чередования аминокислот Элементарный состав белковых веществ Углерод (С) – 51-53 % Кислород (О) – 21.5-23.5 % Азот (N) – 16.8-18.4 % Сера (S) – 0,3-2,5 % Водород (Н) – 6.5-7.3 %
5 слайд

Описание слайда:
Первичная структура белковых молекул Последовательность соединения аминокислотных остатков в полипептидной цепи получила название первичной структуры белка Группа атомов –СО – NH -, с помощью которой связаны две α-аминокислоты, называется пептидной связью
6 слайд

Описание слайда:
Вторичная структура белковых молекул Вторичная структура белка — это спираль, которая образуется в результате скручивания полипептидной цепи за счет водородных связей между группами СО и NH. α-вторичная структура -правозакрученная спираль, образованная при помощи водородных связей между пептидными группами 1-го и 4-го, 4-го и 7-го, 7-го и 10-го и так далее аминокислотных остатков. β- складчатая вторичная структура — белковая молекула лежит «змейкой», удаленные отрезки цепи оказываются поблизости друг от друга. В результате пептидные группы ранее удаленных аминокислот белковой цепи способны взаимодействовать при помощи водородных связей.
7 слайд

Описание слайда:
Участие водородных связей в формировании вторичной структуры Вторичная структура белков в виде β-складчатого слоя Под направлением белковой цепи понимают направление от N-конца (N-концевой аминокислоты) к C-концу (С-концевой аминокислоте) Укладка белка в виде α-спирали
8 слайд

Описание слайда:
Третичная структура белковых молекул Третичная структура белка — пространственная конфигурация спирали в пространстве. Эта структура поддерживается за счет гидрофобных взаимодействий, водородных, дисульфидных, ионных связей Глобулярные (шаровидные) белки Фибриллярные (нитевидные) белки Пример глобулярной структуры – белок альбумин, к классу альбуминов относят белок куриного яйца Пример фибриллярной структуры – белок фиброин – основной компонент натурального шелка и паутины
9 слайд

Описание слайда:
Четвертичная структура белка Четвертичная структура белка — способ укладки в пространстве отдельных полипептидных цепей, обладающих одинаковой (или разной) первичной, вторичной или третичной структурой, и формирование единого в структурном и функциональном отношениях макромолекулярного образования
10 слайд

Описание слайда:
Функции белковых молекул
11 слайд

Описание слайда:
Химические свойства белков Гидратация белков Молекулы белка связывают молекулы воды, проявляя гидрофильные свойства. Набухают, масса и объем белков увеличиваются. Могут образовывать сложные системы – студни. Пенообразование белков Белки образуют высококонцентрированные системы «жидкость-газ», называемые пенами. Горение белков Белки горят с образованием азота, углекислого газа и воды. Горение сопровождается характерным запахом жженых перьев.
12 слайд

Описание слайда:
Химические свойства белков Гидролиз белков – это расщепление молекулы белка до составляющих аминокислот
13 слайд

Описание слайда:
Химические свойства белков Денатурация белка — это процесс изменения вторичной, третичной и четвертичной структур белковой макромолекулы под влиянием внешних факторов (температуры, механического воздействия, действия кислот, щелочей, ультразвука и др.) Первичная структура и химический состав белка не меняются. Изменяются физические свойства: снижается растворимость, теряется биологическая активность. Процесс денатурации (коагуляции) белка сульфатом меди
14 слайд

Описание слайда:
Качественные реакции на белки Биуретовая реакция Ксантопротеиновая реакция
15 слайд

Описание слайда:
Тест по теме: «Белки» 1. Первичная структура белка удерживается: а) водородными связями; б) пептидными связями; в) гидрофобными связями; г) дисульфидными связями. 2. Вторичную структуру белковой молекулы поддерживают в основном … связи. а) водородные; б) ионные; в) пептидные; г) гликозидные. 3. Молекулы белков отличаются друг от друга: а) последовательностью чередования аминокислот; б) количеством аминокислот в молекуле; в) формой третичной структуры; г) всеми указанными особенностями. 4. Как поступают в клетки животных незаменимые аминокислоты? а) синтезируются в самих клетках; б) поступают вместе с пищей; в) поступают вместе с витаминами; г) поступают всеми указанными путями. 5. Полипептидная цепь, свернутая в клубок, – это … структура белка. а) первичная; б) вторичная; в) третичная; г) четвертичная.
16 слайд

Описание слайда:
Проверь себя! 1 2 3 4 5 б а г б в
17 слайд

Описание слайда:
Домашнее задание § 27 (с. 227-241) прочесть, ответить на вопросы 1-5 на стр. 241-242. Задание 10 на стр. 242 выполнить письменно. Решить предложенные задачи (по желанию, на оценку): 1. Вычислите массу соли, которую можно получить при взаимодействии 150 г 5%-ного раствора аминоуксусной кислоты с необходимым количеством гидроксида натрия. Сколько граммов 12%-ного раствора щелочи потребуется для реакции? 2. Навеску аминоуксусной кислоты разделили на две порции в соотношении 1:2. Меньшую порцию нейтрализовали избытком раствора гидроксида натрия. При этом образовалось 29,1 г соли. Какую массу сложного эфира можно получить из большей порции аминоуксусной кислоты, если массовая доля выхода эфира составляет 73%? Для реакции этерификации использовали этанол. Долгосрочное индивидуальное задание. Выполнить на выбор творческую работу: 1. Составить кроссворд на тему «Органические соединения» 2. Создать презентацию по теме «Превращения белков в организме»
18 слайд

Описание слайда:
Полезные ссылки по теме «Белки»: https://files.school-collection.edu.ru/dlrstore/5bc7baa2-0ff5-7ba3-5838-35fb7120ea4e/00148919052680926.htm https://him.1september.ru/ https://school-sector.relarn.ru/nsm/chemistry/Rus/chemy.html https://www.himhelp.ru/section25/section27kilur/section141/
19 слайд

Описание слайда:
Спасибо за урок!!!
Выберите книгу со скидкой:
БОЛЕЕ 58 000 КНИГ И ШИРОКИЙ ВЫБОР КАНЦТОВАРОВ! ИНФОЛАВКА
Инфолавка — книжный магазин для педагогов и родителей от проекта «Инфоурок»

Курс профессиональной переподготовки
Учитель химии

Курс повышения квалификации

Курс профессиональной переподготовки
Учитель биологии и химии
Найдите материал к любому уроку,
указав свой предмет (категорию), класс, учебник и тему:
также Вы можете выбрать тип материала:
Общая информация
Номер материала:
ДБ-390236
Вам будут интересны эти курсы:

