Аллотропия это какое свойство

Алмаз и графит — аллотропические формы углерода, отличающиеся строением кристаллической решётки
Аллотро́пия (от др.-греч. ἄλλος «другой» + τρόπος «поворот, свойство») — существование двух и более простых веществ одного и того же химического элемента.
Явление аллотропии обусловлено либо различным составом молекул простого вещества (аллотропия состава), либо способом размещения атомов или молекул в кристаллической решётке (аллотропия формы).
История[править | править код]
Понятие аллотропии введено в науку Й. Берцелиусом в 1841 году для обозначения разных форм существования элементов; одновременно он предполагал, по-видимому, применить его и к изомерии соединений. После принятия гипотезы А. Авогадро в 1860 году стало понятно, что элементы могут существовать в виде многоатомных молекул, например, О2 — кислород и О3 — озон.
В начале XX века было признано, что различия в кристаллической структуре простых веществ (например, углерода или фосфора) также являются причиной аллотропии. В 1912 году В. Оствальд отметил, что аллотропия элементов является просто частным случаем полиморфизма кристаллов, и предложил отказаться от этого термина. Однако по настоящее время эти термины используются параллельно. Аллотропия относится только к простым веществам, независимо от их агрегатного состояния; полиморфизм — только к твёрдому состоянию независимо от того, простое это вещество или сложное. Таким образом, эти термины совпадают для простых твёрдых веществ (кристаллическая сера, фосфор, железо и др.)[1].
Примеры аллотропии[править | править код]
Аллотропные модификации фосфора (белый, красный, жёлтый, чёрный фосфор)
В настоящее время известно более 400 разновидностей простых веществ. Способность элемента к образованию аллотропных форм обусловлена строением атома, которое определяет тип химической связи, строение молекул и кристаллов.
Как правило, большее число аллотропных форм образуют элементы, имеющие переменные значения координационного числа или степени окисления (олово, фосфор). Другим важным фактором является катенация — способность атомов элемента образовывать гомоцепные структуры (например, сера).
Склонность к аллотропии более выражена у неметаллов, за исключением галогенов, благородных газов, и полуметаллов.
Принято обозначать различные аллотропические формы одного и того же элемента строчными буквами греческого алфавита; причём форму, существующую при самых низких температурах, обозначают буквой α, следующую — β и т. д.
Неметаллы[править | править код]
| Элемент | Аллотропные модификации |
|---|---|
| Водород: | Молекулярный водород может существовать в виде орто- и пара-водорода. В молекуле орто-водорода o-H2 (т. пл. −259,10 °C, т. кип. −252,56 °C) ядерные спины параллельны, а у пара-водорода p-H2 (т. пл. −259,32 °C, т. кип. −252,89 °C) — антипараллельны. |
| Углерод: | Множество модификаций: алмаз, графит, фуллерен, карбин, графен, углеродные нанотрубки, лонсдейлит и др. Точное число модификаций указать затруднительно вследствие разнообразия форм связывания атомов углерода между собой. Наиболее многочисленны молекулярные структуры фуллеренов и нанотрубок. |
| Фосфор: | Известно 11 аллотропных модификаций фосфора. |
| Кислород: | Две аллотропные модификации: О2 — кислород и О3 — озон. |
| Сера: | Большое число аллотропных модификаций, второе место после углерода. |
| Селен: | Красный цикло-Se8, серый полимер Se и чёрный селен. |
Полуметаллы[править | править код]
| Элемент | Аллотропные модификации |
|---|---|
| Бор: | Бор существует в аморфном и кристаллическом видах. Аморфный бор — порошок бурого цвета. Обладает большей реакционной способностью, чем кристаллический бор. Кристаллический бор — вещество чёрного цвета. Известно более 10 аллотропных модификаций бора, которые кристаллизуются в ромбической и тетрагональной сингониях. Наиболее устойчивая модификация — β-ромбический бор — состоит из икосаэдров B12, которые образуют слои, объединенные в бесконечную структуру. |
| Кремний: | Различают две основные аллотропные модификации кремния — аморфную и кристаллическую. Решётка кристаллической модификации кремния — атомная, алмазоподобная. Также выделяют поликристаллический и монокристаллический кремний. |
| Мышьяк: | Три основные аллотропные модификации: жёлтый мышьяк (неметалл, состоящий из молекул As4 — структура, аналогичная белому фосфору), серый мышьяк (полуметаллический полимер), чёрный мышьяк (неметаллическая молекулярная структура, аналогичная красному фосфору). |
| Германий: | Две аллотропные модификации: α-Ge — полуметалл с алмазоподобной кристаллической решёткой и β-Ge — с металлической структурой, аналогичной β-Sn. |
| Сурьма: | Известны четыре металлических аллотропных модификаций сурьмы, существующих при различных давлениях, и три аморфные модификации (взрывчатая, чёрная и жёлтая сурьма), из которых наиболее устойчива металлическая форма серебристо-белого цвета с синеватым оттенком |
| Полоний: | Полоний существует в двух аллотропных металлических модификациях. Кристаллы одной из них — низкотемпературной — имеют кубическую решетку (α-Po), а другой — высокотемпературной — ромбическую (β-Po). Фазовый переход из одной формы в другую происходит при 36 °C, однако при обычных условиях полоний находится в высокотемпературной форме вследствие разогрева собственным радиоактивным излучением. |
Металлы[править | править код]
Среди металлов, которые встречаются в природе в больших количествах (до U, без Tc и Pm), 28 имеют аллотропные формы при атмосферном давлении: Li, Be, Na, Ca, Sc, Ti, Mn, Fe, Co, Sr, Y, Zr, Sn, La, Ce, Pr, Nd, Sm, Gd, Tb, Dy, Yb, Hf, Tl, Th, Pa, U.
Также важны аллотропные формы ряда металлов, образующиеся при их технологической обработке: Ti при 882˚C, Fe при 912˚C и 1394˚C, Co при 422˚C, Zr при 863˚C, Sn при 13˚C и U при 668˚C и 776˚C.
| Элемент | Аллотропные модификации |
|---|---|
| Олово: | Олово существует в трех аллотропных модификациях. Серое олово (α-Sn) мелкокристаллический порошок, полупроводник, имеющий алмазоподобную кристаллическую решётку, существует при температуре ниже 13,2 °С. Белое олово (β-Sn) — пластичный серебристый металл, устойчивый в интервале температур 13,2—161 °С. Высокотемпературное гамма-олово (γ-Sn), имеющее ромбическую структуру, отличается высокой плотностью и хрупкостью, устойчиво между 161 и 232 °С (температура плавления чистого олова). |
| Железо: | Для железа известны четыре кристаллические модификации: до 769 °C (точка Кюри) существует α-Fe (феррит) с объёмноцентрированной кубической решёткой и свойствами ферромагнетика; в температурном интервале 769—917 °C существует β-Fe, который отличается от α-Fe только параметрами объёмноцентрированной кубической решётки и магнитными свойствами парамагнетика; в температурном интервале 917—1394 °C существует γ-Fe (аустенит) с гранецентрированной кубической решёткой; выше 1394 °C устойчиво δ-Fe с объёмоцентрированной кубической решёткой |
| Лантаноиды: | Церий, самарий, диспрозий и иттербий имеют по три аллотропических модификации; празеодим, неодим, гадолиний и тербий — по две. |
| Актиноиды: | Для всех актиноидов, кроме актиния, характерен полиморфизм. Кристаллические структуры протактиния, урана, нептуния и плутония по своей сложности не имеют аналогов среди лантаноидов и более похожи на структуры 3d-переходных металлов. |
Энантиотропные и монотропные переходы[править | править код]
Переход одной аллотропной модификации в другую происходит при изменении температуры или давления (или одновременном воздействии обоих факторов) и связан со скачкообразным изменением свойств вещества. Этот процесс бывает обратимым (энантиотропным) и необратимым (монотропным).
Примером энантиотропного перехода может служить превращение ромбической серы в моноклинную α-S (ромб.) ↔ β-S (монокл.) при 95,6 °C. При обычной температуре стабильной является ромбическая модификация серы, которая при нагревании до 95,6 °С при нормальном давлении переходит в моноклинную форму. Последняя при охлаждении ниже 95,6 °С вновь переходит в ромбическую форму. Таким образом, переход одной формы серы в другую происходит при одной и той же температуре, и сами формы называются энантиотропными.
К монотропному переходу относится превращение белого фосфора P4 под давлением 1,25 ГПа и температуре 200 °C в более стабильную модификацию — чёрный фосфор. При возвращении к обычным условиям обратный переход не происходит. Переход из нестабильной формы в стабильную в принципе возможен при любой температуре, а обратный — нет, то есть определенная точка перехода отсутствует. Ещё один пример — превращение графита в алмаз при давлении 6 ГПа и температуре 1500 °C в присутствии катализатора (никель, хром, железо и другие металлы), то есть при условиях термодинамической устойчивости алмаза. Тогда как алмаз легко и быстро переходит в графит при температурах выше 1000 °С. В обоих случаях давление способствует превращению, поскольку образуется вещества с более высокой плотностью, чем исходные.
Три известные модификации олова переходят друг в друга различным образом. При обычных условиях устойчиво β-Sn (пластичное белое олово) с тетрагональной кристаллической решеткой[2]. Выше 173 °С β-Sn энантиотропно превращается в хрупкую модификацию γ-Sn, а ниже 13,2 °C β-Sn переходит монотропно в порошкообразное α-Sn (серое олово) с кубической решёткой типа алмаза. Этот полиморфный переход происходит с малой скоростью, но резко ускоряется в контакте с серым оловом — плотные куски белого олова рассыпаются в пыль («оловянная чума»). Обратный процесс возможен только путём переплавки.
Примечания[править | править код]
- ↑ Угай Я. А. Общая и неорганическая химия: Учеб. для студентов вузов, обучающихся по направлению и спец. «Химия». — М.: Высш. шк., 1997. — 524 с.: ил.
- ↑ Химическая энциклопедия: в 5 т. / Редкол.:Кнунянц И. Л. (гл. ред.). — Москва: Советская энциклопедия, 1992. — Т. 3. — С. 382. — 639 с. — 50 000 экз. — ISBN 5-85270-039-8
См. также[править | править код]
- Изомерия
- Полиморфизм кристаллов
- Кристаллическая решётка
Литература[править | править код]
- Эддисон У. Аллотропия химических элементов. — М.: Мир, 1966. — 207 с.
Ссылки[править | править код]
- Аллотропия // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
Химия изучает свойства и строение простых веществ. В большинстве своем они остаются неизменными в любых ситуациях. Однако есть ряд элементов, способных менять свои свойства в различных своих состояниях. Такое явление называется аллотропией. Знание о поведении элементов, подверженных аллотропии, расширяет понимание устройства мира и поведения в нем веществ и элементов.
Определение
Аллотропия — это возможность элемента трансформироваться в другой. В некоторых случаях даже в два или три. Если переводить название термина с греческого языка, то аллотропия — это «другое свойство». То есть буквальный перевод раскрывает сущность явления.
Виды аллотропии

Аллотропия, свойственная некоторым веществам, условно делится на два вида — по составу и по строению. В первом случае различно число атомов в молекуле. Во втором — строение кристаллической решетки.
В химии аллотропия — это изменение вещества независимо от того, жидкое оно, твердое или газообразное. Единственное отступление от терминологии появляется в работе с твердыми веществами, их строение сложнее, для их трансформации используется слово «полиморфизм», в переводе с греческого означающее «многообразный».
Каким веществам свойственна аллотропия
Не все вещества способны преобразоваться из сложных в простые даже под действием температур или других воздействий. Это может происходить только с теми из них, у которых есть способность к образованию гомоцепных структур или хорошо окисляющихся. Именно поэтому аллотропия веществ свойственна неметаллам. Хотя справедливости ради следует сказать, что есть металлы, способные преобразовываться в простые элементы, но это, скорее, полуметаллы.
Примеры аллотропии
Для понимания процесса существует ряд примеров преобразования вещества, причем оно бывает обратимым и необратимым. То есть вещество может после воздействия на него температуры или давления вернуться к первоначальному состоянию. Но бывает так, что оно остается в видоизмененном состоянии. Например, ромбическая сера — при нагревании ее до температуры 95,5 градуса по Цельсию она преобразуется в моноклинную форму. При снижении температуры до 95,5 градуса наступает обратное преобразование — из моноклинной формы в ромбическую.
Другой пример аллотропии — это изменение белого фосфора в черный. В данном случае для проведения преобразования требуется температура в 200 градусов по Цельсию и давление в 1,25 г Па. При воздействии тех же температур и давления на преобразованный черный фосфор он не сможет вернуться к первоначальному состоянию.
Как уже упоминалось, явление аллотропии свойственно и некоторым металлам. Но из-за сложности их структуры переходы из одного в другое состояние могут чередоваться. Например, в нормальных условиях белое олово является пластичным металлом, но при нагревании его при температуре 173 градуса по Цельсию оно перестраивает свою кристаллическую решетку до очень хрупкого состояния, а при снижении температуры до 13 градусов кристаллическая решетка принимает вид кубической алмазоподобной и делает вещество порошкообразным.
Модификации неметаллов

Самыми яркими и многообразными физическими свойствами аллотропии обладает углерод. Он способен перерождаться в самое большое количество аллотропных форм, причем с различными не только свойствами, но и строением кристаллической решетки. Взять, например, графит и алмаз. Формы одного вещества, но с разными строениями кристаллических решеток – графит чуть плотнее порошка, а алмаз — самое крепкое вещество на земле. И это уже не говоря об углеродных нанотрубках, лонсдейлите, фуллерене, карбине и других формах углерода.
Аллотропия характерна для серы. В нормальных условиях структура вещества моноклинная, а под воздействием температур может преобразоваться в пластическую и следом за этим в ромбовидную.
Фосфор способен изменяться в 11 форм. Причем 3 из них — белый, черный, красный — даже встречаются в природе, остальные можно получить искусственным путем. Отличается одна форма вещества от другой количеством атомов в молекуле. Различными цветами в химии представлен селен. Он также бывает серный, черный и красный.
Очень известная аллотропия — это кислород. Он видоизменяется до озона под действием температуры или электрического тока. Известный пример природного воздействия – молния. Во время разряда электрического поля кислород превращается в озон.
Модификации полуметаллов

Бор — это полуметалл, встречающийся в природе в аморфной и кристаллической форме. Но у него есть еще 10 известных науке форм.
Аморфным и кристаллическим бывает кремний. Сурьма в четырех формах по своей структуре представляется металлом, и в трех она аморфная, аллотропная.
Как и в случае с фосфором или селеном, мышьяк бывает серый или черный, в зависимости от формы – полимер или неметаллическая структура.
Модификации металлов

Самым широким спектром форм среди металлов обладает железо. В первом виде феррита, с характерной объемно-центрированной кубической кристаллической решеткой, железо способно существовать в температурных пределах от 0 до 769 градусов по Цельсию. Имеет свойства ферромагнетиков.
Второй тип феррита существует при температурах в диапазоне 769-917 градусов по Цельсию. Отличается объемно-центрированной кубической кристаллической решеткой. Магнетические свойства проявляет как парамагнетик.
Третий тип железа называется аустенит, характерен гранецентрированной кубической кристаллической решеткой. Способен существовать только при температурах от 917 до 1394 градусов по Цельсию. Магнитных свойств не имеет.
Четвертый тип железа возникает при температурах свыше 1397 градусов по Цельсию. Магнитных свойств не имеет, характерен объемно-центрированной кубической кристаллической решеткой.
Другой металл, имеющий несколько типов преобразования, — это олово. В аллотропной форме может существовать в виде порошка с кристаллической решеткой, подобной алмазной. Это так называемое серое олово. Есть и более привычная форма металла – белое олово. Оно встречается в виде пластичного метала серебряного цвета. Третья форма характерна тугоплавкостью, так как обладает ромбической кристаллической решеткой, называется она гамма-оловом.
Заключение

Все металлы, полуметаллы и неметаллы различных аллотропных типов с характерным строением кристаллических решеток, массой, количеством и зарядом протонов и нейтронов могут встречаться в природе в чистом, натуральном виде или получаются только в лаборатории. В обычных условиях они не сохраняют своей стабильности. Все это говорит о многообразии химических элементов и перспективах открытий новых доселе неизвестных науке форм и типов веществ. Такие исследования ведут к развитию всех отраслей жизнедеятельности человека.

Атомы одного и того же химического элемента могут образовывать несколько простых веществ. Это явление носит название аллотропии. (Термин «аллотропия» произошел от греческого словосочетания, означающего «другая форма». Он был введен в химическую литературу Я. Берцелиусом в 1841 г. Первоначально этим термином определялось явление существования химического элемента или соединения в твердом состоянии в нескольких кристаллических формах (модификациях). Я. Берцелиус ошибочно считал, что различные аллотропные формы элементов образуют в результате химических реакций различные вещества.) Аллотропные формы отличаются составом своих молекул (кислород О2 и озон О3), строением кристаллов (графит и алмаз) или направлением вращения атомных ядер в молекулах (ортоводород и параводород). Последний случай аллотропии характерен не только для водорода, но и для некоторых других двухатомных газов. Однако молекула Н2 имеет очень маленькую массу и направление вращения ядер в ту или иную сторону заметно влияет на ее свойства.
Самопроизвольное превращение одной аллотропной формы в другую представляет собой переход от структуры с более высокой внутренней энергией к структуре с меньшей внутренней энергией. При низких температурах устойчивыми являются те аллотропные формы, в которых частицы расположены ближе друг к другу и связаны между собой наибольшим числом химических связей. С повышением температуры амплитуда колебательного движения частиц возрастает и более устойчивыми оказываются аллотропные формы с большими межатомными расстояниями.
Теоретически любое изменение внешних условий должно приводить к перестройке взаимного расположения частиц в молекулах или кристаллических решетках. В действительности же мы наблюдаем на первый взгляд странную картину: при одинаковой температуре сосуществуют различные аллотропные формы одного и того же элемента. Так, например, озон О3 и кислород О2 могут сосуществовать во всех трех агрегатных состояниях. Однако никакого противоречия здесь нет. Просто мы не учли одно очень важное обстоятельство: чтобы произошел переход одной аллотропной формы в другую, необходимо первоначально затратить определенное количество энергии, которая называется энергией возбуждения или потенциальным барьером перехода. И если атомы не обладают такой энергией, то аллотропного превращения не происходит.
Аллотропия водорода
Ядра атомов, подобно электронам, обладают спином. Поэтому молекула, состоящая из двух одинаковых атомов, может находиться в двух различных формах в зависимости от того, параллельны ядерные спины или антипараллельны. Для молекул Н2 они получили название орто- и параводорода. Обычный водород при комнатной температуре содержит 25% параформы и 75% ортоформы. Это соотношение не изменяется с повышением температуры, так как переход Н2 (лара)→Н2 (орто), сопровождающийся поглощением небольшого количества теплоты, запрещен законами квантовой механики. Обратное превращение может протекать при низких температурах. Пропуская обычный водород сквозь слой охлажденного до 20К активированного угля, удается получить почти чистый параводсрод (99,7%).
Аллотропия кислорода
Простое вещество кислород при .обычных условиях может существовать в виде двух аллотропных модификаций — кислорода О2 и озона О3. Кислород является наиболее распространенной формой этого элемента. Он составляет приблизительно одну пятую часть всего объема земной атмосферы.
Как показывают магнитные исследования, молекула О2 имеет два неспаренных электрона. В соответствии с этим ее строение можно выразить следующей структурной формулой:

Благодаря наличию нескольких ковалентных связей молекула кислорода очень устойчива; ее диссоциация на атомы становится заметной лишь при температуре выше 2000°С. Поскольку масса молекулы О2сравнительно невелика, кислород имеет низкие температуры плавления (-218,9°С) и кипения ( — 183°С). Его растворимость в воде при обычных условиях составляет примерно 3 мл в 100 мл.
Образование озона наблюдается во всех химических процессах, сопровождающихся выделением атомного кислорода, а также при действии на молекулярный кислород быстрых электронов и протонов, рентгеновских и ультрафиолетовых лучей. Его возникновение можно изобразить в виде схемы:

или суммарно:
3О2 = 2О3 — Q
В природе озон образуется при грозовых разрядах и в процессе окисления некоторых смол. На высоте 10—30 км над поверхностью Земли имеется тонкий слой озона, обеспечивающий возможность биологической жизни на Земле. Он задерживает идущее от Солнца жесткое ультрафиолетовое излучение и отражает инфракрасные лучи Земли, препятствуя ее охлаждению.
Молекула озона имеет угловую форму и небольшой дипольный момент:

Поскольку молекулы O3 обладают относительно большой массой и сложным строением, озон характеризуется более
высокими температурами кипения и плавления, чем кислород. Этим же объясняется интенсивная окраска жидкого и твердого озона и его хорошая растворимость в воде.
Озон является неустойчивым соединением и при большой концентрации способен распадаться со взрывом. Он обладает гораздо более высокой окислительной способностью, чем молекулярный кислород. Так, уже при обычных условиях озон окисляет серебро, ртуть и многие другие вещества:
8Ag+2O3= 4Ag2O + O2
Для качественного обнаружения озона обычно пользуются его реакцией с иодидом калия:
2KI + O3 + Н2O = I2 + 2КОН + О2
С молекулярным кислородом О2 эта реакция не идет. Существует и другой, более простой и оригинальный метод качественного определения озона, основанный на его способности быстро разрушать резину. Если тонкую резиновую полоску натянуть в озонированном воздухе, она разрывается в течение нескольких секунд.
В последнее время озон находит все более широкое и разнообразное применение. Он используется для устранения неприятных запахов, обеззараживания питьевой воды и стерилизации перевязочных материалов. Благодаря исключительно высокой окислительной способности озон применяется для получения органических кислот, быстрого старения вин и выдерживания табака.
Аллотропия серы
 Элементная сера существует в виде нескольких аллотропных форм. При температуре ниже 95,6°С устойчивой является ромбическая сера, для которой характерна высокая растворимость в неполярных органических растворителях, например в сероуглероде CS2. Плотность этой формы равна 2,07 г/см3. Кристаллы ромбической серы построены из восьми атомных молекул S8, имеющих форму короны (рис. 5).
Элементная сера существует в виде нескольких аллотропных форм. При температуре ниже 95,6°С устойчивой является ромбическая сера, для которой характерна высокая растворимость в неполярных органических растворителях, например в сероуглероде CS2. Плотность этой формы равна 2,07 г/см3. Кристаллы ромбической серы построены из восьми атомных молекул S8, имеющих форму короны (рис. 5).
Рис. 5. Строение кольцевых молекул S8
 В интервале температур 95,6÷119,3°С (темп, пл.) устойчива моноклинная или призматическая сера. Ее плотность составляет 1,96 г/см3. Кристаллы моноклинной и ромбической серы отличаются взаимной ориентацией молекул S8. Переход ромбической серы в моноклинную может занимать от нескольких минут до нескольких часов. При быстром нагреве ромбическая сера не успевает полностью перейти в моноклинную и плавится при 112,8°C.
В интервале температур 95,6÷119,3°С (темп, пл.) устойчива моноклинная или призматическая сера. Ее плотность составляет 1,96 г/см3. Кристаллы моноклинной и ромбической серы отличаются взаимной ориентацией молекул S8. Переход ромбической серы в моноклинную может занимать от нескольких минут до нескольких часов. При быстром нагреве ромбическая сера не успевает полностью перейти в моноклинную и плавится при 112,8°C.
Есть еще две аллотропные модификации серы, нерастворимые в сероуглероде. Это пластичная и пурпурная сера; первая получается при быстром охлаждении расплава серы, а вторая — при быстром охлаждении ее паров, нагретых до высокой температуры.
Рис. 6. Изменение вязкости жидкой серы в зависимости от температуры
Рассмотрим превращения, происходящие с серой при постепенном повышении температуры выше температуры ее плавления. В интервале от t°пл до 155° C в расплаве присутствуют в основном молекулы S8. Эти сравнительно небольшие и почти сферические частицы легко смещаются друг относительно друга, благодаря чему вязкость жидкой серы при этих температурах сравнительно невелика (рис. 6). Начиная со 155—159°C происходит процесс полимеризации — кольца (S8) разрываются и соединяются в длинные цепи:

Образующиеся цепочки скручиваются, переплетаются и утрачивают способность свободно перемещаться с повышением температуры концентрация полимерных цепочек возрастает, а их средняя длина увеличивается. Расплав серы становится все более вязким, а его цвет изменяется от оранжево-желтого до темно-коричневого. При 187— 195°с вязкость серы достигает наибольшего значения. Ее не удается даже вылить из сосуда. Максимальная длина цепочек соответствует молекулярной массе 3•107 у. е., что составляет около миллиона атомов серы.
С увеличением температуры выше 200°C полимерные цепочки начинают постепенно уменьшаться и вязкость серы понижается. Если такой расплав вылить в холодную воду, образуется пластичная сера. Она имеет аморфную структуру и не растворяется в CS2.
Пластичная сера очень быстро превращается в ромбическую модификацию.
При обычном давлении сера кипит при 444°C; образующиеся пары содержат циклические молекулы S8. с увеличением температуры появляются частицы с меньшей массой: S6, S4, S2. Изменение состава молекул вызывает постепенное обесцвечивание паров серы. Выше 900°C в парах присутствуют только двухатомные молекулы S2. Они представляют собой электронные аналоги молекул O2 и содержат два неспаренных электрона:
![]()
Выше 1500°C молекулы S2 начинают диссоциировать на отдельные атомы
S2 + Q⇄ S + S
Аллотропия фосфора
Атомы фосфора могут образовывать двухатомные, четырех атомные и полимерные молекулы. Двухатомные молекулы аналогичны по своему электронному строению молекулам азота:
![]()
Они существуют при температурах выше 1000°C. В жидком состоянии, в растворе, а также в парах ниже 1000°C
устойчивы четырехатомные молекулы Р4, имеющие форму тетраэдра (рис. 10). Каждый атом фосфора в такой молекуле связан ковалентными связями с тремя другими атомами и имеет неподеленную пару электронов.
 Рис. 10 . Строение молекул Р4
Рис. 10 . Строение молекул Р4
Конденсируясь, пары фосфора образуют белый фосфор — воскообразное бесцветное вещество, растворимое в сероуглероде, бензоле, диэтиловом эфире и некоторых других органических жидкостях; его плотность 1,828 г/см3, темп. пл. 44,1 °С, темп. кип. 280,5 °С. Белый фосфор имеет молекулярную кристаллическую решетку, в узлах которой расположены тетраэдрические молекулы Р4. Поскольку связи Р—Р в молекулах Р4 довольно легко рвутся, белый фосфор является исключительно реакционноспособным веществом. При температуре, близкой к 40°С, он самопроизвольно воспламеняется на воздухе, образуя густой белый «дым» оксида Р2О5:
Р4 + 5O2 = 2Р2O5 + Q
Медленное окисление белого фосфора (например, под водой) сопровождается характерным свечением — фосфоресценцией. Желтоватая окраска, появляющаяся при его длительном хранении, объясняется постепенным превращением белого фосфора в красный. Этот переход ускоряется под действием рентгеновских и ультрафиолетовых лучей, а также в присутствии катализатора — молекулярного иода I2.
 Рис. 11 . Структура черного фосфора
Рис. 11 . Структура черного фосфора
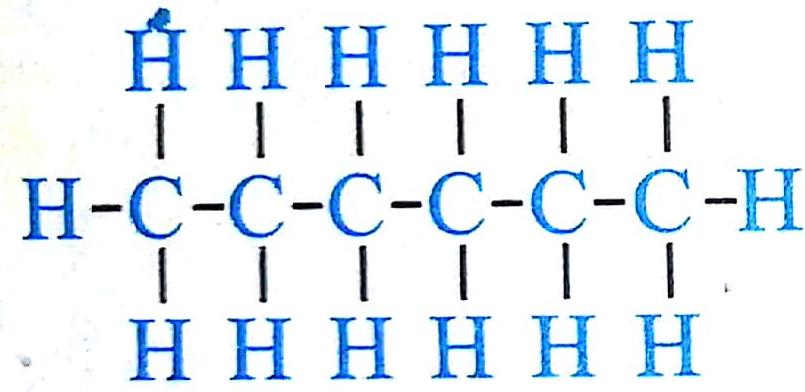
Красный фосфор получают из белого, нагревая последний до 275—340°С без доступа воздуха. Он гораздо устойчивее, чем белый фосфор: не растворяется ни в одном из известных растворителей и не воспламеняется при нагревании на воздухе до 240°С. В зависимости от условий получаются различные формы красного фосфора. Его цвет может меняться от темно-коричневого до красного или фиолетового; плотность изменяется в интервале 2,0—2,4 г/см3, а температура плавления — от 585 до 600°С. Красный фосфор построен из длинных цепей, в которых каждый атом связан с тремя другими соседними атомами:
![]()
На концах макромолекул находятся атомы кислорода галогенов или группы ОН. При 500—600°С полимер начинает медленно разлагаться и испаряться, причем образующиеся пары содержат тетраэдрические молекулы Р4. Наиболее устойчивой модификацией является черны фосфор, получающийся из белого при 200°С и 12•108 н/м2
Белый фосфор (t°, P) nР4 →(Р)4n Черный фосфор
Его можно обрабатывать на воздухе, не опасаясь воспламенения; он загорается лишь выше 400°С. По внешнему виду черный фосфор напоминает графит, но является полупроводником. Его кристаллы построены из волнистых слоев (рис. 11). При нагревании до 550°С он самопроизвольно превращается в красный, а с повышением давления переходит в металлическое состояние.
Аллотропия углерода
 Существуют три аллотропных модификации углерода: алмаз, графит и карбин. Другие хорошо известные формы углерода — сажа, кокс, древесный и каменный уголь — представляют собой аморфные образования с графитоподобной структурой.
Существуют три аллотропных модификации углерода: алмаз, графит и карбин. Другие хорошо известные формы углерода — сажа, кокс, древесный и каменный уголь — представляют собой аморфные образования с графитоподобной структурой.
Алмаз — это бесцветное полимерное тело, превосходящее по твердости все известные вещества. Каждый
Рис. 13. Природные кристаллы алмаза
атом углерода образует четыре одинаковые ковалентные связи, направленные из центра правильного тетраэдра к его вершинам. В такой трехмерной структуре нельзя выделить какие-либо отдельные группы атомов; все атомы совершенно равноценны. Поскольку на образование химических связей затрачиваются все наружные электроны атомов углерода, кристалл алмаза является изолятором.
Алмазы встречаются чаще всего в виде октаэдров с округленными плоскостями (рис. 13). Благодаря высокой светопреломляющей способности они переливаются всеми цветами радуги. Окрашенные за счет посторонних примесей голубые и розовые алмазы в природе очень редки. Зато черные непрозрачные кристаллы (карбонадо), обладающие повышенной твердостью, составляют около половины всех добываемых алмазов.
 Рис. 18. Кристаллическая решетка идеального графита
Рис. 18. Кристаллическая решетка идеального графита
Рис. 14. Структура графита
Алмазы находят самое различное применение. Наиболее крупные и красивые кристаллы дополнительно шлифуют и под названием «бриллианты» используют для изготовления дорогих украшений. Масса бриллиантов выражается в каратах; один карат равен 0,2 г. Самый крупный из когда-либо найденных алмазов, до того как он был распилен на более мелкие куски, весил 2024 карата.
Крупные бриллианты очень часто остав?
